蒸发和结晶、重结晶 知识点题库
-
(1) 实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌; ⑤停止加热.其正确的操作顺序为
-
(2) 如何运用最简方法检验溶液中有无SO42﹣离子? .如果有,应该如何除去SO42﹣离子?
-
(3) 在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止.请问这步操作的目的是
-
(4) 将经过操作(3)后的溶液过滤.请问这一操作能除掉哪些杂质?
-
(5) 实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时: .过滤时: .蒸发时: .
)CuSO4•5H2O是铜的重要化合物,有着广泛的应用.以下是CuSO4•5H2O的实验室制备流程图.
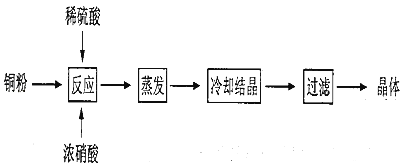
根据题意完成下列填空:
-
(1) 向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:
-
(2) 如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4•5H2O中可能存在的杂质是
-
(3) 已知:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
称取0.1000g提纯后的CuSO4•5H2O试样于锥形瓶中,加入0.1000mol/L氢氧化钠溶液啊28.00mL,反应完全后,过量的氢氧化钠用0.1000mol/L盐酸滴定至终点,耗用盐酸20.16mL,则0.1000g该试样中含CuSO4•5H2O g.
-
(4) 如果采用重量法测定CuSO4•5H2O的含量,完成下列步骤:
① ②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)
在过滤前,需要检验是否沉淀完全,其操作是
选项 | 异常情况 | 可能的原因 |
① | 蒸发结晶时,蒸发皿破裂 | 将溶液蒸干或酒精灯灯芯碰到蒸发皿底部 |
② | 分液时,分液漏斗中的液体很难滴下 | 没有打开分液漏斗颈上的玻璃塞或塞上的凹槽与漏斗上的小孔没有对齐 |
③ | 萃取时,振荡溶液,静置不分层 | 萃取剂加得太多 |
④ | 蒸馏时,发现冷凝管破裂 | 没有通冷凝水或先加热后通冷凝水 |
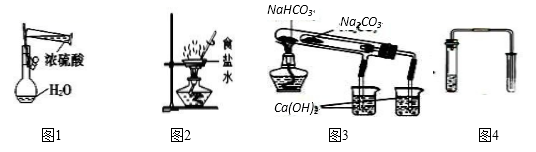
-
(1) 对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、加热分解等。
下列各组混和物的分离或提纯应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
②提取碘水中的碘,用方法。
③除去食盐溶液中的水,可采用的方法。
④淡化食盐水,可采用的方法。
⑤除去氧化钙中的碳酸钙可用的方法
-
(2) ①分离沸点不同但又互溶的液体混合物,常用什么方法?试举例说明。。
-
(3) 在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。 。
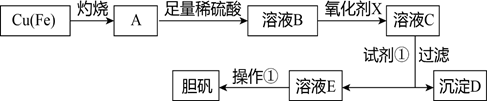
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀 | 2.7 | 7.5 | 4.4 |
| 完全沉淀 | 3.7 | 9.7 | 6.7 |
请回答:
-
(1) 溶液B中含有的阳离子有(填离子符号)。
-
(2) 下列物质中最适宜做氧化剂X的是(填字母)。
a.NaClO b.H2O2 c.KMnO4
-
(3) 加入试剂①是为了调节pH,要调整pH范围是,则试剂①可以选择(填化学式)。
-
(4) 沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是(用离子方程式表示)。
-
(5) 溶液E经过操作①可得到胆矾,操作①为、过滤、洗涤。
-
(6) 已知溶液中c(Cu2+)与pH的关系为lgc(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1mol/L,此时溶液中的Fe3+能否沉淀完全:(填“能”或“否”) 。
-
(1) 工业上制取纯净的CuCl2·2H2O的主要过程是
①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;
②对①所得滤液按下列步骤进行操作:
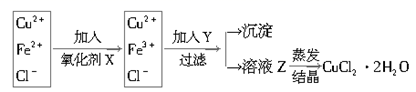
已知:
物质
Fe(OH)2
Cu(OH)2
Fe(OH)3
Ksp/25 ℃ mol3·L-3
8.0×10-16
2.2×10-20
4.0×10-38
完全沉淀时的pH范围
≥9.6
≥6.4
3~4
请回答下列问题:
①加入的氧化剂X,下列物质最好选用的是 .
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②加入Y的作用是,Y的化学式为。
③溶液乙在蒸发结晶时应注意:。
-
(2) 如图为相互串联的甲、乙两个电解池,试回答下列问题:
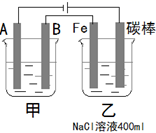
甲池若为用电解原理精炼铜的装置,阴极增重19.2 g,则乙池阳极放出气体在标准状况下的体积为L(不考虑气体的溶解情况)
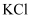 和
和  (溶解过滤,再蒸发结晶)
D . 氮气和氧气(蒸馏)
(溶解过滤,再蒸发结晶)
D . 氮气和氧气(蒸馏)
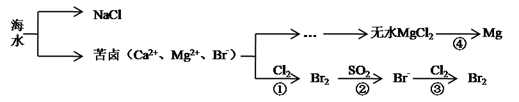
-
(1) 淡化海水的方法有(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、(填化学式),之后(填操作名称),再加入适量(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
-
(2) 反应④由无水MgCl2制取金属镁的常用工业方法是。
-
(3) 向苦卤中通入Cl2置换出Br2 , 再用空气吹出溴并用SO2吸收,转化为Br- , 反复多次,
以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是。
-
(4) 工业上也可以用Na2CO3溶液吸收吹出的Br2 , 生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式,最后再用H2SO4处理所得溶液重新得到Br2。
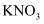 晶体含有少量
晶体含有少量  杂质,可用溶解、蒸发结晶的方法提纯
杂质,可用溶解、蒸发结晶的方法提纯 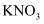 B . 用移液管移取25.00mL待测液时,若移液管内残留少量液体,必须用洗耳球将其吹出,否则使测量结果偏低
C . 用酸性
B . 用移液管移取25.00mL待测液时,若移液管内残留少量液体,必须用洗耳球将其吹出,否则使测量结果偏低
C . 用酸性  溶液鉴别苯和甲苯
D . 用
溶液鉴别苯和甲苯
D . 用 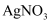 溶液鉴别
溶液鉴别  溶液和
溶液和 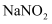 溶液
溶液
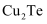 )、三氧化二铬(
)、三氧化二铬(  )以及少量的金(
)以及少量的金( 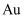 ),可用于制取
),可用于制取 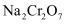 溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下: 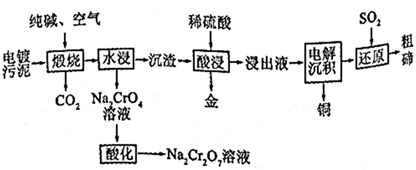
已知:煅烧时, 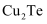 发生的反应为:
发生的反应为: 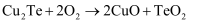
-
(1)
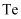 元素在元素周期表中的位置为,该元素最高化合价。
元素在元素周期表中的位置为,该元素最高化合价。
-
(2) 煅烧时,
 发生反应的化学方程式为。
发生反应的化学方程式为。
-
(3) 浸出液中除了含有
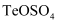 (在电解过程中不反应)外,还含有(填化学式)。电解沉积过程中析出单质铜的电极为极。
(在电解过程中不反应)外,还含有(填化学式)。电解沉积过程中析出单质铜的电极为极。
-
(4) 工业上用重铬酸钠(
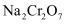 )母液生产重铬酸钾(
)母液生产重铬酸钾(  )的工艺流程如图所示:
)的工艺流程如图所示: 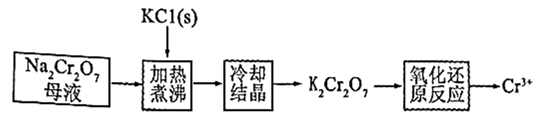
通过冷却结晶能析出大量
 的原因是。
的原因是。 -
(5) 测定产品中
 含量的方法如下:称取试样
含量的方法如下:称取试样 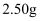 配成
配成 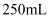 溶液,取
溶液,取 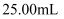 置于锥形瓶中,加入足量稀硫酸和几滴指示剂,用
置于锥形瓶中,加入足量稀硫酸和几滴指示剂,用 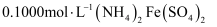 标准液进行滴定。滴定过程中发生反应的离子方程式为。若三次实验消耗
标准液进行滴定。滴定过程中发生反应的离子方程式为。若三次实验消耗  标准液的体积平均为
标准液的体积平均为 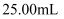 ,则所得产品中
,则所得产品中  的纯度为。
的纯度为。
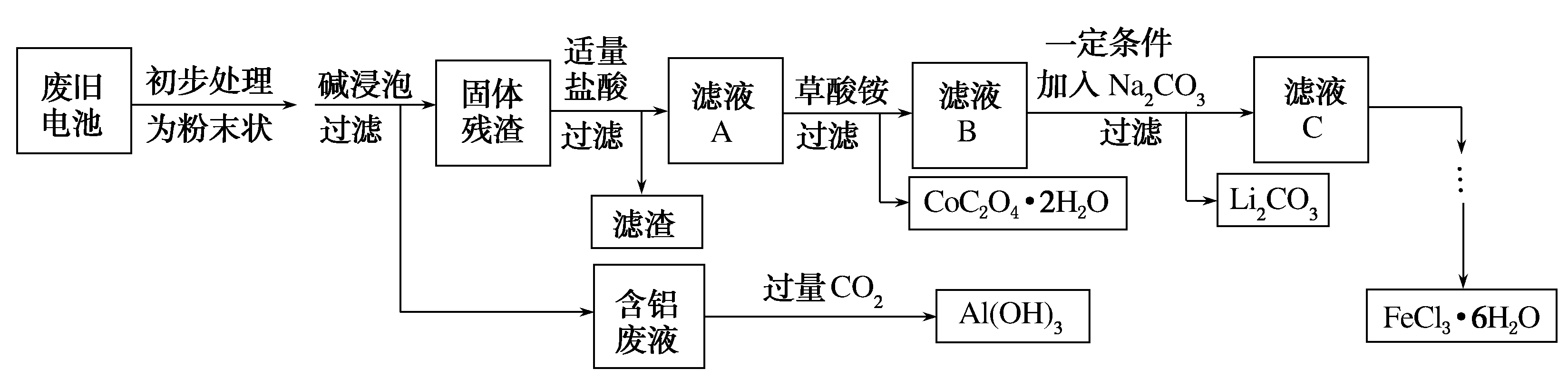
请回答下列问题:
-
(1) LiCoO2中Co元素的化合价为。
-
(2) 请写出“碱浸”过程中所发生反应的化学方程式。
-
(3) 加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+。请写出该反应的离子方程式:,过滤后所得滤渣的主要成分为(写化学式)。
-
(4) 已知Fe3+能与C2O
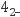 结合成[Fe(C2O4)3]3- , [Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+ , 该过程中(填“有”或“没有”)发生元素化合价的变化;从FeCl3溶液中得到FeCl3·6H2O晶体的操作是:往溶液中加入适量盐酸后,蒸发浓缩、冷却结晶、、洗涤、干燥。
结合成[Fe(C2O4)3]3- , [Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+ , 该过程中(填“有”或“没有”)发生元素化合价的变化;从FeCl3溶液中得到FeCl3·6H2O晶体的操作是:往溶液中加入适量盐酸后,蒸发浓缩、冷却结晶、、洗涤、干燥。
-
(5) 已知Ksp(Li2CO3)=8×10-4 , 滤液B中c(Li+)=0.2mol/L。要生成Li2CO3沉淀,则加入的等体积的Na2CO3溶液中,c(CO
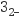 )不低于mol/L(忽略溶液混合引起的体积变化),检验滤液中含有Na+的实验方法为。
)不低于mol/L(忽略溶液混合引起的体积变化),检验滤液中含有Na+的实验方法为。
-
(1) 苯甲酸在A、B、C三种溶剂中的溶解度(S)随温度变化的曲线如图所示:
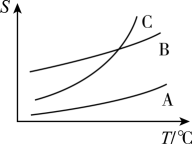
重结晶时,合适的溶剂是。 重结晶过程中,趁热过滤的作用是。洗涤时采用的合适洗涤剂是(填字母)。
A.饱和食盐水 B.Na2CO3溶液 C.稀硫酸 D.蒸馏水
-
(2) 检验乙烯时可用溴的四氯化碳溶液或用溴水,其现象的不同是。
-
(3) 实验室制取乙炔的反应方程式是。
选项 | 实验操作和现象 | 结论 |
A | 重结晶法提纯苯甲酸,主要步骤为:加热溶解、趁热过滤、冷却结晶、过滤、洗涤、干燥 | 苯甲酸在水中的溶解度受温度的影响较大 |
B | 在试管中滴入10~15滴溴乙烷,再加入1mL5%NaOH溶液,振荡后加热,静置分层后取少量上层水溶液于另一支试管中,加入2滴AgNO3溶液,有浅黄色沉淀生成 | 溴乙烷水解生成溴化钠 |
C | 在圆底烧瓶中加入20mL乙醇和浓硫酸的混合液,加热迅速升温到170℃,将生成的气体先通入NaOH溶液,再通入溴的四氯化碳溶液中,溶液褪色 | 乙醇发生消去反应生成乙烯 |
D | 在试管中先加入2mL10%CuSO4溶液,再加入5滴5%NaOH溶液,得到新制的Cu(OH)2 , 振荡后加入0.5mL乙醛溶液,加热后得到砖红色沉淀 | 乙醛具有还原性 |
 , 含有少量
, 含有少量 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( ),工艺流程如下:
),工艺流程如下: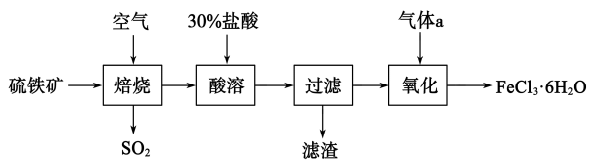
已知:氯化铁晶体受热会生成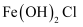 , 最后得到
, 最后得到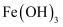 。
。
请回答下列问题:
-
(1) 焙烧时为加快反应速率可采取的方法(答出两点即可)。
-
(2) 焙烧时反应的化学方程式为
 , 则
, 则 的化学式为。酸溶时反应的化学方程式为。
的化学式为。酸溶时反应的化学方程式为。
-
(3) 氧化时通入的气体
 为(填化学式),反应的离子方程式为。
为(填化学式),反应的离子方程式为。
-
(4) 制取
 晶体的操作包括蒸发浓缩、、过滤。烘干时需要减压烘干,原因是。
晶体的操作包括蒸发浓缩、、过滤。烘干时需要减压烘干,原因是。
-
(5) 焙烧排出的尾气中主要含
 、
、 、
、 , 可用于尾气处理的试剂有(填字母)
, 可用于尾气处理的试剂有(填字母)a.浓硫酸 b.
 溶液 c.
溶液 c.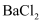 溶液 d.
溶液 d. 溶液
溶液
- 分解因式:x3−4xy2= ▲ .
- sin15°cos15°=___________.
- 下列说法正确的是( ) A.因为SO2有漂白性,所以它能使品红溶液、溴水、KMnO4溶液褪色 B.能使品红
- 已知椭圆以双曲线的焦点为顶点,以双曲线的顶点为焦点。 (1)求椭圆的方程; (2)若直线与椭圆相交于点,两点(,不是左右
- 右图是自然界碳循环简图,请回答(I)含碳单质矿物燃烧的化学方程式为______________; (2)海水吸收二氧化碳
- 法国化学家库尔特瓦在一次实验中,偶然发现海藻灰溶液(主要成分为Nal)与浓硫酸混合时产生一种美丽的紫色蒸气,从而发现了碘
- 如图,若程序框图输出的S是254,则判断框①处应为 A. B. C. D.
- 图甲是小明家的一台速热电热水壶,在壶中装入0.6kg、20℃的水,断开其他用电器只接入此壶,4min将水烧开(标准大气压
- 2010年10月1日下午18时59分57秒,中国探月二期工程先导星“嫦娥二号”在西昌点火升空,准确入轨,赴月球拍摄月球表
- The disc,digitally in the studio,sounded fantastic a
- 白细胞能吞噬绿脓杆菌,与这一现象有关的是 ( ) A、主动运输 B
- To be honest, every season of the year I do ___________watch
- 江苏省常州市横山桥高级中学10-11学年高二上学期期中考试(英语 It would be ________(有益的)
- 实蝇的黑背对彩背为显性,基因位于常染色体上,黑背纯合子致死;红腹对黑腹为显性,基 因位于X染色体上。一只彩背红腹雄蝇和一
- 下图所示实验操作正确的是 ( ) A.过滤 B.倾倒液体 C.检查气密性 D.加热液体
- 下列句中没有通假现象的一项是( ) A.虽有槁暴 B.则知明而行无过矣 C.君
- 在矩形ABCD中,点P在AD上,AB=2,AP=1.将直角尺的顶点放在P处,直角尺的两边分别交AB,BC于点E,F,连接
- 宁夏新闻网讯:2009年4月9日,宁夏回族自治区党委、政府在吴忠市隆重召开“沿黄城市带(群)建设”启动大会,正式拉开了打
- 近几年来,珠江流域持续干旱,江河水位显著偏低,海水倒灌,咸潮上溯,给珠江三角洲的澳门、珠海、中山、广州等地供水造成很大影
- 绿色开花植物要形成果实和种子,必须经过的两个必要生理过程是( ) A.开花和传粉 B.开花和受精 C.传粉和



