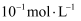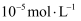蒸发和结晶、重结晶 知识点题库
蒸发操作中必须用到蒸发皿,下面对蒸发皿的操作中正确的是( )
A . 将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热
B . 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
C . 将蒸发皿放置在三脚架上直接用酒精灯火焰加热
D . 在三脚架上放置泥三角,将蒸发皿放置在泥三角上加热
在蒸发皿中蒸发液体,下列操作不正确的是( )
A . 直接用酒精灯的外焰加热蒸发皿
B . 加热过程中不断用玻璃棒搅拌
C . 加热到液体全部消失
D . 蒸发皿中出现多量晶体、少量液体时,停止加热,利用蒸发皿的余热烘干
下列操作中正确的是( )
A . 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B . 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部.
C . 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D . 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
如图1可实现由亚硫酸钠和硫粉反应制硫代硫酸钠(Na2S2O3).已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如图2.下列说法错误的是( )
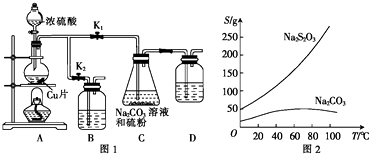
A . 盛装浓硫酸的仪器的名称为分液漏斗
B . B、D中都可以盛放氢氧化钠溶液,防止污染
C . 该装置设计不够严密,可能会出现倒吸
D . 析出硫代硫酸钠晶体的方法是蒸发结晶
净水剂能够改善水质,给人们的生活、健康带来很大的益处。
-
(1) 明矾[KAl(SO4)2·12H2O]是常见的净水剂。其在水中的电离方程式为;明矾可净水是因为在天然水中生成胶状Al(OH)3 , Al(OH)3具有的作用。
-
(2) 碱式氯化铝(简称BAC)是高效净水剂的主要成分。实验室模拟利用铝土矿(主要含Al2O3 , 还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝[Al2(OH)nCl6-n]的过程如下:
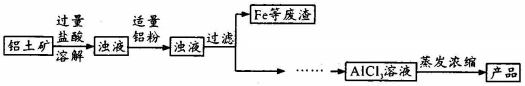
①盐酸溶解铝土矿过程中,发生反应的离子方程式为、;溶解过程中需不断搅拌,目的是。
②加适量铝粉的主要作用是。
③蒸发浓缩所需玻璃仪器为。
下列实验操作能达到实验目的的是( )
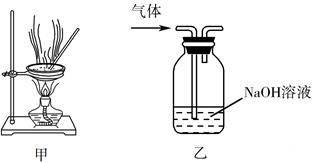
A . 用经水湿润的pH试纸测量溶液的pH
B . 将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度,配制1.000 mol·L−1NaOH溶液
C . 用装置甲蒸干AlCl3溶液制无水AlCl3固体
D . 用装置乙除去实验室所制乙烯中的少量SO2
粗盐中含有不溶性的泥沙,可溶性的CaCl2、MgCl2及Na2SO4等杂质。
-
(1) 经过溶解、、蒸发等操作可将粗盐初步提纯;
-
(2) 在蒸发过程中需要用到的仪器有铁架台、酒精灯、玻璃棒和;
-
(3) 检验粗盐中是否含有SO42-所用的试剂是和。
硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
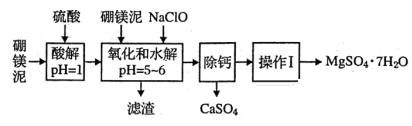
-
(1) 实验中需用1mol/L的硫酸480mL,若用18.4mol/L的浓硫酸来配置,量取浓硫酸时需使用的量筒规格为()。
A 10mL B 20mL C 50mL D 100mL
-
(2) 加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-还有一种离子也会被NaClO氧化,该反应的离子方程式为;滤渣中除含有氢氧化铁、氢氧化铝外还有。
-
(3) 在“除钙”前需检验滤液中Fe3+是否被除尽,简述检验方法。
-
(4) 已知硫酸镁、硫酸钙的溶解度如下表
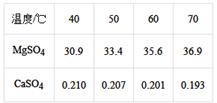
“除钙”是将;硫酸镁和硫酸钙混合溶液中的硫酸钙除去根据上表数据,采取的操作是、趁热过滤、、,便得到比较纯净的硫酸镁。
-
(5) 实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2g,则MgSO4·7H2O的产率为。
下列实验操作正确的是( )
A . 用pH试纸测定某溶液的pH时,需预先用蒸馏水湿润pH试纸
B . 蒸馏石油时为了更好地控制温度,应将温度计的水银球伸入液面以下
C . 蒸发结晶时不能将溶液全部蒸干,应该在有大量晶体析出时停止加热
D . 稀释浓硫酸时,可向盛有浓硫酸的烧杯中直接加蒸馏水
Ⅰ、选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解 C.结晶法 D.分液法 E.渗析法 F.蒸馏法 G.过滤法
-
(1) 分离水和煤油的混合物。
-
(2) 分离水和酒精。
-
(3) 分离溴水中的溴和水。
-
(4) 上述仪器中,在配制稀H2SO4时不需要使用的有(填代号),还缺少的仪器是;
-
(5) 经计算,需浓H2SO4的体积为;如果实验室有15mL、20mL、50mL的量筒应选用mL的量筒最好,量取时俯视量筒读数将使浓度(“偏高”、“偏低”、“无影响”);
-
(6) 将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌的目的是,若未冷却至室温便将溶液转移至容量瓶会使浓度偏。
关于下列实验装置的说法正确的是( )
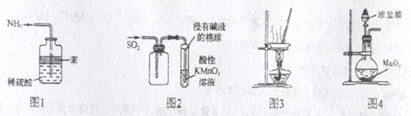
A . 用图1吸收多余氨气且防止倒吸
B . 用图2收集SO2并验证其还原性
C . 图3蒸干NH4Cl饱和溶液制备NH4Cl晶体
D . 用图4实验室制取氯气
硫酸四氨合铜晶体([Cu(NH3)4]SO4·H2O)常用作杀虫剂,媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。常温下该物质溶于水,不溶于乙醇、乙醚,在空气中不稳定,受热时易发生分解。某化学兴趣小组以Cu粉、3mol/L的硫酸、浓氨水、10% NaOH溶液、95%的乙醇溶液、0.500 mol/L稀盐酸、0.500 mol/L的NaOH溶液来合成硫酸四氨合铜晶体并测定其纯度。
-
(1) I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL 3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
A仪器的名称为。
-
(2) 某同学在实验中有1.5g的铜粉剩余,该同学将制得的CuSO4溶液倒入另一蒸发皿中加热浓缩至有晶膜出现,冷却析出的晶体中含有白色粉末,试解释其原因。
-
(3) II.晶体的制备
将上述制备的CuSO4溶液按如图所示进行操作
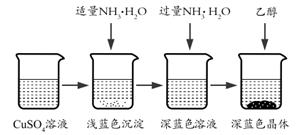
已知浅蓝色沉淀的成分为Cu2(OH)2SO4 , 试写出生成此沉淀的离子反应方程式。
-
(4) 析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是。
-
(5) III.氨含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V1mLClmol/L的盐酸标准溶液完全吸收。取下接收瓶,用C2mol/L NaOH标准溶液滴定过剩的HCl(选用甲基橙作指示剂),到终点时消耗V2mLNaOH溶液。
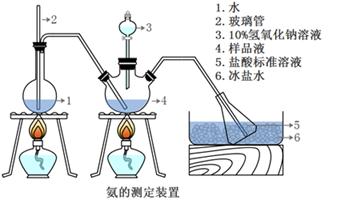
玻璃管2的作用,样品中氨的质量分数的表达式。
-
(6) 下列实验操作可能使氨含量测定结果偏低的原因是____________________。A . 滴定时未用NaOH标准溶液润洗滴定管 B . 读数时,滴定前平视,滴定后俯视 C . 滴定过程中选用酚酞作指示剂 D . 取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁
利用乙醚、95%乙醇浸泡杜仲干叶,得到提取液,进步获得绿原酸粗产品的种工艺流程如下,下列说法不正确的是( )
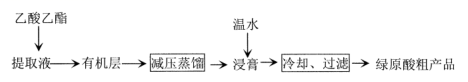
A . 常温下,绿原酸易溶于水
B . 浸膏的主要成分是绿原酸
C . 减压蒸馏的目的是降低蒸馏温度,以免绿原酸变质
D . 绿原酸粗产品可以通过重结晶进一步提纯
下列实验操作能达到实验目的的是 ( )
A . 用热的碳酸钠溶液洗涤试管内壁的油污
B . 需将 pH 试纸润湿来测定 Na2CO3 溶液 pH
C . 蒸发 AlCl3 溶液获得无水 AlCl3
D . 用 CCl4 从溴水中萃取溴时,先从分液漏斗下端管口放出有机层,再放出水层
下列有关实验装置的叙述正确的是( )
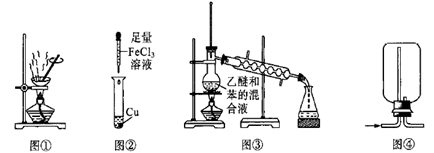
A . 用图①装置蒸发KCl溶液制备KCl晶体
B . 用图②装置比较Fe、Cu的金属性强弱
C . 用图③装置分离乙醚和苯
D . 用图④装置收集H2、CH4、NO等气体
结晶操作中需要用到的仪器是( )
A . 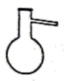 B .
B .  C .
C . 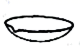 D .
D . 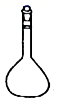
 B .
B .  D .
D . 
下列实验设计能达到实验目的的是( )
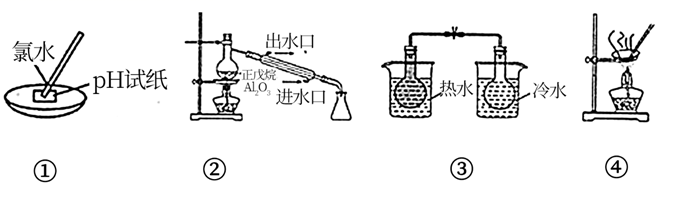
A . ①用于测量氯水的  B . ②可以探究正戊烷(
B . ②可以探究正戊烷( 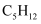 )催化裂化
C . ③可用于探究温度对
)催化裂化
C . ③可用于探究温度对 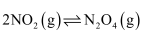 平衡移动的影响
D . ④用
平衡移动的影响
D . ④用  溶液制备
溶液制备  晶体
晶体
 B . ②可以探究正戊烷(
B . ②可以探究正戊烷( 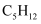 )催化裂化
C . ③可用于探究温度对
)催化裂化
C . ③可用于探究温度对 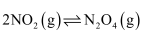 平衡移动的影响
D . ④用
平衡移动的影响
D . ④用  溶液制备
溶液制备  晶体
晶体
下列有关说法正确的是( )
A . CaCO3(s) =CaO(s)+CO2(g) 在室温下不能自发进行,说明该反应  H<0
B . 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
C . 0.1mol·L-1Na2CO3溶液在50℃时的碱性比25℃强,说明盐类水解反应是放热反应
D . 蒸发FeCl3溶液,所得固体在坩埚中充分加热,最后得到Fe2O3固体
H<0
B . 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
C . 0.1mol·L-1Na2CO3溶液在50℃时的碱性比25℃强,说明盐类水解反应是放热反应
D . 蒸发FeCl3溶液,所得固体在坩埚中充分加热,最后得到Fe2O3固体
 H<0
B . 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
C . 0.1mol·L-1Na2CO3溶液在50℃时的碱性比25℃强,说明盐类水解反应是放热反应
D . 蒸发FeCl3溶液,所得固体在坩埚中充分加热,最后得到Fe2O3固体
H<0
B . 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
C . 0.1mol·L-1Na2CO3溶液在50℃时的碱性比25℃强,说明盐类水解反应是放热反应
D . 蒸发FeCl3溶液,所得固体在坩埚中充分加热,最后得到Fe2O3固体
下列实验中,所选装置不合理的是( )
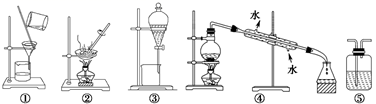
A . 粗盐提纯,选①和②
B . 分离食用油和水的混合液,选④
C . 用NaOH溶液吸收少量Cl2 , 选⑤
D . 用CCl4提取溴水中的溴,选③
碲被誉为现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁。工业上从某电镀污泥(含有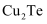 、
、 以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
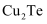 、
、 以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。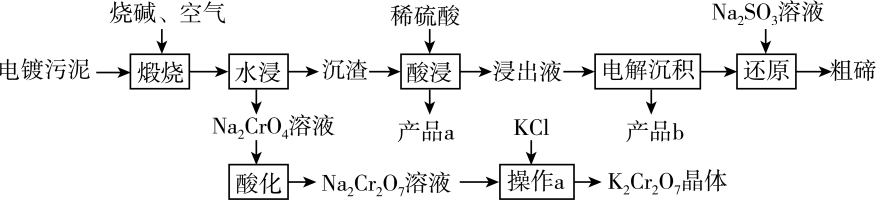
已知:①沉淀时 与pH的关系
与pH的关系
| pH | |
开始沉淀 |
| 3.68 |
沉淀完全 |
| 5 |
②溶解度
溶解度 |
| NaCl |
100℃ | 95.1g | 39.8g |
25℃ | 4.6g | 36g |
回答下列问题:
-
(1) “煅烧”时气体与固体原料逆流而行,目的是;“煅烧”时
 发生反应的化学方程式为。
发生反应的化学方程式为。
-
(2) 金在(填操作单元名称)过程中回收。已知浸出液中含有
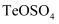 , 每得到128g碲,理论上消耗
, 每得到128g碲,理论上消耗 溶液的体积为L。
溶液的体积为L。
-
(3) 根据相关物质溶解度特点分析“操作a”的步骤:向
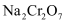 溶液中加入KCl固体,(填操作名称,下同),使NaCl结晶析出后,再得到
溶液中加入KCl固体,(填操作名称,下同),使NaCl结晶析出后,再得到 晶体。
晶体。
-
(4) 铬(VI)毒性很高,工业上常用铁和石墨作电极,处理含
 的酸性废水。通电后
的酸性废水。通电后 先转变为
先转变为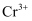 , 一段时间后变成
, 一段时间后变成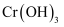 沉淀而被除去。其中铁电极的作用是电子导体和,当电解后溶液中
沉淀而被除去。其中铁电极的作用是电子导体和,当电解后溶液中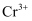 浓度为
浓度为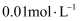 时,其开始沉降时废水的pH为。
时,其开始沉降时废水的pH为。
最近更新
- 阅读下列材料 材料一 楚越之地(长江流域及江南一带),地广人稀,饭稻羹鱼,或火耕水
- 观察图中的小旗,说出船相对岸上楼房的运动情况可能有哪几种,并简要说明其中的道理。
- 每个人都不完美 (15分) ①每个人对于自己要成为一个什么样的人,都应该有一个自我设计。但这种设计应该是相对模糊的,是不
- 下列商业部门与下图中所属城镇对应正确的是( )A.甲为普通服装店、乙为家具商店、丙为星级宾馆 B.甲为早点店、乙为
- 2010年我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥二号”卫星成功送入太空,“嫦娥二号”绕月探测飞行。现已知
- 是硫的原子结构示意图,其核电荷数为 A.2 B.6 C.
- 根据拼音写出相应的词语。(4分) ⑴须晴日,看红装素裹,分外yāo ráo( )。 ⑵牛背上牧童
- “三个代表”重要思想创造性地回答了( ) A、社会主义道路的建设问题 B、社会主义初级阶段理论问题 C
- 下列有关生态系统结构的叙述,正确的是() A.每种生物在生态系统中只能处在一个营养级上 B.动物都属于消费者,其中食草动
- 已知某原子的实际质量为Mg,又知碳原子的质量为N g ,则该原子的相对原子质量为 ( ) A.
- (本小题10分)云南省是我国花卉产业大省,一年四季都有大量鲜花销往全国各地,花卉产业已成为我省许多地区经济发展的重要项目
- 锌片和碳棒用导线连接后插入稀硫酸中,锌片是 A.阴极 B.正极 C.阳极
- 12.有学者认为,自中国古代进入文明社会,先后出现了“方国联盟(内服外服)”等三种政治统治模式。据此,与下图匹配的正确选
- 生态文明的发展是建立在生产力、科学技术的快速进步以及人类对自然的改造能力的不断提高的基础上的,是继采猎文明、农耕文明、工
- 假设某化学反应的反应过程如下图表示,观察分析,符合图中变化的化学反应为( )A.A2+3B22AB3
- 已知硫酸亚铁溶液中加入过氧化钠时发生反应: 4Fe2++4Na2O2+6H2O= 4Fe(OH)3↓+O2↑+8Na+
- 汽车需求量(Q)随着汽车价格(P)、汽车购置税(T)、汽油价格(E)、居民收入(I) 的变动而变动。下列曲线图中正确反映
- 聚美优品通过开辟化妆品网上销售的蓝海区域(指未知的市场空间),首创“化妆品团购”模式,同时承诺“百分百正品”以及“拆封3
- SEOUL, Sept. 26 (Xinhua) — Hundreds of families from the two
- 鉴于塑料购物袋已成为“白色污染”的主要来源,2008年1月国务院办公厅下发《关于限制生产销售使用塑料购物袋的通知》,要求