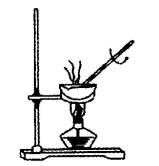
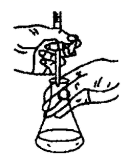
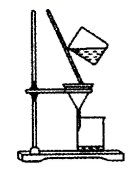
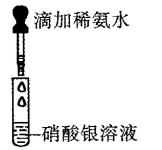
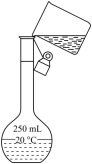
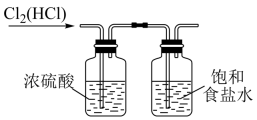
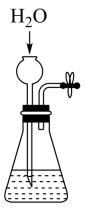
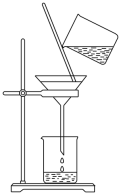
过滤 知识点题库
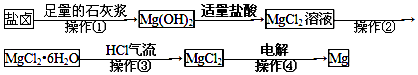
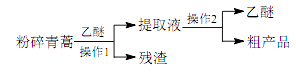
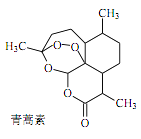
根据上述信息分析,下列判断或叙述中肯定错误的是( )
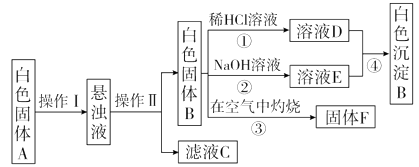
-
(1) 操作Ⅱ所需要的玻璃仪器有、、。
-
(2) 写出下列反应的方程式:
③的化学方程式:,
④的离子方程式:。
-
(3) 根据实验推测,该胃药的主要成分为。
-
(4) 该同学通过阅读课外读物了解到:常用胃药中除了上述实验已检出的物质外,还有NaHCO3 , 请你帮助该同学完成对滤液C中主要成分的探究实验(简要描述操作步骤):。
 B . 稀释
B . 稀释 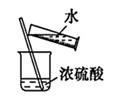 C . 尾气处理
C . 尾气处理 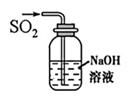 D . 蒸发结晶
D . 蒸发结晶 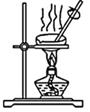
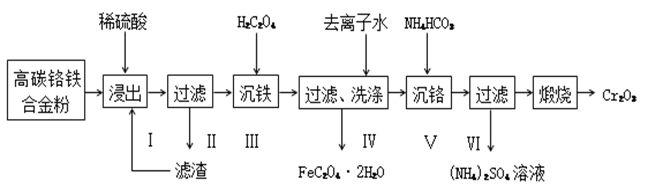
已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
-
(1) 步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是(写一点);浸取铬时反应的离子方程式为。
-
(2) 步骤Ⅱ滤渣返回再次浸取的目的是。
-
(3) 步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图所示:
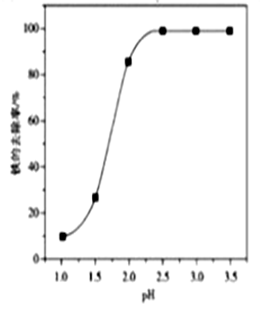
pH小于2.3时,铁去除率低,其原因是。
-
(4) 步骤Ⅳ能说明沉淀已洗涤干净的操作是。
-
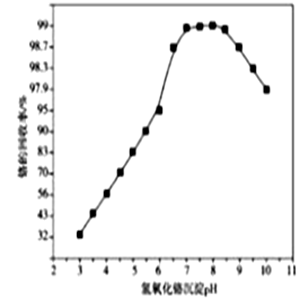
(5) 步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为;沉铬时,溶液pH与铬的回收率关系如图所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是。
 B . 分离氢氧化铁胶体和氯化钠溶液
B . 分离氢氧化铁胶体和氯化钠溶液  C . 实验室中制取少量蒸馏水
C . 实验室中制取少量蒸馏水 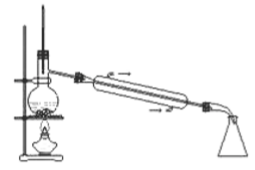 D . 配制100mL0.10mol﹒L-1盐酸
D . 配制100mL0.10mol﹒L-1盐酸 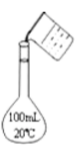
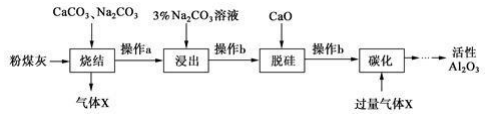
已知烧结过程的产物主要是NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
-
(1) 写出烧结过程中铝元素转化的化学方程式。
-
(2) 操作 a 为冷却、研磨,其中研磨的目的是。
-
(3) ①浸出过程中, NaFeO 2 可完全水解,生成沉淀为。
②3%Na2 CO3溶液显(填 “酸性 ”、 “碱性 ”或“中性 ”),请用离子方程式解释:。
-
(4) 操作b 所用的玻璃仪器有漏斗、、。
-
(5) “碳化”时,通入过量气体 x 主要成分的化学式为。
-
(6) 工业上电解Al2O3制备 Al 是为使Al2O3在较低温下融化,通常加入。电解过程中做阳极的石墨易消耗,原因是。
| A | B | C | D |
| 蒸拌原料 | 淀粉发酵 | 清水浸淋 | 放置陈酿 |
| | | | |
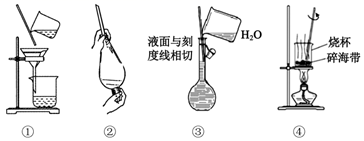
| A | B | C | D |
| | | | |
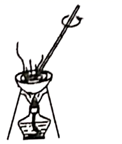
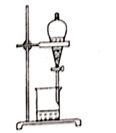
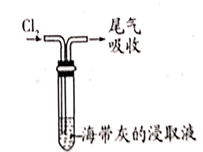
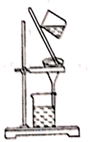
| 干海带烧灼为海带灰 | 分离海带灰的浸取液 | 氧化碘离子为碘单质 | 分四离四氯化碳中的碘 |
|
|
|
|
A.蒸发除去苯甲酸中的乙醇 | B.用氢氧化钠溶液滴定醋酸溶液 | C.除去水中的苯酚 | D.配制银氨溶液 |
 Li2S +4H2O。已知:Li2S易潮解,在加热条件下易被空气中的O2氧化。实验室用粗锌(含少量铜、FeS)和稀硫酸反应制备H2。
Li2S +4H2O。已知:Li2S易潮解,在加热条件下易被空气中的O2氧化。实验室用粗锌(含少量铜、FeS)和稀硫酸反应制备H2。
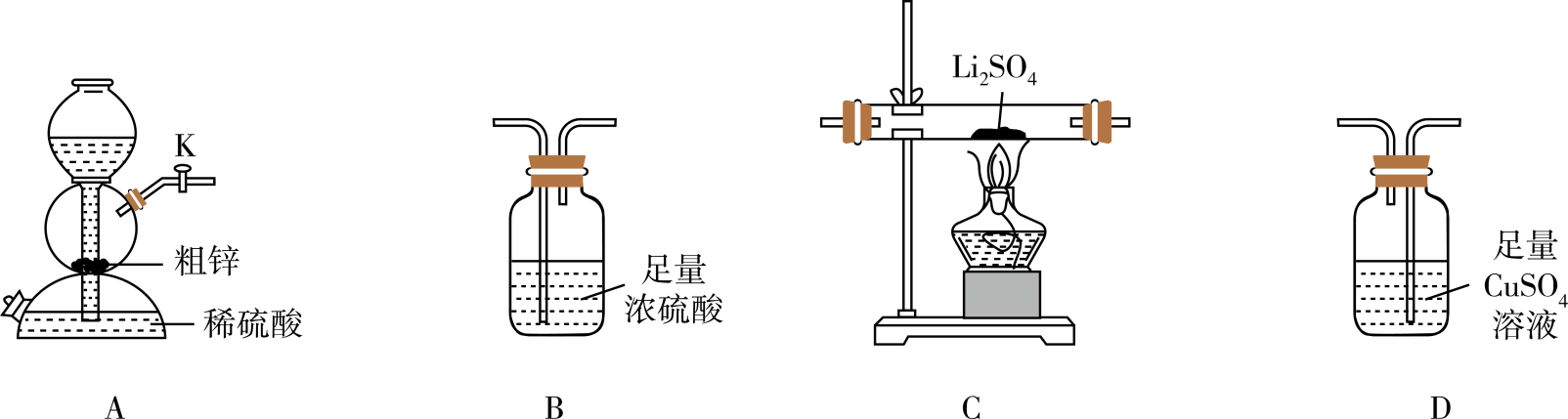
请回答下列问题:
-
(1) 按气流从左至右,装置的连接顺序是A→ (填字母)。
-
(2) 其他条件相同,粗锌与稀硫酸反应比纯锌 (填“快"或“慢”)。实验中观察到装置D中产生黑色沉淀,其离子方程式为。
-
(3) 利用装置A制氢气的主要优点是,还可用该装置制备的下列气体是 (填字母)。
A.SO2:70%硫酸、亚硫酸钠粉末 B.CO2:稀盐酸、大理石
C.NH3:浓氨水生石灰 D.Cl2:浓盐酸、二氧化锰
-
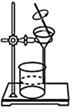
(4) 实验完毕后,采用图1、图2(夹持装置已略去)装置对装置A中混合物进行分离可得到副产物皓矾(ZnSO4·7H2O)晶体。先选择图1装置进行过滤,并将滤液进行蒸发浓缩、降温结晶,再选择图2装置过滤,得到粗皓矾晶体。
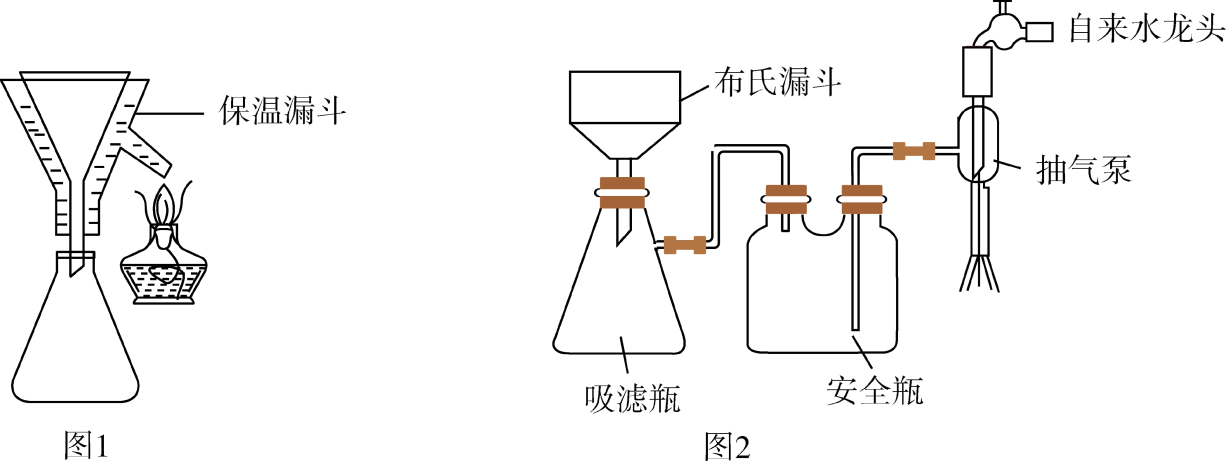
下列有关说法正确的是____(填字母)。
A . 采用图1装置过滤的优点是避免析出ZnSO4·7H2O B . 采用图1装置过滤主要是分离FeSO4·7H2O和ZnSO4溶液 C . 粗皓矾晶体中可能含少量CuSO4·5H2O杂质 D . 采用图2装置过滤的优点是过滤速度快 -
(5) 欲探究Li2S产品的成分,现进行如下实验:
实验
操作与现象
结论
Ⅰ
取少量Li2S样品,滴加足量的稀盐酸,将气体通入品红溶液中,溶液褪色
样品含Li2SO3
Ⅱ
在实验Ⅰ的溶液中滴加BaCl2溶液,产生白色沉淀
样品含
①由上述实验I可知,Li2S样品中含有杂质(填化学式),产生该杂质的原因可能是。
②测定产品纯度的方法:取w g Li2S样品加入V1 mLc1 mol·L-1稀硫酸(过量)中,充分反应后,煮沸溶液以除去残留的酸性气体;滴加酚酞溶液作指示剂,用c2mol·L-1标准NaOH溶液滴定过量的硫酸,消耗NaOH溶液V2 mL。若该Li2S样品中杂质不参加反应,用上述方法测得的Li2S样品的纯度为%(用含V1、V2、c1、c2、w的代数式表示)。
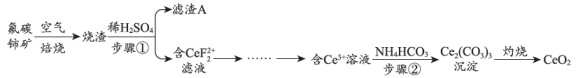
下列说法错误的是( )
 =Ce(CO3)3↓+3CO2↑+3H2O
=Ce(CO3)3↓+3CO2↑+3H2O
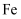 )去除含氮废水中的硝酸盐(
)去除含氮废水中的硝酸盐( )是环境修复的重要方法。一种去除
)是环境修复的重要方法。一种去除 的过程如下。
的过程如下。
-
(1) Ⅱ中充分反应后,分离混合物的方法是。
-
(2) Ⅱ中反应的离子方程式是。
-
(3) 实验发现,在Ⅱ中补充一定量的
 可以明显提高
可以明显提高 的去除率。向两份含氮废水[
的去除率。向两份含氮废水[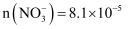
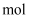 ]中均加入足量
]中均加入足量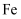 粉,做对比研究。
粉,做对比研究。实验序号
ⅰ
ⅱ
所加试剂
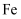 粉
粉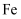 粉、
粉、 (
( )
) 的去除率
的去除率≈50%
≈100%
分析ⅱ中
 的去除率提高的原因:
的去除率提高的原因:a.
 直接还原
直接还原 了。
了。通过计算说明电子得、失数量关系:,证明该原因不合理。
b.研究发现:
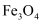 (导电)覆盖在铁粉表面;随着反应的进行,产生
(导电)覆盖在铁粉表面;随着反应的进行,产生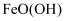 (不导电),它覆盖在
(不导电),它覆盖在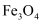 表面,形成钝化层,阻碍电子传输。
表面,形成钝化层,阻碍电子传输。c.
 能与
能与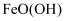 反应生成
反应生成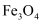 。
。用
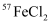 做同位素示踪实验,证明该原因合理。
做同位素示踪实验,证明该原因合理。d.
 破坏钝化层。
破坏钝化层。将ⅱ中的
 替换为,
替换为, 的去除率约为50%,证明该原因不合理。
的去除率约为50%,证明该原因不合理。 -
(4) ⅰ、ⅱ中均能发生
 。该反应明显有助于ⅰ中
。该反应明显有助于ⅰ中 的去除,结合方程式解释原因:。
的去除,结合方程式解释原因:。
-
(5) 测定
 含量
含量步骤1.取v
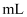 含氮(
含氮( )水样,加入催化剂、
)水样,加入催化剂、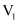
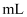
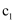

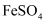 标准溶液(过量),再加入稀
标准溶液(过量),再加入稀 。
。步骤2.用
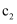

 标准溶液滴定剩余的
标准溶液滴定剩余的 (
( 被还原为
被还原为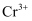 ),终点时消耗
),终点时消耗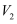
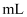 。
。已知:
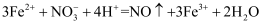
①水样中
 的含量为
的含量为 。
。②溶液中
 影响测定。向步骤1中加入适量
影响测定。向步骤1中加入适量 , 产生
, 产生 驱赶
驱赶 , 否则会使测定结果(填“偏大”或“偏小”)。
, 否则会使测定结果(填“偏大”或“偏小”)。
A | B | C | D |
|
|
|
|
溶液的配制 | 氯气的净化 | 检查装置的气密性 | 沉淀的过滤 |
- 请从下列物质中选择适当的物质填空(填字母编号): A.活性炭 B.酒精 C.氦气 D.氯化钠 E氮气
- 某公共汽车5分钟一班准时到达某站,则任意一人在该车站等车时间少于3分钟的概率为( )A.
- 如图,在梯形ABCD中,AD∥BC,∠B=∠ACD.(1)证明:△ABC∽△DCA;(2)若AC=6,BC=9,求AD长
- 下列句子没有语病的一项( ) A.为了全面提升办学水平,育才中学决定加快创建文明校园的规模与速度。 B.为了杜绝校园事
- 输送4800kW的电功率,分别采用120kV高压和240V电压输电,输电线上的电流之比是多少?损失的电功率之比是多少?
- 阅读下面的文字,完成16~18题。
- 如图13,∠1=∠2 ,CF⊥AB ,DE⊥AB ,求证:FG∥BC 证明:因为CF⊥AB ,DE⊥AB ( ) 所以
- 下列关于特异性免疫的叙述,正确的是 A.机体受抗原刺激后,T细胞不直接参与攻击抗原 B.细胞免疫中T细胞分泌的淋巴因子能
- 若方程表示椭圆,则的取值范围是
- What the doctor really doubts is_____my mother will recover
- 汽车轮胎的表面制成凹凸花纹,其作用是通过 来增大摩擦;自行车刹车时,用力捏闸能增大闸皮与车轮间的
- 计算:4cos30°+
- 下面的资料为某种植物体(注1)进行光合作用的速率记录,请回答下列有关光合作用与生物钟的问题:测量时间(h) 0 6 12
- 2.下列各组词语书写全部正确的一项是( ) A.寥廓 胸臆 掺和 橘子州头 B.侘傺 遏制 翱游 峥嵘岁月 C
- Four interesting festivals Grand Old Days Phone numeber: (65
- 下面关于细胞器分布的说法,正确的是 A.植物细胞都具有叶绿体 B.动物细胞都具有中心体 C.原核生物没有细胞器
- 15.某有机物X能发生水解反应,水解产物为Y和Z。同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是()A.
- 汉译英。每空一词。 1.玛丽把她的新朋友介绍给我们。 Mary________hernew friend _______
- 阅读下面两则新闻材料,然后作文。 (1)中国国家防汛抗旱总指挥部4月9日发布消息说,受近期降雨影响,重庆市农业旱情基本解
- A、B、C、D、E五个景点之间的路线如图所示。若每条路线的里程a (km)及行驶的平均速度b (km/h)用(a,b)表