过滤 知识点题库
A.过滤法 B.分液法
C.蒸馏法 D.结晶法
①分离水和豆油的混合物;
②从含有硝酸钾和少量氯化钾的混合溶液中获得硝酸钾;
③分离饱和食盐水和沙子的混合物;
④分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃),已知四氯化碳和甲苯互溶。
步骤一:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入Na2CO3溶液,加热、过滤、洗涤、干燥、称量,质量记为m1。
步骤二:FeSO4的制备。将上述铁屑加入到一定量的稀硫酸中,充分反应后过滤并用少量热水洗涤锥形瓶和滤纸。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量记为m2。
步骤三:硫酸亚铁铵的制备。准确称取所需质量的(NH4)2SO4加入“步骤二”中的蒸发皿中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥,称量所得晶体质量。
步骤四:用比色法测定硫酸亚铁铵的纯度。
回答下列问题:
-
(1) 步骤三中称取的(NH4)2SO4质量为。
-
(2) ①铁屑用Na2CO3溶液处理的目的是。
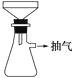
制备FeSO4溶液时,用右图装置趁热过滤,原因是。
②将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机是。
③比色法测定硫酸亚铁铵纯度的实验步骤为:Fe3+标准色阶的配制、待测硫酸亚铁铵溶液的配制、比色测定。标准色阶和待测液配制时除均需加入少量稀盐酸外,还应注意的问题是。
④该实验最终通过确定硫酸亚铁铵产品等级。
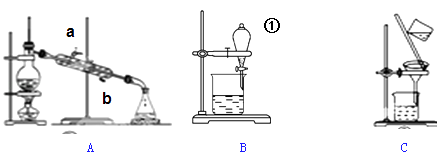
根据上图装置回答下列问题:
-
(1) 若用装置A分离CCl4和溴苯的混合物(已知CCl4和溴苯互溶,沸点分别为76.75℃和156.2℃),在实验时冷却水从冷凝管的(填“a”或“b”)端通入;温度计读数为80℃时,锥形瓶中收集到的物质是.
-
(2) 装置B中仪器①的名称是,用装置B分离混合物时,为使液体顺利流下,应进行的操作是.
-
(3) 粗盐中含有少量泥沙、MgCl2、CaCl2及硫酸盐,将粗盐溶解后,先用装置C将泥沙除去,除去泥沙后还需进一步提纯,粗盐提纯步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl3溶液;③加入过量的NaOH溶液;④调节溶液PH等于7;⑤溶解;⑥过滤;⑦蒸发.正确的操作顺序是 .A . ⑤②③①⑥④⑦ B . ⑤①②③⑥④⑦ C . ②①③④⑥⑦ D . ⑤③②①⑥④⑦
 B . 除去氯化钠晶体中混有的I2晶体:
B . 除去氯化钠晶体中混有的I2晶体: 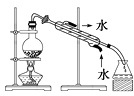 C . 分离CCl4中的Br2:
C . 分离CCl4中的Br2: 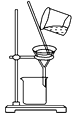 D . 除去CO2气体中的HCl气体:
D . 除去CO2气体中的HCl气体: 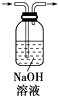
| 选项 | 物质 | 杂质 | 试剂 | 主要操作 |
| A | K2CO3 | KHCO3 | 无 | 加热 |
| B | CuO | Al2O3 | 氨水 | 过滤 |
| C | I2 | H2O | 乙醇 | 萃取 |
| D | CO2 | HCl | 饱和Na2CO3溶液 | 洗气 |
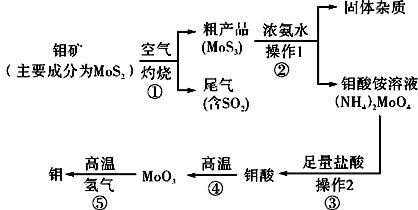
-
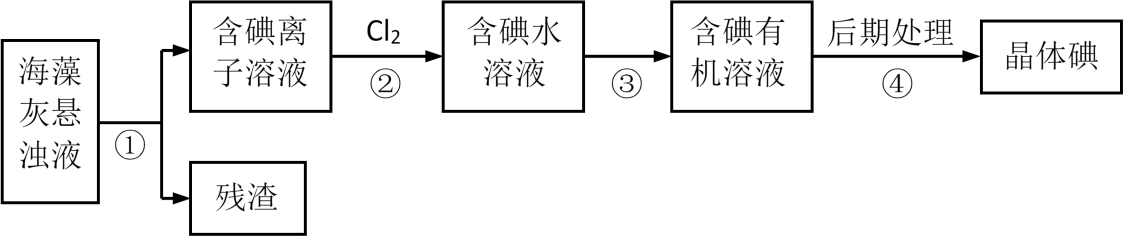
(1) 反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂:。
-
(2) 如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有:。
-
(3) 钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式为。
-
(4) 工业上制备还原性气体CO和H2的反应原理为CO2+CH4
 2CO+2H2 , CH4+H2O
2CO+2H2 , CH4+H2O  CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为。
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为。
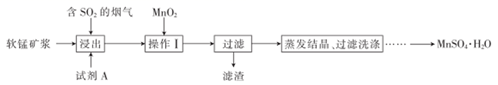
已知:浸出液中的金属离子主要是Mn2+ , 还含有少量的Fe2+。回答下列问题:
-
(1) 实验室进行过滤操作时用到的玻璃仪器有玻璃棒、。
-
(2) 浸出后,锰主要以Mn2+的形式存在,写出相应反应的离子方程式:。
-
(3) 浸出过程的副反应之一是部分SO2被氧化为硫酸,致使浸出液的pH下降,这将不利于软锰矿浆继续吸收SO2。欲消除生成的硫酸,可选用的试剂A是________(填字母)。A . MnCO3 B . MnO2 C . Mn(OH)2 D . MnSO4
-
(4) 操作I的目的是和调节溶液的pH至3~4。检验过滤后的滤液中是否含有Fe3+的操作是。
-
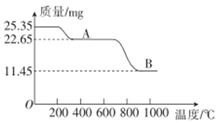
(5) 通过煅烧MnSO4·H2O可制得软磁铁氧体材料(MnxO4),在不同温度下煅烧MnSO4·H2O时剩余固体质量变化的曲线如图所示。根据图中数据可得MnxO4中x的值为。A到B过程中分解得到的气体中SO2与SO3的物质的量之比为2∶1,则该过程中发生反应的化学方程式:。
| 选项 | 实例 | 分离方法 |
| A | 除去氯化钠溶液中的泥沙 | 过滤 |
| B | 用乙醚提取青蒿中的青蒿素 | 萃取 |
| C | 分离乙酸(沸点为118摄氏)与乙醚(沸点为34摄氏度) | 蒸馏 |
| D | 分离汽油和水的混合物 | 结晶 |
 B . 过滤
B . 过滤 C . 将剩余钠放回试剂瓶
C . 将剩余钠放回试剂瓶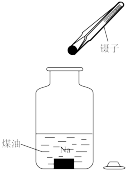 D . 转移溶液
D . 转移溶液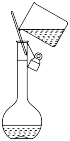
下列判断不正确的是( )
 是一种局部麻醉剂。某小组拟制备苯硫酚并探究其性质,已知相关物质的部分信息如下表所示:
是一种局部麻醉剂。某小组拟制备苯硫酚并探究其性质,已知相关物质的部分信息如下表所示: | 物质 | 化学式 | 相对分子质量 | 熔点/ | 沸点/ | 相对密度 | 溶解性 |
| 苯硫酚 | | 110 | | 169.5 | 1.07 | 难溶于水 |
| 苯磺酰氯 | | 176.5 | 14.5 | 251 | 1.38 | 难溶于水 |
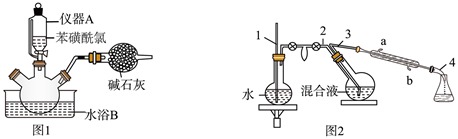
操作步骤:
①向三口烧瓶中加入 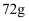 冰和
冰和 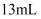 浓硫酸。
浓硫酸。
②再向三口烧瓶中慢慢加入 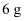 苯磺酰氯,尽快地分次加入
苯磺酰氯,尽快地分次加入 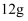 锌粉,继续反应
锌粉,继续反应 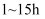 ,温度保持在
,温度保持在 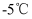 左右,如图1。
左右,如图1。
③撤去水浴B,微热三口烧瓶,并保持一定的回流。反应平稳后,再加热 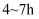 。
。
④将反应后的混合液进行水蒸气蒸馏,分出苯硫酚,如图2。
⑤加入氯化钙,经操作X得粗品 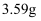 。再进行蒸馏,收集馏分,得纯品
。再进行蒸馏,收集馏分,得纯品 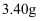 。
。
回答下列问题:
-
(1) 仪器A的名称是。
-
(2) 已知:在水中加入盐,水的沸点会升高,凝固点会降低。水浴B应选择(填标号)。
a.冰盐水浴 b.冷水浴 c.热水浴
-
(3) 在水蒸气蒸馏中(如图2),导管1的作用是,冷凝管中冷却水从(填“a”或“b”,下同)口进、口出。
-
(4) 步骤⑤中操作X是。蒸馏时,收集馏分时温度计的读数为
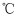 。
。
-
(5) 本实验中,苯硫酚的产率约为(保留整数)
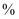 。
。
-
(6) 取少量苯硫酚产品于酸性
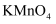 溶液中,振荡,溶液褪色,说明苯硫酚具有(填“氧化”或“还原”)性。
溶液中,振荡,溶液褪色,说明苯硫酚具有(填“氧化”或“还原”)性。

-
(1) ①“溶浸”时提高溶浸率的措施有(任写一个)。
②“溶浸”后的锡主要以SnCl4的形式存在于混合液中。写出Sn与SnCl4反应的化学方程。
③“溶浸”时,加热反应器使反应液温度升高至60℃,开始通入Cl2 , 随着反应的进行,反应所放出的热量使溶液的温度提高,此时需保持反应温度在80~90℃之间,不宜过高。温度不宜过高的原因是。“操作a”的名称是。
-
(2) ①基态Sn原子价层电子的电子排布式为,在元素周期表中属于区。
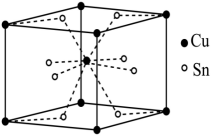
②铜锡合金晶体有多种结构,其中一种晶体的晶胞为立方晶胞(如图),则该晶体中铜、锡原子个数比为,若阿伏加德罗常数为NA , 晶胞参数为apm,则合金晶体的密度为g•cm-3(用含a、NA的式子表示,不必化简)。
- 穷则独善其身,______________。 (《孟子·尽心》)
- 运用所学《生活与哲学》有关知识回答下列问题: 材料 :高中物理、化学等课程向我们介绍了很多大胆精彩的猜想、精确控制的
- 把一只标有“12V 6W”字样的灯和一只电阻连到12V的电源上,灯能正常发光,而电路的总功率是9W,那么灯泡与电阻肯定
- 下列关于常见有机物的说法不正确的是 A.乙烯和苯都能与溴水反应 B.乙酸和油脂都能与氢氧化钠溶液反
- 在180℃,101Kpa下,1L稀轻与炔烃的混合气体与相同状态下11L氧气混合,点火充分 燃烧后,恢复到原来状况,
- 如图所示,额定电压都为110 V的两盏电灯,额定功率分别为PA=100 W,PB=40 W,把它们接在220 V的电路中
- (09年双鸭山一中期末)(6分)某同学用伏安测定一节干电池的电动势和内电阻,图是用测出的实验数据画出的干电池U―I图线,
- BUDGET FOR A BRITISH SCHOOL’S VISIT TO XX SCHOOL IN BEIJING
- 如图I所示,甲、乙之间的隔板K和活塞F都可以左右移动,甲中充入2 molA和1 mol B,乙中充入2 mol C和1
- It’sunfair! You sit there, listening to me, Istand her
- 在pH=1的无色溶液中,可以大量存在的物质是() A.NaOH、NaNO3、KNO3 B.Na2CO3、NaCl、KCl
- 2015年6月,山东省德州市制定了《2015年德州市农村土地承包经营权流转实施方案》。据此回答下列问题。 20.农地流转
- 根据下表的内容,回答问题。 某旅游景点统计表年份 2006 2007 2008 2009 2010 门年票价格 (元)
- 如图,已知在平面直角坐标系中,是坐标原点,点,在反比例函数的图象上,过点的直线交轴于点. (1)求和的值; (2)求的面
- 如图所示,ABC和DEF是在同一竖直平面内的两条光滑轨道,其中ABC的末端水平,DEF是半径为r=0.4m的半圆形轨道,
- 下列说法中正确的是 A.“神舟五号”从地面加速升空的过程中,动能增大,势能增大,机械能不变 B.“神五”在飞行过程中,
- Only Mother’s love is true love.It gives everybody everythin
- 为贯彻从紧的货币政策,中国人民银行决定:从 2007年 12月 21日起调整金融机构人民币存贷款基准利率,一年期存款基准
- 2006年4月22日是第 37个“世界地球日”,宣传的主题是“善待地球—珍惜资源、持续发展”。 下列行为不符合这一主题的
- 关于氢键,下列说法不正确的是( )A.HF的沸点比HCl的沸点高是由于HF分子间存在氢键所致B.水在结冰时体积膨胀