空气的成分及探究 知识点题库
空气中氧气含量测定的再认识.

-
(1) 【实验回顾】如图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式 .
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内 减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进人瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大.
-
(2) 【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
测量项目
实验前
实验后
烧杯中水的体积
烧杯中剩余水的体积
集气瓶(扣除内容物)和导管的容积
体积/mL
80.0
54.5
126.0
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式 .【交流表达】
(2)根据如表数据计算,改进实验后测得的空气中氧气的体积分数是 (计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
① ;
② .
根据如图所示实验分析得出的结论中,不正确的是( )
|
|
|
|
A.甲烷燃烧生成二氧化碳和水 | B.铁能在氧气中燃烧 | C.白磷的着火点比红磷的低 | D.氧气约占空气质量的 |

-
(1) 甲组同学采用课本实验装置(图2),他们先用图1的组合装置在空气中点燃红磷,然后慢慢地将燃烧匙从上到下插入广口瓶中,目的使上、下层空气中的氧气都能得到充分消耗,直到橡皮塞塞紧瓶口,红磷在瓶中继续燃烧直到熄灭,等广口瓶冷却后,打开止水夹.但这样测出的氧气的体积分数明显大于1/5.请分析原因
-
(2) 该装置本身在设计上还存在一定的缺陷,也是造成实验误差的原因,请分析其中一种缺陷,说明这种缺陷造成误差的理由.
-
(3) 乙组同学先查阅资料(如下表),然后对课本上的实验装置进行了图3所示的改进,右端玻璃管上端开口(其它仪器忽略).
颜色、状态
熔点/℃
着火点/℃
密度/(g/cm3)
红磷
暗红色固体
590
240
2.34
白磷
白色或黄白色固体
44.1
40
1.82
①乙组同学红磷换成了白磷的优点是
②大家用改进的实验装置进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了一段距离,此时他们应该怎样操作之后,才能读取左管页面的刻度.

-
(1) 图A中若红磷用量不足,测得空气中氧气的体积分数将远
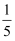 (填“大于”、“小于”或“等于”);
(填“大于”、“小于”或“等于”);
-
(2) 图B中实验运用了的研究方法,二氧化锰在反应前后化学性质和质量均不改变;
-
(3) 图C中反应后天平示数减少,你认为该反应(填“能”或“不能”) 验证质量守恒定律;
-
(4) 图D中铜片上的白磷燃烧了,热水里的白磷没有燃烧,说明燃烧条件之一是.
-
(5) 图E中实验中生成物是(填化学式).
 B . 氧气可用于医疗急救
C . 燃料燃烧一般离不开氧
D . 氧气可用于食品保鲜
B . 氧气可用于医疗急救
C . 燃料燃烧一般离不开氧
D . 氧气可用于食品保鲜


图Ⅰ 图Ⅱ
-
(1) 图Ⅰ实验中红磷燃烧的实验现象是产生大量,等A瓶冷却后打开止水夹,现象为;
-
(2) 图Ⅱ实验的操作步骤如下:
①点燃酒精灯;②撤去酒精灯,待试管冷却后松开弹簧夹;③将少量红磷平装入试管中,将20毫升的注射器活塞置于10毫升刻度处,并按图Ⅱ中所示的连接方式固定好,再将弹簧夹夹紧橡皮管;④读取注射器活塞的数据。你认为正确的实验操作顺序是(填序号);
-
(3) 图Ⅱ实验中,注射器活塞将从10毫升刻度处慢慢前移到约为毫升刻度处才停止;
-
(4) 对照图Ⅱ实验,你认为图Ⅰ实验有何不足之处?(回答一点即可)。


他用激光笔点燃红磷。
【提出问题】红磷在烧瓶内熄灭后,瓶中是否有氧气剩余?
【猜想假设】猜想:①有氧气剩余;②无氧气剩余。
【实验验证】待装置完全冷却后,将装有白磷的燃烧匙提出水面,用激光笔点燃白磷。
-
(1) 【得出结论】分析图乙得出,猜想正确(填“①”或“②”)。
-
(2) 【反思交流】根据本实验的结论,教材中用“燃烧红磷测定空气中氧气含量”的方法是否可行并说明理由 。
-
(3) 曲线DE段氧式浓度变化的主要原因是 。
-
(4) 查阅资料,验证空气中氧气体积分数,可利用铁的缓慢氧化,将空气中氧气浓度消耗至0.2%。如图丙将足量细铁丝置于试管底部,并倒扣在装有水的烧杯中,一段时间后你将看到的现象是。
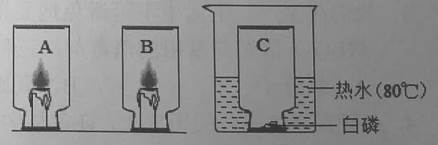
其结果:
⑴A中的蜡烛会立即熄灭。
⑵B瓶中的蜡烛突然十分明亮,一段时间后,该蜡烛也渐渐熄灭,其熄灭的原因可能是。
A.氧气耗尽 B.温度降低
C.瓶内产生了二氧化碳 D.蜡烛着火点改变
⑶C瓶倒扣住足量的白磷后,再往烧杯中倒入80摄氏度的热水,出现的现象是。


⑴取足量铁粉、活性炭混合均匀制得脱氧剂,平铺在锥形瓶内拱形有孔塑料板上,迅速塞紧瓶塞,用记号笔标记瓶塞下端位置;
⑵在量筒中加入体积为V1的红墨水,导管插入液面以下;
⑶一段时间后,待量筒液面不再下降时,此时量筒内红墨水的体积为V2;
⑷实验结束后,将锥形瓶内注水至记号笔标记处,测得整瓶水的体积为V3 , 计算空气中氧气的体积分数。
回答下列问题:
-
(1) 检查图甲气密性的基本操作;
-
(2) 该实验测得空气中的氧气含量为(用含V1、V2、V3符号表示);
-
(3) 与课本中红磷燃烧进行此实验相比,本实验的主要优点是;
-
(4) 小金通过该实验测得数据,比实际空气中氧气含量偏大,请推测可能的原因是。
 B . 实验室加热高锰酸钾制取氧气
B . 实验室加热高锰酸钾制取氧气  C . 将水通电分解一段时间
C . 将水通电分解一段时间  D . 用等质量、等浓度的双氧水分别制取氧气
D . 用等质量、等浓度的双氧水分别制取氧气 

-
(1) 水自动进入集气瓶的原因是。
-
(2) 如果进入集气瓶内水的体积明显小于瓶内空气体积的,其原因可能是__________。A . 使用的红磷量不足 B . 没塞紧瓶塞 C . 没夹紧止水夹,红磷燃烧时瓶内空气受热从导管逸出 D . 插入燃烧匙速度太慢,塞紧瓶塞前,瓶内部分空气受热逸出
-
(3) 若空气中氮气也能和红磷反应,能否用该方法来测定空气中氧气的含量?。

如图乙,保持活塞处于打开状态,则:

-
(1) 如图乙时,若广口瓶的底部A点和烧杯底部B点所受压强分别为PA和PB , 则PAPB (选填“>”、“=”或“<”)
-
(2) 要准确测出空气中氧气体积分数,应往图乙的烧杯中注水至与集气瓶内液面相平,若测得此时集气瓶内的气体体积为V2。则氧气体积占空气总体积的比例可用V1、V2表示为。

-
(1) 步骤①中,检查装置气密性的具体方法是。
-
(2) 该兴趣小组测得的空气中氧气体积分数可用题目中的字母表示为(拱型支架和导管体积忽略不计)。
-
(3) 图乙为教材上“测量空气中氧气含量”的实验,该实验需要用到止水夹,而图甲实验一般不需要止水夹,其原因是。
- When you make a mistake, big orsmall, cherish it like it’s t
- 下列实验操作或装置(略去部分夹持仪器)正确的是 A.配制溶液 B.中和滴定 C.制备乙酸乙酯
- 2011年1月18-21日,我国对美国进行国事访问。中美两国就建设相互尊重、互利共赢的中美合作伙伴关系达成共识。中美合作
- 石油是一种重要能源,人类正面临着石油短缺、油价上涨的困惑。以下解决能源问题的方法不当的是 A.用木材作燃料
- 下列说法不正确的是()A.只要空间的三个基向量的模为1,就是空间的一个单位正交基底B.竖坐标为0的向量,在x轴与y轴所确
- 神舟五号载人飞船的返回舱距地面10km时开始启动降落伞装置,速度减至10m/s,并以这个速度在大气中降落。在距地面某一高
- 你认为图中全球平均气温的变化与二氧化碳浓度的变化大体上呈现出了怎样的关系A.正比例 B.反比例
- 2014年10月24日,国务院副总理马凯在四川调研时强调,要加大就业援助力度,把零就业家庭等困难群体作为帮扶重点。要规范
- 如图,已知A(3,0),B(0,﹣1),连接AB,过B点作AB的垂线段BC,使BA=BC,连接AC. (1)如图1,求C
- 2.“今世用人,大率以文词进。大臣,文士也;近侍之臣,文士也;钱谷之司,文士也;边防大帅,文士也;天下转运使,文士也;知
- 已知AB、CD为异面线段,E、F分别为AC、BD中点,过E、F作平面α∥AB.求证:CD∥α.
- 小农经济的狭隘性主要表现在 A.男耕女织,自给自足 B.抗击自然灾害的能力弱 C.对封建国家的依赖性强D.导致土地兼并,
- It’s only too natural that personal characteristics play a v
- 如图是人体部分生理活动示意图,字母a~f代表某些物质。请据图回答下列问题:(1)淀粉在小肠内被消化成物质a 后进入血
- 二、古代诗文阅读(37分) (一)文言文阅读(19分) 阅读下面文言文,完成4~7题。 王勃字子安,绛州龙门人。六岁善文
- 老师为同学们提供了如下实验装置:(1)写出图中带有标号的仪器名称:a;B装置中长颈漏斗须伸入液面下的原因是 . (2)实
- 对生物遗传和变异的表述正确的是 A.生物的遗传现象是普遍存在的,而变异现象则不是普遍存在的 B.子女一定和父母的性状相同
- 国家发改委发出通知,决定自2009年11月10日零时起将汽、柴油价格每吨均提高480元。据此回答1~2题。 1.成品油价
- 我们往往用杜甫《望岳》中的“____________________,____________________”来表达勇
- 关于下图DNA分子片段的说法正确的是()A.限制性核酸内切酶可作用于①②处 B.“G”是鸟嘌呤脱氧核糖核苷酸 C.该DN