化学实验基本操作 知识点题库
(1)粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42﹣等杂质,必须精制后才能供电解使用.精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2 , 这3种试剂添加的合理顺序是 (填序号
(2)工业生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.选择适宜的催化剂,是否可以提高SO2的转化率? (填“是”或“否”),是否可以增大该反应所放出的热量? (填“是”或“否”);
(3)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得: SiO2(s) + C(s) + N2(g) ![]() Si3N4(s)+ CO(g)
Si3N4(s)+ CO(g)
①配平上述反应的化学方程式
②该反应的平衡常数表达式为K=
(4)水是一种重要的自然资源,天然水在净化处理过程中加入的混凝剂可以是 (填两种物质名称),其净水作用的原理是
 B .
B . 
C .
C . 
D .
D . 
①用稀硝酸清洗做过银镜反应后的试管
②用酒精清洗做过碘升华的烧杯
③用浓盐酸清洗做过高锰酸钾分解实验的试管
④用盐酸清洗长期存放三氯化铁溶液的试剂瓶
⑤用氢氯化钠溶液清洗盛过苯酚的试管
⑥用氢氧化钠溶液清洗沾有硫磺的试管
下列对以上操作的判断.正确的是( )
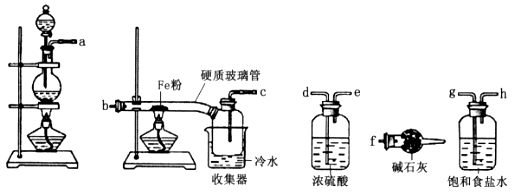
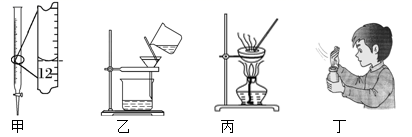
a.量筒 b.容量瓶 c.托盘天平 d.温度计 e.分液漏斗
-
(1) 标出仪器使用温度的是 (填写编号).
-
(2) 使用前需要检查是否漏水的是 (填写编号).
-
(3) 称取10.5g固体样品(1g以下使用游码)若样品与砝码错放位置,则实际称取的样品质量为 g.
-
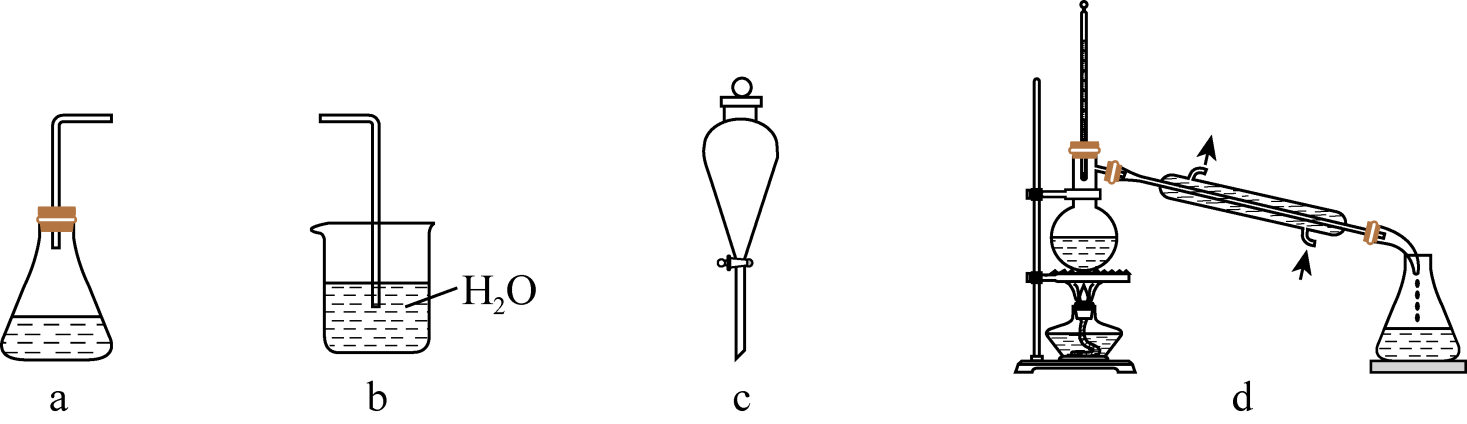
(4) 蒸馏时加入碎瓷片的作用是;分液时应先,再放液.
①量筒 ②锥形瓶 ③烧杯 ④试管 ⑤烧瓶 ⑥蒸发皿 ⑦坩埚
-
(1) 装置的连接顺序为a→→→→→b→c→f。
-
(2) 硬质玻璃管与收集器之间没有用导管连接,这样做的优点是。
-
(3) 反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
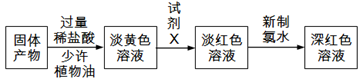
试剂X中溶质的化学式为;固体产物的成分可能为(填字母)。
A.Fe和FeCl3
B.FeCl2 和FeCl3
C.Fe、FeCl2和FeCl3
D.Fe和FeCl2
-
(4) 加入少许植物油的作用是,加入新制氯水后溶液红色加深的原因:(用离子方程式表示)。
-
(5) 现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为。(计算结果保留两位有效数字)
-
(1) 以下操作顺序不合理的是_____________。A . ②⑤④③① B . ④⑤②①③ C . ⑤②④①③ D . ⑤④②①③
-
(2) 通过步骤①中过滤后的滤液,检验SO42-是否除尽的操作方法是。
-
(3) 实验室将上述得到的精制食盐水制成精盐的过程中,还需要进行某一操作,该操作中需要加热的仪器为:。
-
(4) 实验室需要450 mL 4.00 mol·L-1NaCl溶液,现利用提纯的NaCl进行配制,所用仪器除天平、药匙、烧杯、玻璃棒外还有(填仪器名称)。定容时,俯视刻度线,对所配溶液浓度的影响:(填:偏大、偏小、或无影响)。
试剂相关性质如下表:
| 苯甲酸 | 乙醇 | 苯甲酸乙酯 | |
| 常温性状 | 白色针状晶体 | 无色液体 | 无色透明液体 |
| 沸点/℃ | 249.0 | 78.0 | 212.6 |
| 相对分子量 | 122 | 46 | 150 |
| 溶解性 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 | 与水任意比互溶 | 难溶于冷水,微溶于热水,易溶于乙醇和乙醚 |
回答下列问题:
-
(1) 为提高原料苯甲酸的纯度,可采用的纯化方法为。
-
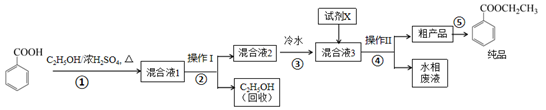
(2) 步骤①的装置如图所示(加热和夹持装置已略去),将一小团棉花放入仪器B中靠近活塞孔处,将吸水剂(无水硫酸铜的乙醇饱和溶液)放入仪器B中,在仪器C中加入 12.2 g纯化后的苯甲酸晶体,30 mL无水乙醇(约0.5 mol)和3 mL浓硫酸,加入沸石,加热至微沸,回流反应1.5~2 h。仪器A的作用是;仪器C中反应液应采用方式加热。
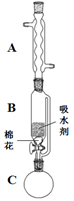
-
(3) 随着反应进行,反应体系中水分不断被有效分离,仪器B中吸水剂的现象为。
-
(4) 反应结束后,对C中混合液进行分离提纯,操作I是;操作II所用的玻璃仪器除了烧杯外还有。
-
(5) 反应结束后,步骤③中将反应液倒入冷水的目的除了溶解乙醇外,还有;加入试剂X为(填写化学式)。
-
(6) 最终得到产物纯品12.0 g,实验产率为 %(保留三位有效数字)。
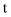 作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中的Ca2+、Mg2+测定中涉及的反应有:①M2+(金属离子)+Y4-(EDTA)=MY2-;
作为指示剂,用EDTA(乙二胺四乙酸)标准溶液直接滴定水中的Ca2+、Mg2+测定中涉及的反应有:①M2+(金属离子)+Y4-(EDTA)=MY2-; ②M2++EBT(铬黑T,蓝色)=MEBT(酒红色);
③MEBT+Y4-(EDTA)=MY2-+EBT。下列说法正确的是( )
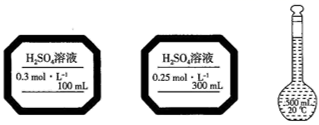
下列说法正确的是( )
 )易潮解,加热条件下易被空气中的
)易潮解,加热条件下易被空气中的 氧化。某小组选择下列装置(装置可重复使用)制备
氧化。某小组选择下列装置(装置可重复使用)制备 。回答下列问题:
。回答下列问题:
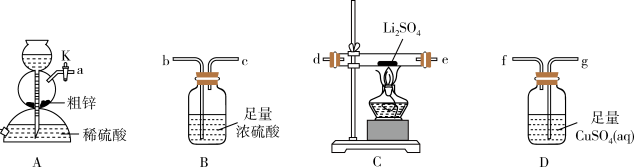
已知:①粗锌中含少量Cu和FeS;
②装置C中发生的反应为 。
。
-
(1) 装置A的名称是,停止装置A中反应的操作是(填“打开”或“关闭”)K。
-
(2) 气流从左至右,导管口连接顺序是a→→→→→d→e→→。
-
(3) 其他条件相同,粗锌与稀硫酸反应比纯锌(填“快”或“慢”),实验中观察到装置D中产生黑色沉淀,其离子方程式为。
-
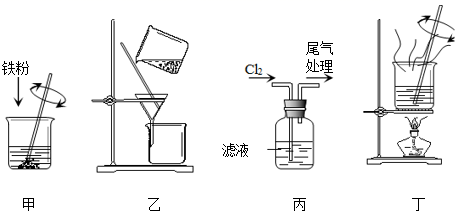
(4) 实验完毕后,选择图1、图2装置对装置A中混合物进行分离。先选择图1装置过滤,再将滤液进行蒸发浓缩、降温结晶,再选择图2装置过滤,得到粗皓矾(
 )。
)。
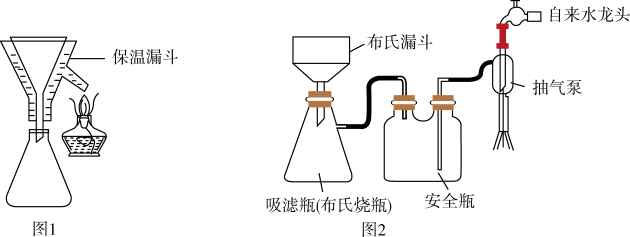
下列有关说法正确的是____(填标号)。
A . 选择图1装置过滤的优点是避免析出 B . 选择图1装置过滤,主要是分离
B . 选择图1装置过滤,主要是分离 和
和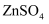 溶液
C . 粗皓矾中可能含胆矾
D . 选择图2装置过滤的优点是过滤速率快
溶液
C . 粗皓矾中可能含胆矾
D . 选择图2装置过滤的优点是过滤速率快
-
(5) 探究
 产品成分:
产品成分:
实验
操作与现象
结论
Ⅰ
取少量
 样品溶于水,滴加足量的稀盐酸,将气体通入品红溶液中,溶液褪色
样品溶于水,滴加足量的稀盐酸,将气体通入品红溶液中,溶液褪色样品中含
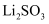
Ⅱ
向实验Ⅰ的溶液中滴加
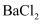 溶液,产生白色沉淀
溶液,产生白色沉淀样品中含
①由实验Ⅱ知,
 样品中还含有(填化学式),产生该杂质的可能原因是(填标号)。
样品中还含有(填化学式),产生该杂质的可能原因是(填标号)。A.通入的氢气过量 B.
 未反应完 C.温度过高
未反应完 C.温度过高②测定产品纯度:向wg样品(设杂质只有
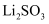 )中加入过量的
)中加入过量的 稀硫酸,充分反应后(设没有S单质生成),煮沸溶液以除去残留的酸性气体;滴加的酚酞溶液作指示剂,用标准
稀硫酸,充分反应后(设没有S单质生成),煮沸溶液以除去残留的酸性气体;滴加的酚酞溶液作指示剂,用标准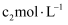 的NaOH溶液滴定过量的硫酸,消耗NaOH溶液
的NaOH溶液滴定过量的硫酸,消耗NaOH溶液 。
。 样品的纯度为(列出计算式)。
样品的纯度为(列出计算式)。
- 能使合成氨反应进行程度增大的方法是 A.升高温度 B.降低压强
- 如图所示,三个完全相同的金属小球a、b、c位于等边三角形的三个顶点上.a和c带正电,b带负电,a所带电荷量的大小比b所带
- 从基因文库中获取目的基因的根据是A.基因的核苷酸序列 B.基因的功能 C.基因的转录产
- 化简4的结果为____________.(其中)
- 物态变化现象在一年四季中随处可见.关于这些现象以及发生这些现象过程中的吸、放热情况,下列说法正确的是 A.春天的早晨经常
- 下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是() A.SO2和SiO2
- 阅读下面这首古诗,完成21-22题。(4分) 泊秦淮
- 阅读下面的文字,完成1—3题。 “鲁迅”的“现代价值”(节选) 钱理群 ①我们讲鲁迅,就是讲他的思想,他的文学,他的实践
- 已知x、y都是实数,且,则=
- 在密闭容器中进行如下可逆反应:X2(g)+Y2(g)⇌2XY(g),已知X2、Y2、XY三者起始浓度分别为0.1mol/
- 如果圆锥的底面周长是20,侧面展开后所得的扇形的圆心角为120°,则其侧面积为 (结果用含的式子表示
- 韩非子“以法为本”中的“法”与孟德斯鸠《论法的精神》中的“法”对君权的作用 A.完全一致 B.大同小异
- 如右图,矩形ABCD的对角线BD经过坐标原点,矩形的边分别平行于坐标轴,点C在反比例函数的图象上,若点A的坐标为(-2,
- 检验集气瓶中氯气是否充满的正确方法是() A.干燥的碘化钾淀粉试纸放在瓶口 B.湿润的酚酞试纸放于瓶口 C.把蘸有氢氧化
- 含碳原子个数为10或小于10的烷烃中,其一卤代烷烃不存在同分异构体的烷烃共有 () A. 2种 B. 3种 C. 4种
- (2011·宁波模拟)下表为某小组同学用大豆种子探究种子萌发的外界条件实验,他们探究的外界条件是( )A.温度
- 下列物质中,不密封保存会变质的是A. 浓硫酸 B. 氢氧化钠 C. 浓盐酸 D. 大理石
- 若二次根式 与是同类二次根式,则ab = _______ 。
- 在动物细胞工程和胚胎工程中所用的物质和其发挥的作用正确的组合是 A.肝素——诱导精子与卵细胞受精 B.胃蛋白酶——动物细
- It may not rain, but you had better take an umbrella________



