化学实验基本操作 知识点题库
①浓盐酸与二氧化锰制取氯气;②苯与浓硝酸、浓硫酸的混合酸反应制硝基苯;③电石与水反应制乙炔;④乙醇与浓硫酸制取乙烯;⑤乙醛溶液与银氨溶液的银镜反应;⑥甲醛溶液与新制氢氧化铜悬浊液反应.
-
(1) Ⅰ、用酒精灯直接加热的有 (填序号,下同).
-
(2) Ⅱ、用酒精灯通过石棉网加热的有
-
(3) Ⅲ、通过水浴加热的有 ,其好处是
-
(1) 下列实验操作的描述中,正确的是 (填序号)
①为使稀硫酸和锌制取氢气的反应速率加快,可向稀硫酸中加入用铜丝网包裹的锌粒
②粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌漏斗中的液体
③配制一定物质的量浓度的溶液时,容量瓶洗涤后不用进行干燥
④蒸馏操作中,温度计水银球部位要插入液面下且不接触蒸馏烧瓶壁
⑤可以在试管中加热氯化铵固体制备少量氨气
⑥盛放石灰水的试剂瓶内壁常有一层白色固体物质,可用稀硫酸清洗除去
-
(2) 下列说法中,符合安全要求的是 (填序号)
①在通风橱内做铜与浓硝酸反应的实验
②给固体加热时,试管口应略向上倾斜
③用胶头滴管滴加液体时可将其伸入试管口一下,以防止滴到外面
④给试管内的液体加热时,试管口不能对着别人,而应朝向自己以便于观察.
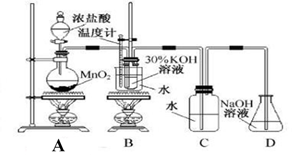
-
(1) 下列说法正确的是_____。A . 为使浓盐酸全部反应完,需加入过量的MnO2固体 B . 为研究饱和氯水的酸性,用干燥的pH试纸来测定饱和氯水的pH值 C . 测定氯水中的氯元素含量,设计实验方案为:加热15.0mL饱和氯水试样,用排饱和食盐水来测定产生气体的体积 D . 若对调B和C装置的位置,可以提高B中氯酸钾的纯度
-
(2) 锥形瓶D中的NaOH溶液改用过量的亚硫酸钠溶液代替,设计实验方案验证尾气吸收后溶液中含有SO42-。。
 B . 高锰酸钾
B . 高锰酸钾  C . 氢氧化钠
C . 氢氧化钠  D . 氧气
D . 氧气 
| | | | |
| A滴加液体 | B过滤 | C稀释浓硫酸 | D称量固体 |
-
(1) 酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是 (填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作符合题意。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
-
(2) 氧化还原滴定——取一定量的草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,表格中记录了实验数据:
滴定次数
待测液体积
(mL)
标准KMnO4溶液体积(mL)
滴定前读数
滴定后读数
第一次
25.00
0.50
20.40
第二次
25.00
3.00
23.00
第三次
25.00
4.00
24.10
①滴定时发生的离子反应方程式,KMnO4溶液应装在 (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是。
②该草酸溶液的物质的量浓度为。
-
(3) 沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是______(填选项字母)。
难溶物
AgCl
AgBr
AgCN
Ag2CrO4
AgSCN
颜色
白
浅黄
白
砖红
白
Ksp
1.77×10-10
5.35×10-13
1.21×10-16
1.12×10-12
1.0×10-12
A . NaCl B . NaBr C . NaCN D . Na2CrO4
①烧杯②量筒③1000mL容量瓶④玻璃棒⑤托盘天平(带砝码)。
请回答下列问题:
-
(1) 用托盘天平称量时,需要称取NaOH固体g。
-
(2) 配制过程中,用到的仪器有(填序号),还缺少的玻璃仪器有(填仪器名称)。
-
(3) 配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)____。A . 继续往容量瓶内小心加水,直到液面接近刻度1cm~2cm处 B . 在盛有NaOH固体的烧杯中加入适量水溶解 C . 将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中 D . 将容量瓶盖紧,反复上下颠倒,摇匀 E . 改用胶头滴管加水,使溶液凹液面恰好与刻度线相切 F . 用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
-
(4) 实验中两次用到玻璃棒,其作用分别是:、。
-
(5) 若出现如下情况,能引起所配溶液浓度偏高的是(填序号)。
①用已经生锈的砝码称量NaOH固体
②实验前容量瓶内有少量蒸馏水
③配制过程中,没有用蒸馏水洗涤
④定容时俯视刻度线
⑤移液前没有冷却至室温
⑥在烧杯中溶解时,溅出少量溶液
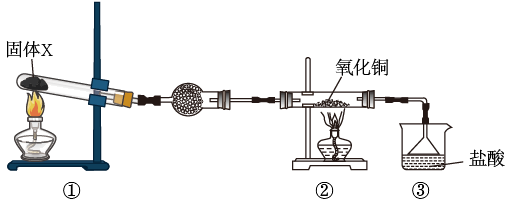
下列说法不正确的是( )
 N2+3Cu+3H2O
D . 先启动装置①中的反应,当装置③漏斗中产生较多白烟时,再点燃装置②中酒精灯
N2+3Cu+3H2O
D . 先启动装置①中的反应,当装置③漏斗中产生较多白烟时,再点燃装置②中酒精灯
-
(1) I.海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
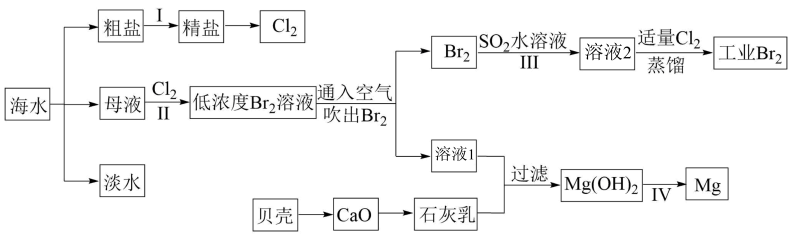
请回答下列问题:
请列举除蒸馏法外海水淡化的一种方法:。
-
(2) 步骤I中,粗盐中含有Ca2+、Mg2+、
 等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
A . ①②③④ B . ②③④① C . ②④③① D . ③④②①
等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
A . ①②③④ B . ②③④① C . ②④③① D . ③④②① -
(3) 步骤II已经获得Br2 , 步骤III又将Br2还原为Br- , 其目的是。
-
(4) 写出步骤III反应的离子方程式:。
-
(5) II.海洋植物如海带、海藻中含有丰富的碘元素。碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

灼烧所用仪器有酒精灯、泥三角、(填仪器名称)。
-
(6) 向酸化的滤液中加入过氧化氢溶液,可将I-氧化为I2;请写出该反应的离子方程式:。
- 把0.05 mo1Na0H 固体分别加入下列 100ml 液体中,溶液导电能力变化不大的是
- (10分)如图所示,边长为0.5m的正方形线框ABCD绕AB边在匀强磁场中匀速转动,AB边和磁场垂直,转速为50转/秒,
- 梁启超在《变法通议》中写道,同治初年,德相俾斯麦对人说,“三十年后,日本其兴,中国其弱乎?日本人之游欧洲者,讨论学业,讲
- 读图11—澳大利亚气候分布图,完成26~27题。 26.澳大利亚的气候分布特点是( ) A.以赤道为中心南北对称
- 2011年9月12日,中国宁波籍科学家屠呦呦因发现青蒿素(化学式为C15H22O5,一种用于治疗疟疾的药物)而获得度拉
- .化学课外活动小组设计了如图所示的一套气体发生、收集和尾气吸收装置,以探究该装置的多功能性能。(1)甲同学认为装置Ⅰ可作
- A man dances with a robot partner at Japan’s National Sci
- 直接民主是古代雅典民主政治的主要特色之一,与此特色形成直接有关的是 A. 雅典人思想活跃
- 文言文阅读。(甲)山不在高,有仙则名。水不在深,有龙则灵。斯是陋室,惟吾德馨。苔痕上阶绿,草色入帘青。谈笑有鸿儒.往来无
- 如图,光在两种物质分界面上发生了反射和折射,若入射光线与界面的夹角是60°,反射光线与折射光线垂直,那么反射角是
- 今年3月召开的全国人大三次会议审议通过了《选举法修正案》,选举法的修正,实现“同票同权”有利于更好地保证城乡人民享有平等
- (16)平行四边形的一个顶点A在平面内,其余顶点在的同侧,已知其中有两个顶点到的距离分别为1和2 ,那么剩下的一个顶点到
- 下图是三种粒子的结构示意图,请回答下列问题: (1)①所属的元素属于______________元素(填“金属”或“非
- 下列关于遗传变异的说法正确的是( ) A.DNA分子中发生碱基对的替换、增添和缺失不一定引起基因突变 B.基因型
- 已知:如图,在平面直角坐标系中,直线AB分别与轴交于点B、A,与反比例函数的图象分别交于点C、D,轴于点E,.(1).
- 某元素的同位素,它的氯化物XCl2 1.11 g溶于水制成溶液后,加入1 mol·L-1的AgNO3溶液20 mL恰好完
- We _______ dinner at six o’clock when JSTV _______ to show t
- (三)阅读《邹忌讽齐王纳谏》(节选)和《成侯邹忌为齐相》(14分)甲 文邹忌入朝见威王,曰:“……由此观之,王之蔽甚矣
- 用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是 ( )A.加热
- 根据右图回答问题:⑴图中所示的内容在生命系统的结构层次中属于 。 ⑵一只蝉