化学实验基本操作 知识点题库
①用标准溶液润洗滴定管
②往滴定管内注入标准溶液
③检查滴定管是否漏水
④滴定
⑤洗涤.
(填字母编号).

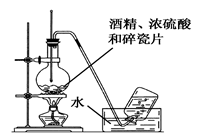 B . 实验室制氨气
B . 实验室制氨气  C . 实验室制氯气
C . 实验室制氯气 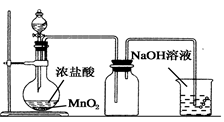 D . 实验室制乙酸乙酯
D . 实验室制乙酸乙酯 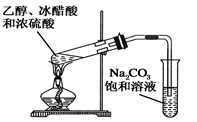
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将过量的CO2通入CaCl2溶液中 | 无白色沉淀出现 | 生成的Ca(HCO3)2可溶于水 |
| B | 常温下将铁片插入浓硫酸中 | 无明显现象 | 铁片和浓硫酸不反应 |
| C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| D | 向澄清石灰水加入某试剂的溶液少许 | 产生白色沉淀 | 该试剂中一定含有CO32— |
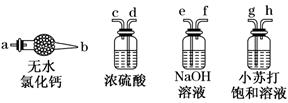
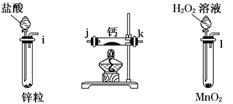
请回答下列问题:
-
(1) 请选择必要的装置,按气流方向连接顺序为(填仪器接口的字母编号)。
-
(2) 根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞;___________(请按正确的顺序填入下列步骤的标号)。A . 收集气体并检验其纯度 B . 加热反应一段时间 C . 关闭分液漏斗活塞 D . 停止加热,充分冷却
-
(3) 实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此判断,上述实验确有 CaH2生成。写出CaH2 的电子式。写出CaH2 与水反应的化学方程式。
 B . 溶解
B . 溶解 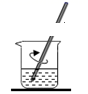 C . 过滤
C . 过滤 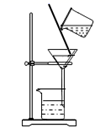 D . 转移溶液
D . 转移溶液 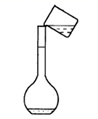
-
(1) Ⅰ.某科学探究小组设计以下装置依次完成氯气的制备、氯酸钠的制备、次氯酸钠的制备并探究氯水的性质。
其中:①为氯气发生装置,烧瓶中盛放 MnO2 固体;
②的试管里盛有 15 mL 30% NaOH 溶液,并置于热水浴中;
③的试管里盛有 15 mL 8% NaOH 溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置。
请填写下列空白:
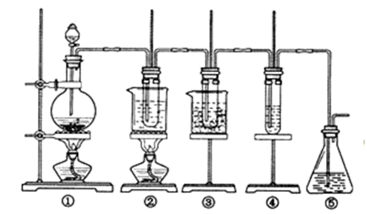
如何检验装置①的气密性。
-
(2) 如果实验室没有 MnO2 , 下列物质可以用来代替 MnO2制 Cl2的是__A . KMnO4 B . Fe2O3 C . 浓硫酸 D . KClO3
-
(3) 制备氯酸钠的化学方程式为 。
-
(4) 比较制取氯酸钠和次氯酸钠的条件,二者的差异是:。
-
(5) ④的试管里紫色石蕊试液现象及原因 。
-
(6) Ⅱ.次氯酸钠溶液可以杀灭新冠病毒,若将其与稀硫酸混合使用可增强消毒能力。现用18mol·L-1 浓硫酸来配制 450 mL 0.2 mol·L-1 的稀硫酸。
①需用量筒量取浓硫酸的体积为mL。
②定容时的操作:当液面离容量瓶颈部的刻度线 1~2cm 时, ,盖好瓶塞,反复上下颠倒,摇匀。
③若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正确的是。
A.配制前,容量瓶用蒸馏水洗涤后再用硫酸润洗
B.量取浓硫酸时,读数时俯视液体的凹液面
C.浓硫酸稀释后立即转移至容量瓶定容
D.颠倒摇匀后,液面低于刻度线,继续滴加蒸馏水
 俗名草酸,易溶于水,其水溶液与酸性
俗名草酸,易溶于水,其水溶液与酸性 溶液反应的离子方程式为:2MnO4-+ 6H+ + 5H2C2O4= 2Mn2++10CO2↑+8H2O,化学学习小组进行如下实验。
溶液反应的离子方程式为:2MnO4-+ 6H+ + 5H2C2O4= 2Mn2++10CO2↑+8H2O,化学学习小组进行如下实验。
-
(1) Ⅰ.探究反应速率的影响因素
设计了如下的方案并记录实验结果(忽略溶液混合体积变化).限选试剂和仪器:
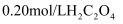 溶液、
溶液、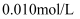 酸性
酸性 溶液、蒸馏水、试管、量筒、秒表、恒温水浴槽
溶液、蒸馏水、试管、量筒、秒表、恒温水浴槽物理量

V(蒸馏水)
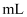

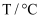
乙
①
3.0
0
5.0
50
②
3.0
0
5.0
25
③
1.0
a
5.0
25
上述实验是探究温度对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则a为;乙是实验需要测量的物理量,则表格中“乙”应填写。
-
(2) Ⅱ.测定
 中x值
中x值为了测定草酸晶体
 中的x值,某实验小组进行实验,步骤如下:
中的x值,某实验小组进行实验,步骤如下:①称取
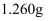 草酸晶体,配成
草酸晶体,配成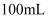 溶液。
溶液。②取
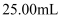 该
该 溶液加入锥形瓶内,再加入适量稀硫酸。
溶液加入锥形瓶内,再加入适量稀硫酸。③用浓度为
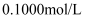 的
的 标准溶液进行滴定,至滴定达到终点。
标准溶液进行滴定,至滴定达到终点。④重复实验。记录整理数据如下:
实验序号
V(
 溶液)
溶液)滴定前刻度
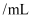
滴定后刻度
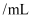
1
0.10
10.00
2
1.10
11.10
3
1.50
13.50
4
0.70
10.80
回答下列问题:
步骤③滴定过程中,盛装
 溶液的仪器为(填名称)。
溶液的仪器为(填名称)。 -
(3) 本实验滴定达到终点的标志是。
-
(4) 根据数据,计算
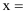 。
。
-
(5) 下列滴定操作会使测得的x值偏大的是____。A . 滴定开始时仰视滴定管刻度,滴定终点时俯视滴定管刻度 B . 滴定时所用的
 溶液因久置而导致浓度变小
C . 滴定管尖嘴内在滴定前有气泡,滴定后气泡消失
D . 滴定前,用
溶液因久置而导致浓度变小
C . 滴定管尖嘴内在滴定前有气泡,滴定后气泡消失
D . 滴定前,用 溶液润洗锥形瓶
溶液润洗锥形瓶
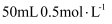 盐酸与
盐酸与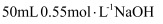 溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸和碱的密度、比热容与水的相同)。回答下列问题:
溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸和碱的密度、比热容与水的相同)。回答下列问题: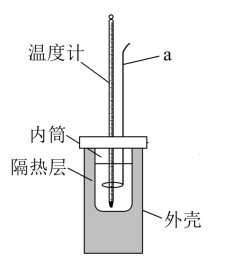
-
(1) 仪器a的名称为,其作用是。
-
(2) 实验中改用
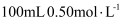 盐酸和
盐酸和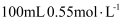
 溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”,下同);生成
溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”,下同);生成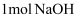 时放出的热量,理由是。
时放出的热量,理由是。
-
(3) 若用等物质的量的
 固体进行上述实验,测得的中和反应的反应热的绝对值
固体进行上述实验,测得的中和反应的反应热的绝对值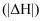 将(填“偏大”、“偏小”或“无影响”)。
将(填“偏大”、“偏小”或“无影响”)。
-
(4) 若四次操作测得终止温度与起始温度差
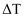 分别为①
分别为①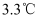 、②
、②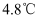 、③
、③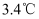 、④
、④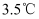 , 则所得的中和反应的反应热
, 则所得的中和反应的反应热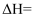
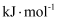 (已知该温度下水的比热容:
(已知该温度下水的比热容: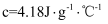 , 忽略量热计的比热容,保留三位有效数字)。
, 忽略量热计的比热容,保留三位有效数字)。
-
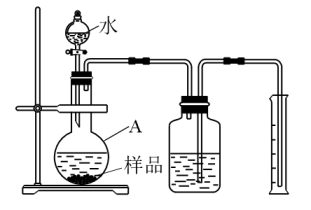
(1) 实验前,需进行的操作是。
-
(2) 仪器A的名称为。
-
(3) 仪器A中发生的反应的化学方程式有、。其中属于氧化还原反应的反应中的氧化剂为(填标号,下同);还原剂为。
a. Na2O b. Na2O2 c.H2O
-
(4) 取1g该样品进行实验,当固体反应完全,得到0.16g (经折算)气体,则该样品的纯度为。
- 当军人在行军礼时,相关肌肉的运动情况是( ) A.肱二头肌舒张,肱三头肌舒张 B.肱二头肌舒张,肱三头肌收缩 C
- 下列各项中,由遗传因素决定的行为是 A.刚出生的婴儿就会吃奶,会抓握物体 B.英格兰的大山雀学会偷喝牛奶 C.蚯蚓学
- 下列句子中标点符号使用有误的一项是() A.(司马)懿曰:“亮平生谨慎,不曾弄险。今大开城门,必有埋伏。我兵若进,中其计
- 使用机械效率低的机械.一定:( ) A费功 B费力 c费距离 D费时闻
- 课本P152有段文字:把函数y=2x的图像分别沿y轴向上或向下平移3个单位长度,就得到函数y=2x+3或y=2x-3的图
- 有一个晚上小明同学在未开灯的房间里看电视时,拿着一个凸透镜在电视机与对面的墙壁移动,忽然他看到墙壁上出现了电视机屏幕的放
- 用NA表示阿伏加德罗常数的值。下列叙述不正确的是( ) A.常温下,1 L 0.1 mol·L-1 的NH4NO3溶液中
- 下列实验操作正确且能达到预期目的的是实验目的 操 作 ① 比较水和乙醇中羟基氢的活泼性强弱 用金属钠分别与水和乙醇反
- 如图为人体细胞的分裂、分化、衰老和死亡过程的示意图,图中①﹣⑥为各个时期的细胞,a﹣c表示细胞所进行的生理过程.据图分析
- 下列常用词语中书写完全正确的一项是 A.尚待商确 声名鹊起 人情世故 B.堕落腐化 明辩是
- Howmuch did you_________that nice MP4? A.pay B
- 阅读理解。阅读下列材料,从A、B、C、D四个选项中选出最佳答案. Haveyou ever returne
- 生物对环境的适应是 存在的,生物只有 才能生存下来。如果 ,就会被环境淘汰。
- 1948年底,著名建筑大师梁思成先生曾写信给中共中央,提出要尽可能地保护故宫、颐和园等,这与当时正在进行的哪一战役有关系
- 如图,▱ABCD中,E为AD上一点,F为BC上一点,EF与对角线BD交于点O,以下三个条件:①BO=DO; ②EO=FO
- 如图所示,虚线a、b、c代表电场中的三个等势面,相邻等势面之间的电势差相等,即Uab= Ubc,实线为一带正电的质点仅在
- 24.德意志第二帝国的联邦议会不同于西方的上院,在这里它是真正的实权机构,相当于各邦使节构成的帝国最高合议机关。在正常情
- 民国二年,某地农村百姓家的春联是:“帝德乾坤大,皇恩雨露深。”该春联反映的历史本质是( ) A.辛亥革命
- 当今世界,影响最大的国际组织是A . 联合国 B . 欧盟 C . 北约 D . 世界贸易组织
- 阅读《父子的母校》,完成21-24题。(20分) 父亲对儿子说起他的母校,腮边的胡楂儿都飞快地跳起了舞。 父亲说,那操



