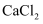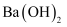离子晶体 知识点题库
下列说法正确的是( )
A . 分子晶体中一定存在分子间作用力,不一定存在共价键
B . 分子中含两个氢原子的酸一定是二元酸
C . 含有金属阳离子的晶体一定是离子晶体
D . 元素的非金属性越强,其单质的活动性一定越强
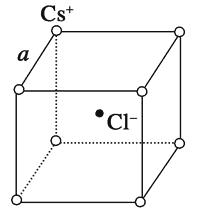
下图是氯化铯晶体的晶胞(晶体中的最小重复单元),已知晶体中两个最近的Cs+离子核间距离为acm,氯化铯的相对分子质量为M , NA为阿伏加德罗常数,则氯化铯晶体密度是( )
A .  g/cm3
B .
g/cm3
B .  g/cm3
C .
g/cm3
C . 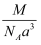 g/cm3
D .
g/cm3
D .  g/cm3
g/cm3
 g/cm3
B .
g/cm3
B .  g/cm3
C .
g/cm3
C . 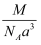 g/cm3
D .
g/cm3
D .  g/cm3
g/cm3
用序号填空:
(1)有下列四种物质:①MgCl2晶体 ②干冰 ③NaOH晶体 ④金刚石.
其中只含有离子键的离子晶体是 ;化学式既能表示物质的组成,又能表示物质的一个分子的是 .
(2)在相同条件下,SO2在水中的溶解度和CO2在水中的溶解度相比,SO2的溶解度大,请从分子性质的角度阐述理由 .
(3)有下列四种无机含氧酸:①H2CrO4 ②HMnO4 ③H3AsO4
根据无机含氧酸的酸性规律,将三种无机含氧酸按酸性由强到弱的顺序是
关于晶体的下列说法正确的是( )
A . 在晶体中只要有阴离子,就一定有阳离子
B . 在晶体中只要有阳离子,就一定有阴离子
C . 原子晶体的熔点一定比金属晶体的高
D . 分子晶体的熔点一定比金属晶体的高
在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有(填化学式,下同),由非极性键形成的非极性分子有,能形成分子晶体的物质是,晶体中含有氢键的是,属于离子晶体的是,属于原子晶体的是,五种物质的熔点由高到低的顺序是.
1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖,其晶胞结构如图。
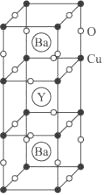
-
(1) 根据图示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,确定其化学式。
-
(2) 根据(1)所推出的化合物的组成,计算其中Cu原子的平均化合价(该化合物中各元素的化合价为
 、
、  、
、  和
和 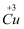 ),试计算化合物中这两种价态Cu原子个数比。
),试计算化合物中这两种价态Cu原子个数比。
下列物质中属于含有非极性键的离子晶体是 ( )
①醋酸钠 ②氢氧化钾 ③过氧化钠 ④金刚石
⑤乙醇 ⑥碳化钙
A . ①②③⑥
B . ①③⑥
C . ①③④⑤
D . ①②⑥
元素a、b、c、d、e为前20号主族元素,原子序数依次增大。b元素原子最外层电子数与核外电子总数之比为2:3;c的氢化物能与其最高价氧化物对应的水化物反应生成一种盐;a与b、c均可以形成电子总数为10的分子;d元素的氧化物能使品红溶液褪色,且加热后品红颜色复原;e原子是前20号主族元素中原子半径最大的。请回答:
-
(1) e元素在周期表中的位置。
-
(2) bd2的电子式;e2d的电子式;ca3的空间构型。
-
(3) e的最高价氧化物的水化物所含化学键类型为、,晶体类型为。其溶液与b的最高价氧化物反应的离子方程式为。
-
(4) 在常温常压下,1g b的最简单气态氢化物完全燃烧放出的热量约为56kJ,写出该反应的热化学方程式。
下列说法不正确的是( )
A . 硅晶体和二氧化硅晶体中都含共价键
B . 冰和干冰熔化时克服的作用力均为分子间作用力
C . 硫晶体和硫酸钠晶体均属于离子晶体
D . 氯气和四氯化碳分子中每个原子的最外电子层都形成了具有8个电子的稳定结构
下面有关晶体的叙述中,错误的是( )
A . 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B . 氯化钠晶体中,每个Na+周围距离相等且紧邻的Na+共有6个
C . 氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D . 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
下列关于晶体的说法中,错误的是( )
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小
⑤晶胞是晶体结构的基本单元
⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定
⑦CsCl和NaCl晶体中阴、阳离子的配位数都为6
A . ①②③
B . ②③④
C . ④⑤⑥
D . ②③⑦
下列有关晶体的叙述中错误的是( )
A . 石墨的层状结构中碳碳键键长比金刚石中碳碳键键长短
B . 氯化钠晶体中每个 Na+周围紧邻的有6个Cl-
C . CsCl 晶体中,与每个 Cs+周围紧邻的有 8 个Cl-和 8 个 Cs+
D . 在面心立方最密堆积的金属晶体中,每个金属原子周围紧邻的有 12 个金属原子
下列晶体的分类正确的一组是( )
|
选项 |
离子晶体 |
共价晶体 |
分子晶体 |
金属晶体 |
|
A |
|
石墨 |
Ar |
Hg |
|
B |
|
金刚石 |
|
Ag |
|
C |
|
SiC |
|
Mg |
|
D |
|
Si |
|
NaH |
A . A
B . B
C . C
D . D
下列关于离子晶体的说法正确的是( )
A . 形成离子晶体的阴、阳离子之间只存在静电引力
B . 阴、阳离子的配位数只与阴、阳离子的电荷比有关
C . 离子化合物的熔点一定比共价化合物的熔点高
D . 熔融状态下离子键被破坏,使离子自由移动从而导电
下列说法中正确的是( )
A . 在晶体中有阳离子不一定有阴离子
B . 硫单质熔点高于白磷的原因是S-S键键能大于P-P键键能
C . 离子晶体中可能存在共价键,而分子晶体中肯定存在共价键
D . 对于组成和结构相似的分子晶体,相对分子质量越大,熔、沸点一定越高
类推是化学学习和研究中常用的思维方法,下列类推正确的是( )
A . H2O2的热稳定性比H2O的弱,则C2H6的热稳定性比CH4的弱
B . 晶体中有阴离子,必有阳离子,则晶体中有阳离子,也必有阴离子
C . Mg—Al原电池,Mg的活泼性比Al强,在稀硫酸介质中,Mg做负极,则在稀氢氧化钠介质中,也是Mg做负极
D . 根据反应Fe(OH)3+3HCl=FeCl3+3H2O,可类推反应Fe(OH)3+3HI=FeI3+3H2O
钴的一种化合物的晶胞结构如图所示,下列说法错误的是( )
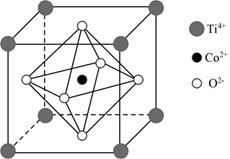
A . 元素钛在元素周期表中的位置为第四周期ⅣB族
B . 基态  的核外电子排布式为
的核外电子排布式为 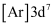 C . 该化合物的化学式为
C . 该化合物的化学式为 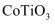 D . 与
D . 与  距离最近的
距离最近的  有4个
有4个
 的核外电子排布式为
的核外电子排布式为 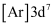 C . 该化合物的化学式为
C . 该化合物的化学式为 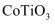 D . 与
D . 与  距离最近的
距离最近的  有4个
有4个
冰晶石是一种在自然界存在的矿物(化学式为 ),熔点
),熔点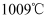 , 如图所示为冰晶石的晶胞。图中“●”位于大立方体的顶点和面心,“○”位于大立方体的12条棱的中点和8个小立方体的体心。则下列说法错误的是( )
, 如图所示为冰晶石的晶胞。图中“●”位于大立方体的顶点和面心,“○”位于大立方体的12条棱的中点和8个小立方体的体心。则下列说法错误的是( )
 ),熔点
),熔点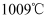 , 如图所示为冰晶石的晶胞。图中“●”位于大立方体的顶点和面心,“○”位于大立方体的12条棱的中点和8个小立方体的体心。则下列说法错误的是( )
, 如图所示为冰晶石的晶胞。图中“●”位于大立方体的顶点和面心,“○”位于大立方体的12条棱的中点和8个小立方体的体心。则下列说法错误的是( )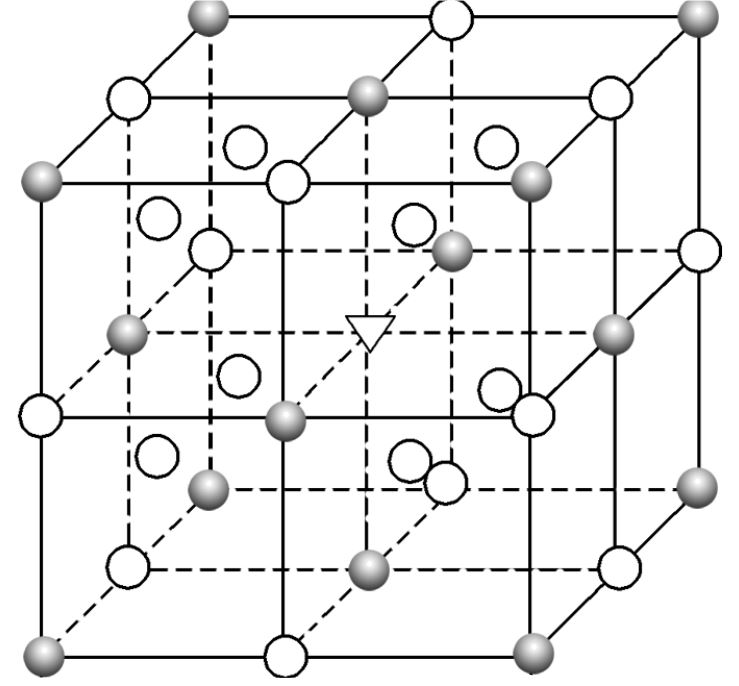
A . 冰晶石的名称是六氟合铝酸钠
B . 该物质中存在离子键和共价键
C . 大立方体的体心处“△”代表的是 D . 该物质是工业电解氧化铝制取金属铝的助熔剂
D . 该物质是工业电解氧化铝制取金属铝的助熔剂
 D . 该物质是工业电解氧化铝制取金属铝的助熔剂
D . 该物质是工业电解氧化铝制取金属铝的助熔剂
下列叙述中正确的是( )
A . 在 中,Cu为配位原子,NH3为配体
B . 冰分子内氢氧原子间以共价键形成的晶体中,每个水分子周围有4个紧邻的水分子
C . HI的相对分子质量大于HF,所以HI的沸点高于HF
D . CaO2和CaH2均是含有共价键的离子晶体
中,Cu为配位原子,NH3为配体
B . 冰分子内氢氧原子间以共价键形成的晶体中,每个水分子周围有4个紧邻的水分子
C . HI的相对分子质量大于HF,所以HI的沸点高于HF
D . CaO2和CaH2均是含有共价键的离子晶体
 中,Cu为配位原子,NH3为配体
B . 冰分子内氢氧原子间以共价键形成的晶体中,每个水分子周围有4个紧邻的水分子
C . HI的相对分子质量大于HF,所以HI的沸点高于HF
D . CaO2和CaH2均是含有共价键的离子晶体
中,Cu为配位原子,NH3为配体
B . 冰分子内氢氧原子间以共价键形成的晶体中,每个水分子周围有4个紧邻的水分子
C . HI的相对分子质量大于HF,所以HI的沸点高于HF
D . CaO2和CaH2均是含有共价键的离子晶体
下列有关物质结构与性质的叙述正确的是( )
A . 等离子体是只由离子组成的具有带电性的气态物质
B . 1molCo3+的八面体配合物[CoClx(NH3)y]Clz与足量AgNO3溶液作用生成2molAgCl沉淀,则x、y、z的值分别为2、4、2
C . 若MgO的化学键中离子键的百分数为50%,则MgO可看作离子晶体与共价晶体之间的过渡晶体
D . 利用超分子的自组装特征,可以分离C60和C70
最近更新
- 2019年3月22日-28日是第三十二届“中国水周”,活动的宣传主题为“坚持节水优先,强化水资源管理”。下列有关水的说法
- 设集合A={x||4x-1|≥9,x∈R},B={x|≥0,x∈R},则A∩B等于 ( )A.(-3,-2]
- 常温下,下列各组离子在指定溶液中一定能大量共存的是() A.使甲基橙变红色的溶液:Mg2+、K+、SO42- 、NO3-
- 某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应经过一段时间后达到平衡。反应过程中测定的
- 王老师要做一个关于法国资产阶级革命的课件,下列从网上搜集的资料中可用的有 ( )①攻占巴士底狱 ②《人权宣言》 ③处
- 已知某几何体的三视图如上,则该几何体的表面积是 。
- 用15.8g KMnO4氧化密度为1.19g/cm3,溶质质量分数为36.5%的盐酸.反应方程式如下:2KMnO4 +
- 下列词语中加点字的读音完全正确的一项是 A.狡黠(xiá)窈窕(yǎo) 参差(cī) 缄默(qiān) B.觊觎
- (16分)阅读下列材料,回答问题。 材料一:几乎每一位西方作者写到中国社会状况时毫无例外地要描述一番中国人吸食鸦片的方式
- 11.阅读下面的文字,完成(1)~(4)题。(25分) 阅读下面文字,完成(1)--(4)题(25分) 为生存辍学走上写
- 设数列{ }的通项公式为( ),其前n项和为Tn,则 A.1 B.
- 甲午中日战争所产生的影响和后果有( ) ①列强对中国的经济侵略进一步加深 ②中国丧失了更多的领土和主权
- 研究性学习小组同学用下图所示实验装置测定果蝇幼虫的呼吸速率。实验开始时,打开软管夹,将装置放入25℃水浴中,10分钟后关
- 人们常说“水比油重”,在学过密度以后应该怎样说才确切,为什么?
- 设椭圆上一点到左准线的距离为10,是该椭圆的左焦点,若点满足,则.
- 完形填空A generation gap (代沟) has become a serious problem. I re
- 下列离子方程式不正确的是 D.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O
- 下列不属于细胞凋亡现象的是 ( ) ①霜冻导致香蕉植株死亡 ②蝌蚪发育成为青蛙过程中尾部消失 ③寄主细
- We have a l__________(本地的) newspaper in our city.