离子晶体 知识点
离子晶体: 由正、负离子或正、负离子集团按一定比例通过离子键结合形成的晶体称作离子晶体,离子晶体属于离子化合物中的一种特殊形式,不能称为分子。强碱、活泼性金属氧化物和大多数的盐类均为离子晶体。
离子晶体 知识点题库
关于晶体的下列说法正确的是( )
A . 分子晶体的熔点不一定比金属晶钵熔点低
B . 离子晶体中一定含金属阳离子
C . 在共价化合物分子中各原子都形成8电子结构
D . 只要含有金属阳离子的晶体就一定是离子晶体
仅由下列各组元素所组成的化合物,不可能形成离子晶体的是( )
A . H O S
B . Na H O
C . K Cl O
D . H N Cl
下面有关晶体的叙述中,正确的是( )
A . 在氯化钠晶体中每个Na+(或Cl﹣)周围都紧邻8个Cl﹣(Na+)
B . 原子晶体中只存在共价键
C . 离子晶体和分子晶体在熔化时,化学键都被破坏
D . 熔融状态下能导电的晶体一定是金属晶体
关于下列几种离子晶体,说法不正确的是( )
A . 由于NaCl 晶体和CsCl晶体中正负离子半径比( 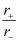 )不相等,所以两晶体中离子的配位数不相等
B . CaF2晶体中,Ca2+配位数为8,F﹣配位数为4不相等,主要是由于F﹣、Ca2+电荷(绝对值)不相同
C . MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大
D . MCO3中M2+半径越大,MCO3热分解温度越低
)不相等,所以两晶体中离子的配位数不相等
B . CaF2晶体中,Ca2+配位数为8,F﹣配位数为4不相等,主要是由于F﹣、Ca2+电荷(绝对值)不相同
C . MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大
D . MCO3中M2+半径越大,MCO3热分解温度越低
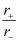 )不相等,所以两晶体中离子的配位数不相等
B . CaF2晶体中,Ca2+配位数为8,F﹣配位数为4不相等,主要是由于F﹣、Ca2+电荷(绝对值)不相同
C . MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大
D . MCO3中M2+半径越大,MCO3热分解温度越低
)不相等,所以两晶体中离子的配位数不相等
B . CaF2晶体中,Ca2+配位数为8,F﹣配位数为4不相等,主要是由于F﹣、Ca2+电荷(绝对值)不相同
C . MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大
D . MCO3中M2+半径越大,MCO3热分解温度越低
下列晶体分类中正确的一组是( )
选项 | 离子晶体 | 原子晶体 | 分子晶体 |
A | NaOH | Ar | SO2 |
B | K2SO4 | 石墨 | S |
C | CH3COONa | 水晶 |
|
D | Ba(OH)2 | 金刚石 | 玻璃 |
A . A
B . B
C . C
D . D
几种晶体的晶胞如图所示:
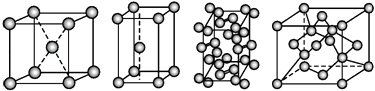
所示晶胞从左到右分别表示的物质正确的排序是( )
A . 碘、锌、钠、金刚石
B . 金刚石、锌、碘、钠
C . 钠、锌、碘、金刚石
D . 锌、钠、碘、金刚石
下列说法正确的是:( )
①NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
②含有共价键的晶体一定具有高的熔、沸点及硬度
③s-s σ键与s-p σ键的电子云形状相同
④含有π键的化合物与只含σ键的化合物的化学性质不同
⑤中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
⑥配位键在形成时,是由成键双方各提供一个电子形成共用电子对
A . ①②⑤
B . ①④⑤
C . ②③⑤
D . ②③⑥
根据表中给出物质的熔点数据(AlCl3沸点为260 ℃),判断下列说法错误的是( )
晶体 | NaCl | MgO | SiCl4 | AlCl3 | 晶体硼 |
熔点/℃ | 801 | 2 800 | -70 | 180 | 2 500 |
A . MgO中的离子键比NaCl中的离子键强
B . SiCl4晶体是分子晶体
C . AlCl3晶体是离子晶体
D . 晶体硼是原子晶体
下图是CaF2晶胞的结构。下列说法正确的是 ( )
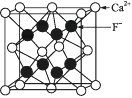
A . 一个CaF2晶胞中含有8个Ca2+
B . 一个CaF2晶胞中含有8个F-
C . 在CaF2晶胞中Ca2+的配位数为4
D . 在CaF2晶胞中F-的配位数为8
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法错误的是( )
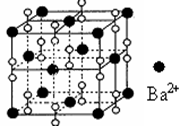
A . 该晶体属于离子晶体
B . 晶体的化学式为Ba2O2
C . 该晶体晶胞结构与NaCl相似
D . 与每个Ba2+距离相等且最近的Ba2+共有12个
下列有关晶体的说法正确的是( )
A . 分子晶体中一定不含离子键
B . 分子晶体中一定含有共价键
C . 离子晶体中一定只含离子键
D . 离子晶体的熔点一定比共价化合物高
如图是从NaCl和CsCl晶体结构中分割出来的部分结构图,其中属于从NaCl晶体中分割出来的结构图是( )
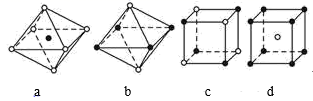
A . 只有c
B . b和c
C . a和c
D . a和d
下面的排序错误的是( )
A . 沸点的高低:乙醇>丙烷
B . 硬度由大到小:金刚石>碳化硅>晶体硅
C . 熔点由高到低:Na>Mg>Al
D . 晶格能由大到小:NaF>NaCl>NaBr>NaI
下列叙述错误的是( )
A . 某物质熔融状态可导电,固态可导电,将其投入水中所形成的水溶液也可导电,则可推测该物质只可能是金属单质
B . 晶体中只要有阴离子,就一定有阳离子;有阳离子不一定有阴离子
C . MgO的熔点比MgCl2高主要是因为MgO的晶格能比MgCl2大
D . 离子晶体中只可能存在阴、阳离子
下列有关氯化钠晶体的叙述中,正确的是( )
A . 氯化钠晶体是由钠离子和氯离子构成的,所以氯化钠晶体能导电
B . 钠离子和氯离子之间因静电吸引而形成氯化钠晶体
C . 氯化钠的分子式为NaCl
D . 每个钠离子周围吸引6个氯离子,每个氯离子周围同样吸引6个钠离子
有关晶体的结构如图所示,下列说法中错误的是( )
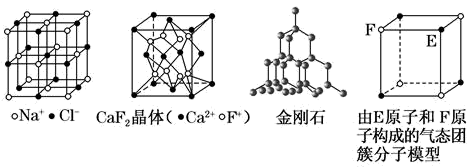
A . 在 晶体中,距
晶体中,距 最近的
最近的 有6个,距
有6个,距 最近且等距的
最近且等距的 共12个
B . 在
共12个
B . 在 晶体中,每个晶胞平均占有4个
晶体中,每个晶胞平均占有4个 ,
, 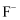 的配位数是4
C . 在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面
D . 该气态团簇分子的分子式为
的配位数是4
C . 在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面
D . 该气态团簇分子的分子式为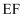 或
或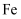 , 其晶体不导电
, 其晶体不导电
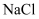 晶体中,距
晶体中,距 最近的
最近的 有6个,距
有6个,距 最近且等距的
最近且等距的 共12个
B . 在
共12个
B . 在 晶体中,每个晶胞平均占有4个
晶体中,每个晶胞平均占有4个 ,
, 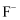 的配位数是4
C . 在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面
D . 该气态团簇分子的分子式为
的配位数是4
C . 在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面
D . 该气态团簇分子的分子式为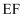 或
或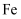 , 其晶体不导电
, 其晶体不导电
NH4Cl的晶胞为立方体,其结构如下。下列说法错误的是( )

A . NH4Cl晶体属于离子晶体
B . NH4Cl晶胞中H-N-H键角为90°
C . NH4Cl晶体中既有离子键又有共价键
D . 每个Cl-周围与它最近且等距离的  的数目为8
的数目为8
 的数目为8
的数目为8
有关晶体的结构如图所示,下列说法中错误的是( )
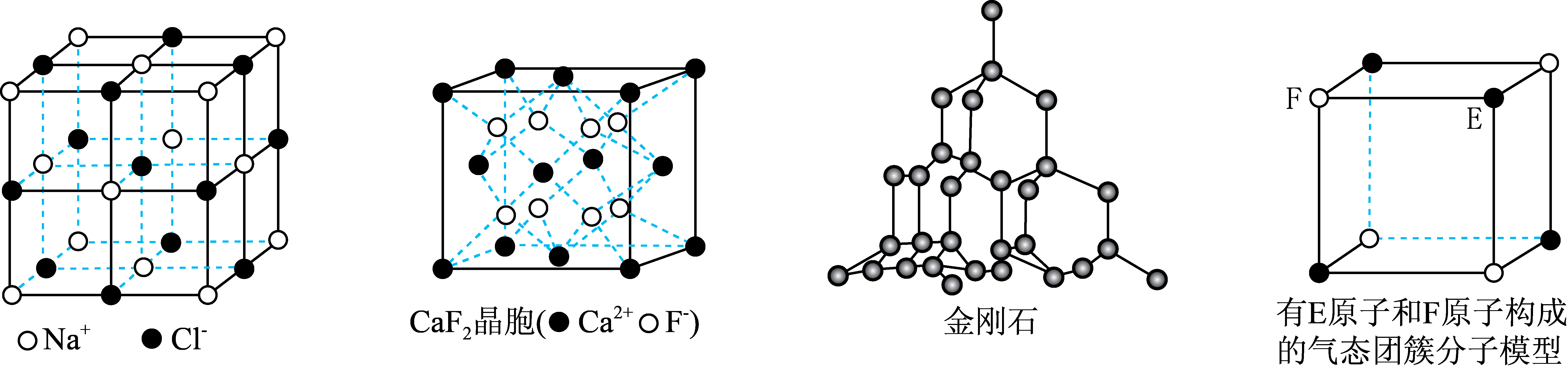
A . 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B . 在CaF2晶体中,F-的配位数为8
C . 在金刚石晶体中,碳原子与碳碳键个数的比为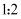 D . 该气态团簇分子的分子式为EF或FE
D . 该气态团簇分子的分子式为EF或FE
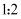 D . 该气态团簇分子的分子式为EF或FE
D . 该气态团簇分子的分子式为EF或FE
钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞的结构如图所示,下列有关说法中错误的是( )
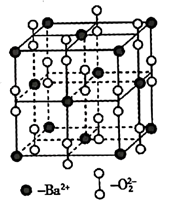
A . 该晶体属于离子晶体
B . 该晶体的晶胞结构与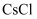 相似
C . 晶体的化学式为
相似
C . 晶体的化学式为 D . 晶体中
D . 晶体中 的配位数与
的配位数与 的配位数之比为
的配位数之比为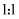
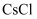 相似
C . 晶体的化学式为
相似
C . 晶体的化学式为 D . 晶体中
D . 晶体中 的配位数与
的配位数与 的配位数之比为
的配位数之比为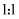
下列说法正确的是( )
A . 晶体在受热熔化过程中一定存在化学键的断裂
B . 原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力
C . 区分晶体和非晶体最科学的方法是对固体进行X射线衍射实验
D . 非金属元素的原子间只形成共价键,金属元素的原子与非金属元素的原子间只形成离子键
最近更新
- 下图表示三个神经元及其联系。其中:“—O—<”表示一个完整的神经元模式(即从树突到胞体,再到轴突及末梢),为了研究
- 俗语说:种瓜得瓜,种豆得豆。从细胞结构上看,这主要取决于:( ) A.细胞壁 B.细胞膜 C.细
- 在空间四边形中,、、、上分别取、、、四点,如果、交于一点,则( ) A.一定在直线上 B.一定
- 下列做法是为了加快液体蒸发的是( )A.酒精灯不用时要盖上灯帽B.洗头后用电吹风把头发吹干C.农业灌溉中用管道输水代
- 如图甲所示,放在光滑面上的木块受到两个水平力F1与F2的作用而静止不动,现保持Fl大小和方向不变,F2方向不变,使F2随
- 下列物质与水混合后静置,不出现分层的是( ) A. 乙醇 B. 苯 C. 三氯甲烷 D. 四氯化
- (本小题满分13分) 袋中装有大小形状完全相同的3个黑球和2个白球,现先掷一粒特制的骰子一次(质地均匀的小正方体的六个面
- 关于相互接触的两个物体之间的弹力和摩擦力,以下说法正确的是( )A.有弹力必定有摩擦力B.有摩擦力必定有弹力C.若
- 水资源是战略资源.下列是节水标识的是()A.B.C.D.
- 根据句意及所给汉语意思写出所缺单词。 1. Paris is the _________(首都)ofFrance.
- --- Can I walkacross the road now, Mrs. Chen? ---No, y
- 下图为细胞亚显微结构示意图,下列有关说法不正确的是 A.此图可用来表示低等植物细胞的亚显微结构 B.若此图表示洋葱根尖
- 某企业第一年把全部商品出售的价格为80万元。第二年,该企业扩大经营规模10%,同时这一年社会出现通货紧缩。若其他条件不变
- (2012年5月湖北武汉模拟)如图甲所示,理想变压器原、副线圈的匝数比是50∶l,P是原线圈的中心抽头,图中电表均为理想
- 下图说明,带宠物到公共场所应该A.关爱宠物 B.加强对宠物的教管
- 下列符号能同时表示一个原子、一种元素和一种物质的是 ( ) A. O2
- ---Would youlike to have some tea or coffee? ---________.
- 化石燃料仍是目前能源的主体,但已经面临危机,开发新能源是解决能源问题的关键.下列能量转换过程,不涉及化学变化的是() A
- 曾用作麻醉剂的“笑气”是一种氮氧化物,其中氮元素的化合价为+1价,“笑气”的化学式是: (A)N2O5
- 将大白鼠从25℃移至0℃的环境中,大白鼠将出现的生理反应是 A.耗氧量减少,竖毛肌舒张



