离子晶体 知识点题库
类推的思维方法在化学学习和研究中常会产生错误的结论,因此类推出的结论最终要经过实践的检验才能决定其正确与否。下列几种类推结论中正确的是 ( )
A . 第二周期元素氢化物稳定性顺序是HF>H2O>NH3;则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3
B . Fe3O4可写成FeO·Fe2O3;Pb3O4也可写成PbO·Pb2O3
C . 可电解熔融MgCl2来制取金属镁;也能电解熔融AlCl3来制取金属铝
D . 晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子
下列物质中不属于离子晶体的是( )
A . 氯化铵
B . 硫酸
C . 食盐
D . 氧化钠
现有几组物质的熔点(℃)的数据:
A组 | B组 | C组 | D组 |
金刚石:3 550 | Li:181 | HF:-83 | NaCl:801 |
硅晶体:1 410 | Na:98 | HCl:-115 | KCl:776 |
硼晶体:2 300 | K:64 | HBr:-89 | RbCl:718 |
二氧化硅:1 723 | Rb:39 | HI:-51 | CsCl:645 |
据此回答下列问题:
-
(1) A组属于晶体,其熔化时克服的微粒间的作用力是。
-
(2) B组晶体共同的物理性质是 (填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
-
(3) C组中HF熔点反常是由于 。
-
(4) D组晶体可能具有的性质是(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电
④熔融状态能导电
-
(5) D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因解释为 。
有关晶体的结构如下图所示,则下列说法中错误的是( )
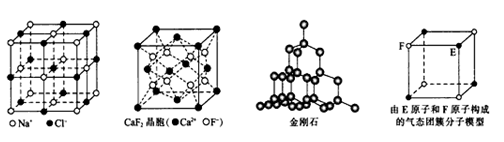
A . 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B . 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C . 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D . 该气态团簇分子的分子式为EF或FE
下列各项的叙述中都包含两个数值,前一数值大于后一数值的是( )
A . 氨分子中N﹣H键的键角和甲烷分子中C﹣H键的键角
B . NaCl晶体中与一个Cl﹣紧邻的Na+数和CsCl晶体中与一个Cl﹣紧邻的Cs+数
C . 晶体硅中Si﹣Si键的键能和金刚石中C﹣C键的键能
D . 单质碘中的分子间作用力和干冰中的分子间作用力
-
(1) 已知甘氨酸的熔点是 233℃,而二苯胺的熔点只有 53℃,为什么甘氨酸的熔点高。
-
(2) 相同条件下HF酸性比H2CO3强,请用一个化学方程式说明。
-
(3) NF3的一种下游产品三聚氟氰(分子式为:C3N3F3),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式。
下列说法正确的是( )
A . 水的沸点较高是因为水分子间存在较强的化学键
B . 离子晶体中可能存在共价键, 而分子晶体中一定存在共价键
C . CO2与 SiO2 均为共价化合物,其固体熔化时,均破坏了分子间作用力
D . 某物质熔点 1067℃, 易溶于水,其水溶液和熔融态均能导电,其晶体一定为离子晶体
下列说法正确的是( )
A . 金刚石和石英晶体都是原子晶体,都属于共价化合物
B . NaOH和MgCl2晶体中都含有共价键,但都属于离子晶体
C . 氮化镁中每个离子的最外电子层都形成了具有8个电子的稳定结构
D . NaCl溶液蒸发结晶过程中,有离子键的形成,但没有分子间作用力的破坏
B和Al为同主族元素,下列说法错误的是( )
A . H3BO3为一元酸,Al(OH)3呈两性
B . 晶体B可能有脆性,Al有延展性
C . BF3和AlF3都可以与F- 形成离子键
D . B和Al分别与N都能形成具有较高硬度和熔点的物质
下列有关分子与晶体的说法正确的是( )
A . 金刚石、氮化硼、C60熔化需克服的作用力类型相同
B . 晶体中有阴离子,必有阳离子;反之晶体中有阳离子,也必有阴离子
C . 钋单质为简单立方堆积,则晶胞中钋原子配位数为6
D . COS 与CO2互为等电子体,故COS 是直线形的非极性分子
下列关于晶体的说法中错误的是( )
A . 固态不导电而熔融状态导电的晶体一定是离子晶体
B . 金属晶体中一定含有金属键,金属键没有方向性和饱和性
C . 熔点是10.31 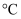 ,液态不导电,水溶液能导电的晶体一定是分子晶体
D . 具有正四面体结构的晶体,可能是共价晶体或分子晶体,其键角都是
,液态不导电,水溶液能导电的晶体一定是分子晶体
D . 具有正四面体结构的晶体,可能是共价晶体或分子晶体,其键角都是 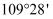 。
。
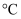 ,液态不导电,水溶液能导电的晶体一定是分子晶体
D . 具有正四面体结构的晶体,可能是共价晶体或分子晶体,其键角都是
,液态不导电,水溶液能导电的晶体一定是分子晶体
D . 具有正四面体结构的晶体,可能是共价晶体或分子晶体,其键角都是 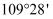 。
。
下列叙述正确的是( )
A . 镁晶体中1个  只与2个价电子存在强烈的相互作用
B . 在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性
C . 熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体
D . 离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关
只与2个价电子存在强烈的相互作用
B . 在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性
C . 熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体
D . 离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关
 只与2个价电子存在强烈的相互作用
B . 在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性
C . 熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体
D . 离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关
只与2个价电子存在强烈的相互作用
B . 在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性
C . 熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体
D . 离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关
2020年12月17日凌晨1时59分,“嫦娥五号”首次实现了我国地外天体采样返回,标志着我国航天事业迈出了一大步。带回的月壤中包含了H、O、N、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:
-
(1) 锌(Zn)、镉(Cd)位于同一副族相邻周期,Cd的原子序数更大,则基态Cd原子的价电子轨道表示式(电子排布图)为。
-
(2) S与O可形成多种微粒,其中SO
 的空间构型为;液态SO3冷却到289.8K时,能得到一种螺旋状单链结构的固体,其结构如图所示,此固态SO3中S原子的杂化轨道类型是 。
的空间构型为;液态SO3冷却到289.8K时,能得到一种螺旋状单链结构的固体,其结构如图所示,此固态SO3中S原子的杂化轨道类型是 。 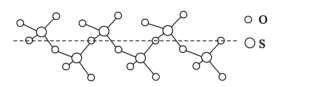
-
(3) 重铬酸铵为桔黄色单斜结晶,常用作有机合成催化剂,Cr2O
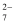 的结构如图所示。则1mol重铬酸铵中含σ键与π键个数比为。
的结构如图所示。则1mol重铬酸铵中含σ键与π键个数比为。 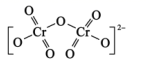
-
(4) α-Al2O3是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054℃)、硬度大的特点,主要原因为。
-
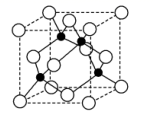
(5) 一种铜金合金具有储氢功能,其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为。该储氢材料储氢时,氢分子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图),该晶体储氢后的化学式为。
-
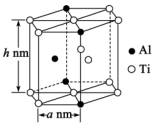
(6) “嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),已知该结构单元底面(正六边形)边长为anm,该合金的密度为ρg·cm-3 , 则高为h=nm(列出计算式,NA为阿伏加德罗常数的值)。
晶体的结构如下图所示,下列说法中错误的是( )
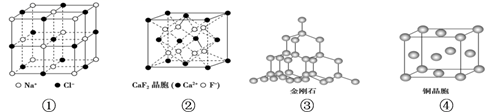
A . 在图①NaCl晶体中,距Na+最近的Cl-形成正八面体
B . 在图②CaF2晶体中,每个晶胞平均占有4个Ca2+
C . 在图③金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D . 图④表示铜晶体为面心立方堆积,铜原子的配位数为8
北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构分析正确的是( )
A . K3C60中既有离子键又有极性键
B . 1molK3C60中含有的离子数目为63×6.02×1023
C . 该晶体在熔融状态下能导电
D . 该物质的化学式可写作KC20
已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间均以单键结合,下列关于晶体说法正确的是( )
A . C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子
B . C3N4晶体中,C—N键的键长比金刚石中C—C键的键长要长
C . C3N4晶体是分子晶体
D . C3N4晶体中微粒间通过离子键结合
工业上通过Al2O3+N2+3C 2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( )
2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( )
 2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( )
2AlN+3CO可制得高温陶瓷材料AlN。下列说法正确的是( )
A . N2的电子式为: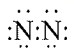 B . AlN是分子晶体
C . 27Al用原子中的中子数为14
D . 基态氮原子轨道表示式:
B . AlN是分子晶体
C . 27Al用原子中的中子数为14
D . 基态氮原子轨道表示式: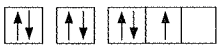
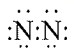 B . AlN是分子晶体
C . 27Al用原子中的中子数为14
D . 基态氮原子轨道表示式:
B . AlN是分子晶体
C . 27Al用原子中的中子数为14
D . 基态氮原子轨道表示式:
下列有关晶体的说法中一定正确的是( )
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤分子晶体的堆积均为分子密堆积
⑥离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
⑦金属晶体和离子晶体都能导电
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
A . ①③⑦
B . 只有⑥
C . ②④⑤⑦
D . ⑤⑥⑧
 晶体在熔融状态下能够导电,下图为该晶体的立方晶胞结构示意图,该结构也被称为反萤石结构。下列说法正确的是( )
晶体在熔融状态下能够导电,下图为该晶体的立方晶胞结构示意图,该结构也被称为反萤石结构。下列说法正确的是( )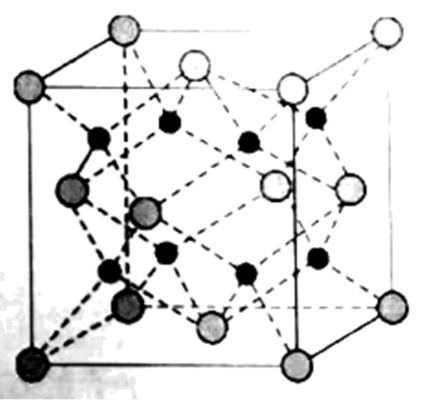
A . 该晶体属于离子晶体
B .  熔点比
熔点比 高
C . 该晶体中Li和O的配位数之比为2∶1
D . 若该晶体密度为
高
C . 该晶体中Li和O的配位数之比为2∶1
D . 若该晶体密度为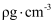 , 则该晶体的晶胞参数为
, 则该晶体的晶胞参数为 (NA为阿伏加德罗常数的值)
(NA为阿伏加德罗常数的值)
 熔点比
熔点比 高
C . 该晶体中Li和O的配位数之比为2∶1
D . 若该晶体密度为
高
C . 该晶体中Li和O的配位数之比为2∶1
D . 若该晶体密度为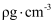 , 则该晶体的晶胞参数为
, 则该晶体的晶胞参数为 (NA为阿伏加德罗常数的值)
(NA为阿伏加德罗常数的值)
钙钛矿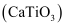 型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
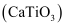 型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
-
(1) 基态
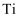 原子的价层电子排布式为。
原子的价层电子排布式为。
-
(2) 已知组成和结构相似的物质,物质的熔点随着相对分子量的增大而增大。
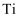 的四卤化物熔点如下表所示,解释
的四卤化物熔点如下表所示,解释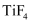 熔点出现反常的原因是。
熔点出现反常的原因是。化合物
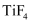


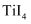
熔点/
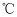
377
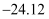
38.3
155
-
(3)
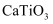 的晶胞如图(a)所示,其组成元素钙位于元素周期表中的区(填s、p、d、
的晶胞如图(a)所示,其组成元素钙位于元素周期表中的区(填s、p、d、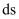 ),钙和镓的第一电离能大小顺序是,图示晶胞中
),钙和镓的第一电离能大小顺序是,图示晶胞中 的配位数是。
的配位数是。
-
(4) 一种立方钙钛矿结构的金属卤化物光电材料的组成为
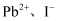 和有机碱离子
和有机碱离子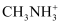 , 其晶胞如图(b)所示。有机碱
, 其晶胞如图(b)所示。有机碱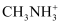 中有配位键,提供空轨道的微粒是;图(a)中的
中有配位键,提供空轨道的微粒是;图(a)中的 与图(b)中的空间位置相同,若晶胞参数(边长)为
与图(b)中的空间位置相同,若晶胞参数(边长)为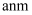 , 则晶体密度为
, 则晶体密度为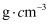 (列出计算式)。
(列出计算式)。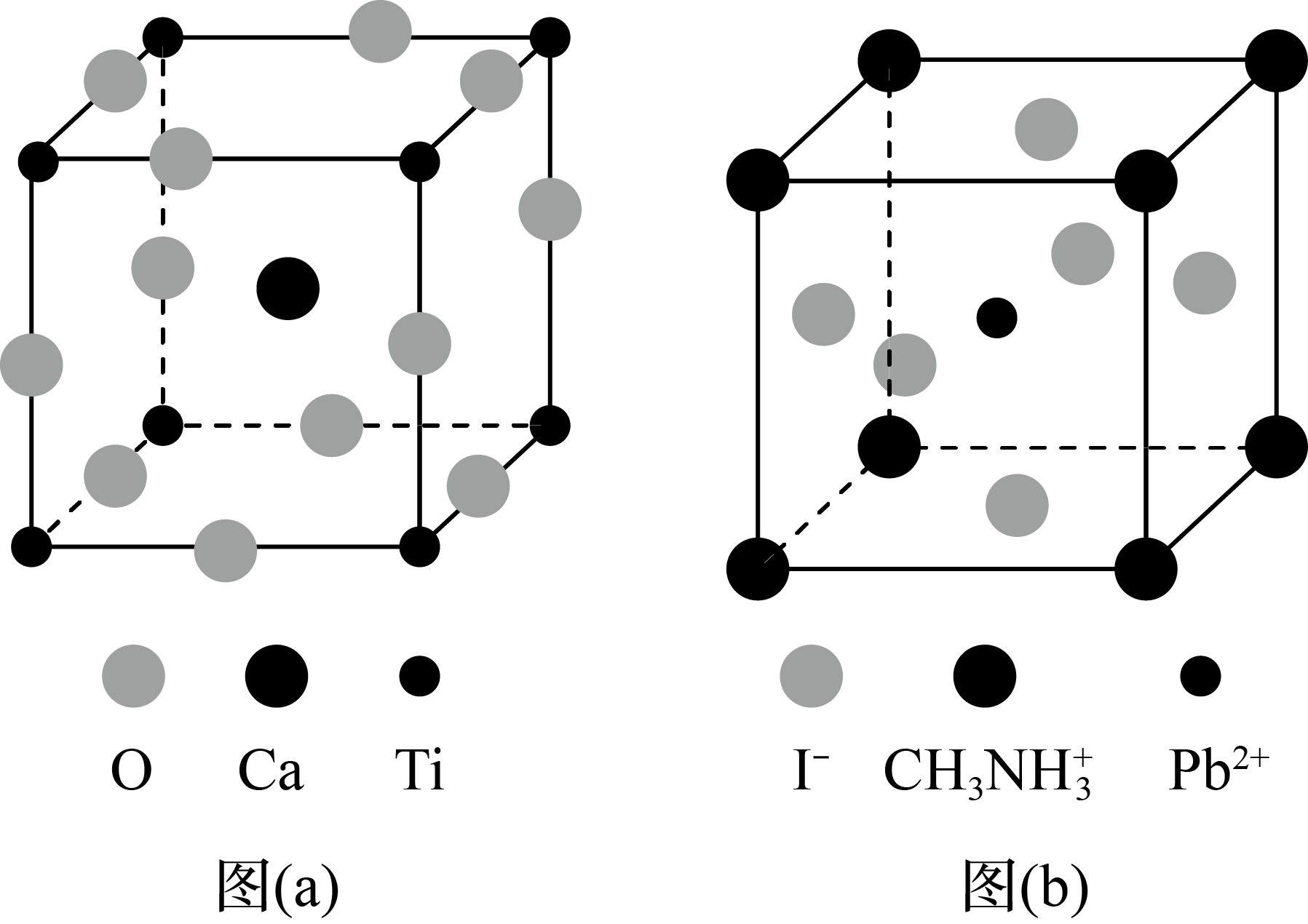
最近更新
- 3.神经细胞中含量最多的有机化合物是( ) A、蛋白质 B、糖类 C、脂质
- 把块煤做成蜂窝煤是为了() A.降低着火点 B.散热面积大 C.方便运输 D.使煤和空气充分接触
- 摔跤时,如果向后跌倒损伤了人脑的( ),则很有可能造成由于呼吸及心血管功能的紊乱而引起死亡。 A.大脑
- 1.依次填入下列各句横线处的成语,最恰当的一组是 ①生活中总有些人 ,平时吵闹不休,表现得很厉害,而真到紧要关头,他
- 江南是什么?气象学家说“江南是梅雨”,经济学家说“江南是财赋”,而地理学家说“江南是丘陵”。 31.江南丘陵的范围是(
- a2-2[a2-(2a2-b)]
- .如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是选项 试剂 现象 结论 A KMnO4酸性溶液 溶液褪色
- 第二届全国道德模范评选广泛吸引了人民群众的积极参与,集中展示了近年来公民道德建设的丰硕成果,使道德标准家喻户晓,深入人心
- 对胚胎分割技术的有关叙述正确的是 A.凡是利用胚胎工程产生新个体都要用到胚胎分割技术 B.分割的胚胎直接移植给受体或在体
- 下列语句中,没有语病的一项是( ) A.香港游客在菲律宾马尼拉市被劫持事件中,本应在几十秒内完成的突击,菲律宾警方
- 右图是小华设计的一种节能电梯工作原理图,R是一个力敏电阻,当电梯上无人时,力敏电阻受到的压力变小,阻值变大,电磁铁的磁性
- 函数的最小值为_____________。
- 在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0mol·L-1,用石墨作电极电解此溶液,当通电一段时间
- 对于A2+3B2═2C的反应,在不同条件下的化学反应速率表示中,反应速率最快的是( ) A. v(A2)=0.4mol/
- Rockclimbing is ___ great fun. You will get close to ____ n
- 在下列中学化学实验常见的实验装置中。 (1)请写出有标号仪器的名称:①__ ;②__ (2)若制取的一种气体是氧气,应选
- pH=1的两种一元酸HX和HY的溶液,分别取50mL,加入足量的镁粉,充分反应,收集的氢气的体积分别为V(HX)和V(H
- 若函数,则 ( ) A. B. C. D.
- (08年南安一中期末)(9分)某同学在做“利用单摆测重力加速度”的实验中,先测得摆线长为101.00cm,摆球直径为2.
- 我国少数民族主要分布在 A.东北 西北 西南 B.东北 西南 东南 C.东部和中部 D.西北 东南 西南



