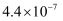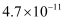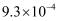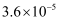电离平衡常数 知识点
电离平衡常数 知识点题库
 用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为
用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为  及少量的FeO、
及少量的FeO、  和
和  )为原料制备马日夫盐的主要工艺流程如图:
)为原料制备马日夫盐的主要工艺流程如图: 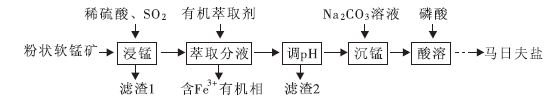
-
(1) “浸锰”过程中,FeO参与氧化还原反应的离子方程式为。
-
(2)
 的萃取率与溶液的pH的关系如图所示,当
的萃取率与溶液的pH的关系如图所示,当 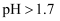 时,
时,  的萃取率急剧下降的原因可能为(用化学用语表示)。
的萃取率急剧下降的原因可能为(用化学用语表示)。 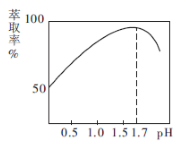
-
(3) “调pH”的最大范围为。
金属离子
开始沉淀的pH
完全沉淀的pH

l. 8
3.2

3.0
5.0

5.8
8.8

7.8
9.8
-
(4) 如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备
 ,需要控制温度在80℃~90℃之间的原因是,采用水浴加热,经蒸发浓缩、(填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
,需要控制温度在80℃~90℃之间的原因是,采用水浴加热,经蒸发浓缩、(填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。 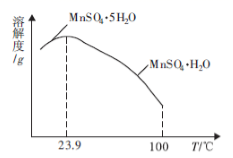
-
(5) 写出检验“沉锰”是否已完成的实验操作。
-
(6) 常温下,马日夫盐溶液显性(填“酸”或“碱”),理由是:。(写出计算过程并结合必要的文字说明。已知:
 的电离常数
的电离常数 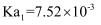 ,
, 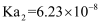 ,
, 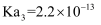 )
)
-
(1) Ⅰ.理论上稀的强酸、强碱反应生成1mol H2O(l)时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 。
-
(2) 已知:乙苯催化脱氢制苯乙烯反应:苯在计算键能时,此处可看作为
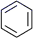 ,
, 
 +H2(g)
+H2(g) 化学键
C—H
C—C
C=C
H—H
键能/kJ·mol-1
412
348
612
436
计算上述反应的ΔH= kJ·mol-1。
-
(3) Ⅱ.25 ℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式
CH3COOH
H2CO3
HClO
电离平衡常数
1.7×10-5
K1=4.3×10-7 K2=5.6×10-11
3.0×10-8
CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为。
-
(4) 将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:。
| 弱酸 | 氢氟酸 | 硼酸[B(OH)3](一元酸) | 草酸(H2C2O4) |
| 电离平衡常数(25℃) | 6.6×10-4 | 5.8×10-10 | K1=5.9×10-2 K2=6.4×10-5 |
则下列有关说法错误的是( )
| 弱酸(或弱碱)化学式 | CH3COOH | NH3·H2O | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10–5 | 1.8×10–5 | K1=4.3×10–7 K2=5.6×10–11 |
在25℃时,下列有关电解质溶液的说法错误的是( )
|
化学式 |
CH3COOH |
H2CO3 |
HClO |
|
电离平衡常数 |
1.8×10-5 |
K1=4.3×10-7 K2=5.6×10-11 |
3.0×10-8 |
回答下列问题:
-
(1) 物质的量浓度为0.1mol/L的下列四种物质的溶液,pH由大到小的顺序是 (填编号)。
a.Na2CO3 b.NaClO c.CH3COONa d.NaHCO3
-
(2) 常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是___。A . c(H+) B .
 C . c(H+)·c(OH-)
D .
C . c(H+)·c(OH-)
D . 
-
(3) 电离平衡常数是用实验的方法测定出来的,现已经测得25℃时cmol/L的HX的电离度为a,试表示该温度下HX的电离平衡常数K=。(用含“c、a的代数式表示”)
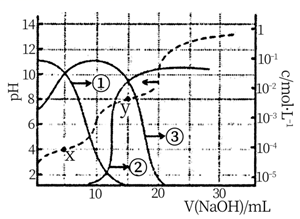
 、NH3·H2O、HCO
、NH3·H2O、HCO  、CO
、CO 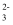 的分布如图(忽略溶液体积的变化)。已知常温下Kb(NH3·H2O)=1.8×10−5 , Ka1(H2CO3)=4.2×10−7 , Ka2(H2CO3)=5.6×10−11 , 则下列说法正确的是( )
的分布如图(忽略溶液体积的变化)。已知常温下Kb(NH3·H2O)=1.8×10−5 , Ka1(H2CO3)=4.2×10−7 , Ka2(H2CO3)=5.6×10−11 , 则下列说法正确的是( ) 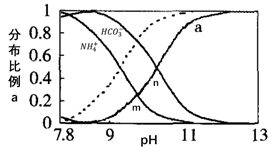
 )
C . n点时,溶液中3c(HCO
)
C . n点时,溶液中3c(HCO  )+c(OH⁻)=c(NH
)+c(OH⁻)=c(NH  )+c(H+)
D . 反应HCO
)+c(H+)
D . 反应HCO  +OH—
+OH—  CO
CO 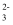 +H2O的平衡常数K=
+H2O的平衡常数K= 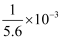
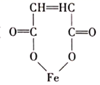 )是一种治疗贫血的药物,该药物与各种营养物质、抗生素的相容性好,具有协同作用。实验室利用糠醛(
)是一种治疗贫血的药物,该药物与各种营养物质、抗生素的相容性好,具有协同作用。实验室利用糠醛( 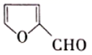 )和部分无机物可制备富马酸亚铁,制备的简易流程、实验装置如下:
)和部分无机物可制备富马酸亚铁,制备的简易流程、实验装置如下:
糠醛 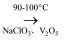
 富马酸晶体
富马酸晶体 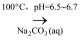
 粗产品
粗产品
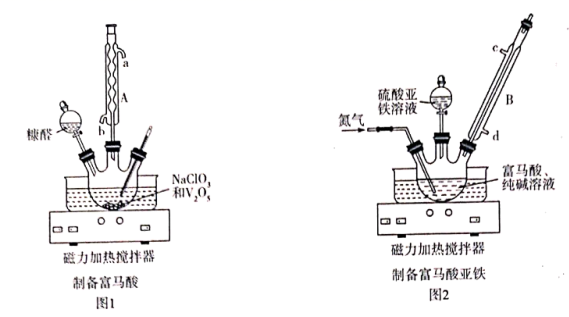
已知:①部分物质的性质如下:
|
物质 |
颜色、状态(常温) |
熔点/℃ |
沸点/℃ |
溶解性 |
|
糠醛 |
无色油状液体 |
-36 |
162 |
可溶( |
|
富马酸 |
无色晶体 |
299 |
355.5 |
微溶于冷水,易溶于热水 |
|
富马酸亚铁 |
红棕色粉末 |
>280 |
微溶于冷水,易溶于热水 |
②常温下,碳酸和富马酸的电离常数如下:
|
|
|
|
|
碳酸 |
|
|
|
富马酸 |
|
|
回答下列问题:
-
(1) 仪器A的名称是,作为冷凝回流装置,仪器A相比仪器B的优点是。
-
(2) 图1中
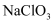 的作用是。
的作用是。
-
(3) 图2中通入氮气的目的是。
-
(4) 将富马酸晶体加入到热的纯碱溶液中发生反应的离子方程式是。
-
(5) 称取制备的粗产品
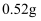 ,溶解在加热煮沸且冷却的稀硫酸(
,溶解在加热煮沸且冷却的稀硫酸( 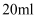 )中,然后用煮沸过的蒸馏水配成
)中,然后用煮沸过的蒸馏水配成 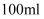 溶液,每次取
溶液,每次取 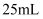 ,加入指示剂,马上用
,加入指示剂,马上用 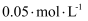 的
的  标准液滴定(
标准液滴定( 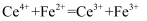 ),三次滴定消耗的标准液的体积平均值为
),三次滴定消耗的标准液的体积平均值为 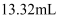 。
。
①用稀硫酸溶解富马酸亚铁的目的是。
②假设杂质不参与上述反应,粗产品的纯度为%(保留4位有效数字)。
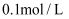 的
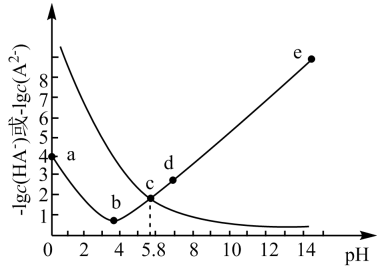
的  溶液体系中,含A粒子的分布系数
溶液体系中,含A粒子的分布系数  平衡时某粒子的浓度占各粒子浓度之和的分数
平衡时某粒子的浓度占各粒子浓度之和的分数  与溶液pH的关系如图所示.下列说法错误的是( )
与溶液pH的关系如图所示.下列说法错误的是( ) 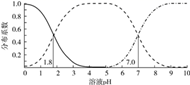
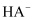 的电离常数
的电离常数 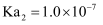 B . 室温下,
B . 室温下, 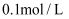 的NaHA溶液显酸性
C . 室温下,
的NaHA溶液显酸性
C . 室温下, 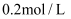 的
的  与
与 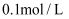 的NaOH溶液等体积混合,溶液
的NaOH溶液等体积混合,溶液 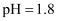 D .
D . 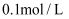 的
的  溶液中
溶液中 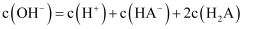
| 酸 | 电离常数(常温下) |
| CH3COOH | Ka=1.8×10-5 |
| H2CO3 | Ka1=4.3×10-7 , Ka2=5.6×10-11 |
| H2S | Ka1=9.1×10-8 , Ka2=1.1×10-12 |
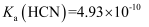 、
、 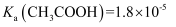 、
、 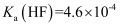 、
、 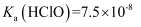 ,则常温下,等
,则常温下,等  的
的 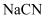 、
、 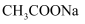 、
、 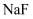 、
、 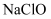 的浓度从大到小的顺序为( )
的浓度从大到小的顺序为( )
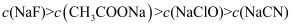 B .
B . 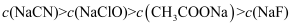 C .
C . 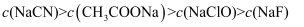 D .
D . 
 、体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入盐酸体积的变化曲线如图所示,d点两种溶液恰好完全反应。
、体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入盐酸体积的变化曲线如图所示,d点两种溶液恰好完全反应。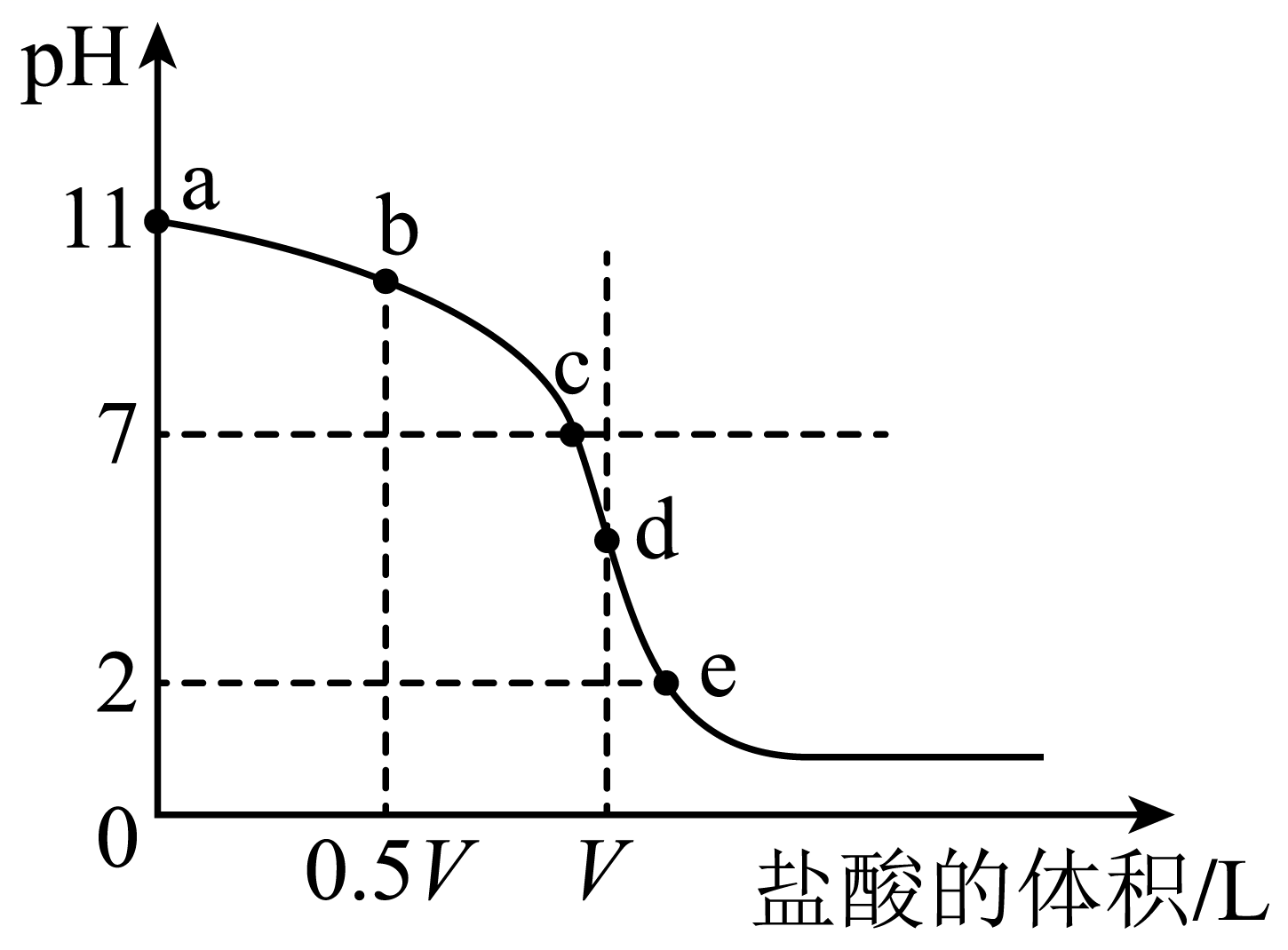
下列说法正确的是( )
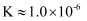 B . 由水电离出的
B . 由水电离出的 由大到小顺序:
由大到小顺序: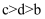 C . 由b点到c点的过程中,
C . 由b点到c点的过程中, 、
、 的值均增大
D . 滴定过程中可能有
的值均增大
D . 滴定过程中可能有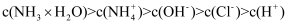
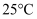 时
时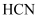 的
的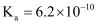 , 下列说法正确的是( )
, 下列说法正确的是( )
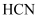 溶液样品的
溶液样品的 发现前者小于后者,可推测
发现前者小于后者,可推测 的
的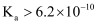 B .
B . 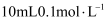 的
的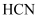 溶液中加入
溶液中加入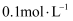 的
的 溶液,当溶液中水的电离程度与纯水相同时,
溶液,当溶液中水的电离程度与纯水相同时,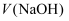 可能大于
可能大于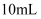 C . 向
C . 向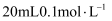 的
的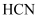 溶液中加入
溶液中加入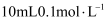 的
的 溶液充分反应,所得溶液中
溶液充分反应,所得溶液中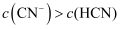 D . 将
D . 将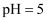 的
的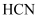 溶液与
溶液与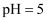 的盐酸混合,
的盐酸混合,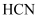 的电离度增大
的电离度增大
-
(1) 25℃时向浓度均为0.1mol/L的
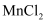 和
和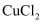 混合溶液中逐滴加入氨水,首先生成沉淀的离子方程式为。已知
混合溶液中逐滴加入氨水,首先生成沉淀的离子方程式为。已知 ,
,  。当两种沉淀共存时,
。当两种沉淀共存时,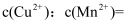 。
。
-
(2) 25℃时,
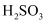 电离常数
电离常数 ,
,  , 则该温度下
, 则该温度下 的水解平衡常数Kh=mol/L(水解平衡常数Kh的书写规则同化学平衡常数)。
的水解平衡常数Kh=mol/L(水解平衡常数Kh的书写规则同化学平衡常数)。
-
(3) 在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中
 , 则溶液显性(填“酸”或“碱”或“中”);用含a的代数式表示
, 则溶液显性(填“酸”或“碱”或“中”);用含a的代数式表示 的电离常数Kb=。
的电离常数Kb=。
-
(4) 25℃时向含有
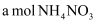 的溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将(填“正向”、“不”或“逆向”)移动,所滴加氨水的浓度为mol/L。(
的溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将(填“正向”、“不”或“逆向”)移动,所滴加氨水的浓度为mol/L。( 的电离平衡常数取
的电离平衡常数取 )
)
-
(5) 向废水中加入硫化物可以依次获得CuS、ZnS纳米粒子。常温下,
 的
的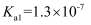 ,
, 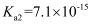 , 溶液中平衡时相关离子浓度的关系如图,下列说法正确的是。
, 溶液中平衡时相关离子浓度的关系如图,下列说法正确的是。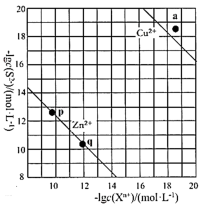
a.
 的数量级为
的数量级为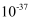
b. a点对应的CuS溶液为不饱和溶液
c.
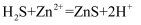 平衡常数很大,反应趋于完全
平衡常数很大,反应趋于完全d. 向p点的溶液中加入少量
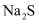 固体,溶液组成由p向q方向移动
固体,溶液组成由p向q方向移动
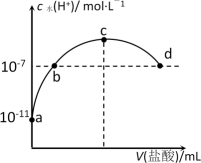
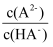 = 104.2
= 104.2
 )>c(OH-)>c(Cl-)>c(H+)
C . c点溶液中c(NH
)>c(OH-)>c(Cl-)>c(H+)
C . c点溶液中c(NH )<c(Cl-)
D . d点代表溶液呈中性
)<c(Cl-)
D . d点代表溶液呈中性
- BarrackObama’s recent visit to the Asian nations clearly se
- 亚砷酸(H3AsO3)可以用于治疗白血病,在溶液中存在多种微粒形态。向1L0.1mol·L-1H3AsO3溶液中逐滴加入
- . Frankly speaking, it’s people’s ________ to keep their pr
- 用科学记数法表示0.000000 080 2.
- 如图是甲和乙的溶解度曲线.下列说法中正确的()A.甲的溶解度大于乙的溶解度 B.乙的溶解度不受温度的影响 C.t1℃时,
- ㈠下列物质属于非电解质的是 ,属于弱电解质的是 ①氨水 ②SO2 ③CI2 ④甲酸 ⑤BaS
- 下列各句中没有语病,句意明确的一句是() A.近日,深圳市卫生局局长江捍平表示,市卫生局将推出八大举措解决市民“看病难、
- 2011年8月1日,山东某市公布了“十一五”期间经济社会发展数据。2010年,该市城镇居民恩格尔系数由2.05年的33.
- 各区域之间要通过区域优势互补,达到共同可持续发展,下列工程最能充分体现的是( ) A.西气东输 B.青藏铁路
- 世界上使用范围最广的语言是 A.汉语 B.英语 C.法语 D.俄语
- 设0≤x<2π,且=sinx-cosx,则( ) A.0≤x≤π
- 下列表示正常情况下,物质穿过细胞膜进入细胞内的四种情况。若在X点加入了呼吸作用抑制剂(影响能量供应),下列曲线中将明显变
- 下列有关反应热的叙述正确的是( ) A.已知2H2(g)+O2(g) 2H2O(g);△H=-483
- The list________ 100 first-class universities at home and ab
- 下列实验操作能达到实验目的的是 选项 实验目的 实验操作 A 探究浓度对化学平衡的影响 向盛有2.5mL 0.005mo
- 为下面文言文语段加上标点。 读书始读未知有疑其次则渐渐有疑中则节节是疑过了这一番疑渐渐释以至融会贯通都无可疑方始是学又云
- 下列氯化物中,既能由单质直接化合制得,又可由金属和盐酸反应制得的是() A.CuCl2 B.FeCl2 C.Fe
- His aunt’s letters him of those beautiful days when they
- 《唐摭言》载:“进士科始于隋大业中,盛于贞观、永徽之际。缙绅虽位极人臣,不由进士者,终不为美,以至岁贡(注:“岁贡”指由
- Though he is in his forties, he is asas a young man. He has
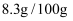 水)
水)