催化剂 知识点题库
 B .
B . 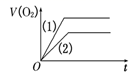 C .
C . 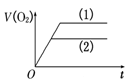 D .
D . 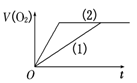
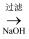 NaAlO2
NaAlO2  Al(OH)3
Al(OH)3 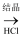 无水AlCl3
无水AlCl3  Al
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
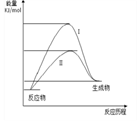
D . 一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
Al
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
表 1 用 MnO2 作催化剂
| 实验序号 | KClO3 质量(g) | MnO2 质量(g) | 反应温度(℃) | 待测数据 |
| 1 | 8.00 | 1.00 | 500 | a |
| 2 | 8.00 | 2.00 | 500 | b |
表 2 用R 作催化剂
| 实验序号 | KClO3 质量(g) | R 质量(g) | 反应温度(℃) | 待测数据 |
| 3 | 8.00 | 1.00 | 500 | c |
| 4 | 8.00 | 2.00 | 500 | d |
下列说法错误的是( )
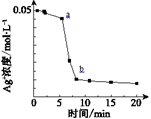
| 操作 | 现象 | Ag+ 浓度变化曲线 | |
| 实验Ⅰ | 向1 mL 0.1 mol/L FeSO4溶液中加入1 mL 0.1 mol/L AgNO3溶液 | 几分钟后,出现大量灰黑色浑浊 | |
| 实验Ⅱ | 先向试管中加入几滴Fe2(SO4)3溶液,然后重复实验Ⅰ的操作 | 现象与实验Ⅰ相同 |
(已知:Ag2SO4为白色微溶物;反应过程中测得温度几乎无变化)
下列说法正确的是( )
-
(1) 如图表示了我国某地区在1959~2019年间,空气中NO,含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的统计数据。结合图中数据,判断下列说法正确的是_______。
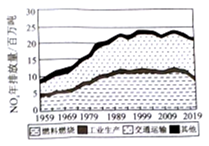 A . 在交通运输中排放的NOx与燃料的不充分燃烧有关 B . 1mol氮氧化物(NOx)形成硝酸型酸雨时转移电子(5-2x)mol C . N2转化为NO的过程不属于氮的固定 D . 随着汽车工业的发展,交通运输的NO,排放量所占比重呈增大趋势
A . 在交通运输中排放的NOx与燃料的不充分燃烧有关 B . 1mol氮氧化物(NOx)形成硝酸型酸雨时转移电子(5-2x)mol C . N2转化为NO的过程不属于氮的固定 D . 随着汽车工业的发展,交通运输的NO,排放量所占比重呈增大趋势 -
(2) 用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1) ΔH=-662 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(1) ΔH=-1248 kJ/mol
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1) ΔH=kJ/mol
-
(3) 工业上可采用碱液来吸收NOx , 有关的化学反应:
①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO2+NaNO3+H2O
现有一定条件下a mol NO2和b mol NO的混合气体恰好被一定体积NaOH溶液完全吸收,则a、b应满足的关系为。
-
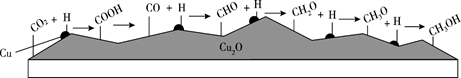
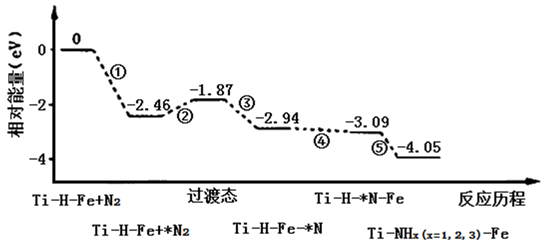
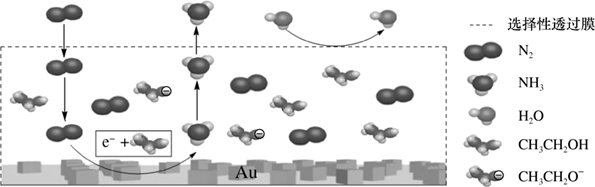
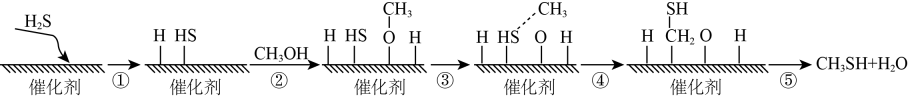
(4) 利用某分子筛作催化剂,可脱除工厂废气中的NO、NO2 , 反应机理如图所示。请写出在此反应机理中脱去NO的离子反应方程式。
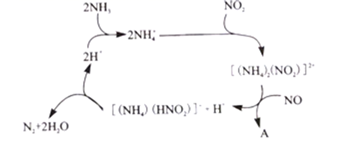
-
(5) 在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2
①NH3与NO2生成N2的反应中,当生成1mol N2时,转移的电子为mol。
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(如图1所示)。反应相同时间NOx的去除率随反应温度的变化曲线如图2所示。下列相关分析正确的是(填序号)
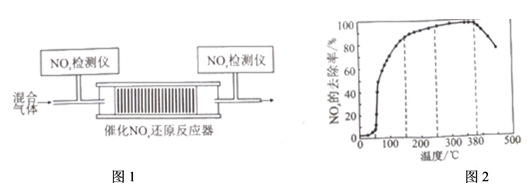
A.在50~150℃范围内随着温度的升高,NOx的去除率迅速上升的原因可能是:催化剂活性随温度升高增大与温度升高共同使NOx去除反应速率迅速增大
B.在150~250℃范围内随着温度的升高,NOx的去除率缓慢上升的原因可能是:温度升高引起的NOx去除反应速率增大
C.反应温度高于380℃时,NOX的去除率迅速下降的原因可能是:催化剂活性下降
D.反应温度高于380℃时,NOx的去除率迅速下降的原因可能是:NH3与O2反应生成了NO
 下列说法正确的是( )
下列说法正确的是( )
-
(1) 实验一:取
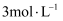 的
的  溶液各10mL分别进行下列实验,实验报告如下表所示。
溶液各10mL分别进行下列实验,实验报告如下表所示。
序号
V(过氧化氢溶液)/mL
V(氯化铁溶液)/mL
二氧化锰质量/g
反应温度/℃
V(水)/mL
结论
1
10
2
0
50
8
2
10
2
0
30
8
3
10
0
1
30
a
①实验1、2研究的是对
 分解速率的影响。
分解速率的影响。②表中数据a的值应该为;实验2、3研究的是对
 分解速率的影响。
分解速率的影响。③如果实验3中30s时共收集到气体的体积为11.2mL(已折算成标准状况下),则用过氧化氢表示的0~30s的平均反应速率为
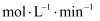 。
。 -
(2) 实验二:已知
 对
对  分解也具有催化作用,为比较
分解也具有催化作用,为比较  和
和  对
对  分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题。
分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题。
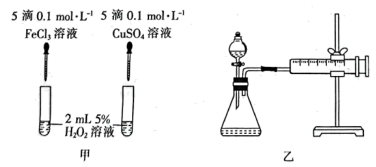
①甲装置:通过观察气泡产生的速率,比较二者的催化效果。但小组某同学提出将硫酸铜改为氯化铜更好,其理由可能是。
②通过乙装置也能比较二者的催化效果。同温同压下,均以生成40mL气体为准,其他可能影响实验的因素均已忽略。则实验中还需要测量的数据是。
-
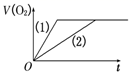
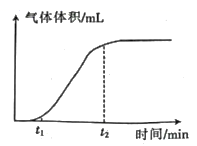
(3) 实验三:取等量的氯酸钾分别加入A、B两试管中,直接加热A试管中的氯酸钾,基本无气体产生;向B试管中再加入少量高锰酸钾,生成气体体积与时间的关系如图。不考虑温度的影响,分析:图中
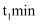 前,B试管中产生气体的速率较慢且量少的原因可能为,
前,B试管中产生气体的速率较慢且量少的原因可能为, 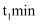 后,B试管中产生气体的速率较快且量多的原因可能为。
后,B试管中产生气体的速率较快且量多的原因可能为。
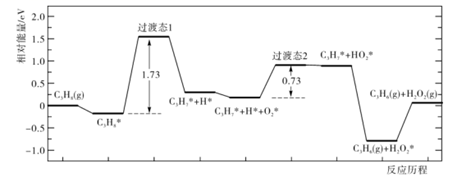
下列说法错误的是( )
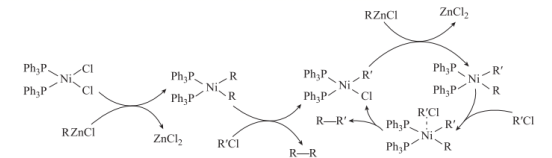
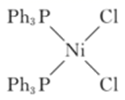 +RZnCl=
+RZnCl= 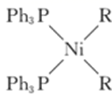 +ZnCl2
+ZnCl2
-
(1) 氮氧化物(以NO为主)直接排放到空气中会形成硝酸型酸雨,反应的化学方程式为。
-
(2) NH3催化还原NO的化学方程式为。
-
(3) 铁基催化剂在260~300℃范围内实现SCR技术的过程如下:
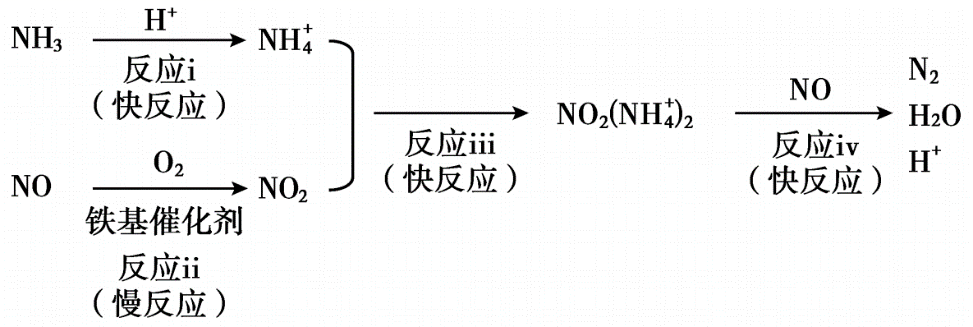
① 反应iv中消耗的NO2 (NH
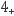 ) 2与NO的物质的量之比为。
) 2与NO的物质的量之比为。② 适当增大催化剂用量可以明显加快脱硝速率,结合上述过程解释原因:。
③ 向反应体系中添加NH4NO3可显著提高NO脱除率。原因如下:
NO
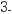 与NO发生反应NO
与NO发生反应NO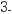 + NO = NO2 + NO
+ NO = NO2 + NO ;
;NO2与NH
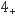 发生反应iii和反应iv转化为N2;
发生反应iii和反应iv转化为N2;NO
 与NH
与NH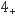 发生反应(填离子方程式)转化为N2。
发生反应(填离子方程式)转化为N2。 -
(4) 相比于铁基催化剂,使用锰基催化剂(活性物质为MnO2)时,烟气中含有的SO2会明显降低NO脱除率。
① 推测SO2与MnO2会发生反应使催化剂失效,其化学方程式是。
② 持续通入含SO2的烟气。不同温度下,每隔1 h测定NO脱除率,结果如下:
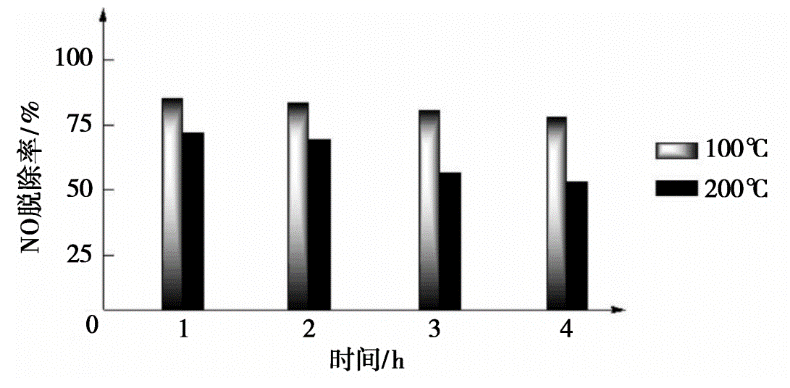
相同时间,200℃时NO脱除率低于100℃,原因是。
- 血浆的主要功能是 A 运输氧、二氧化碳和营养 B 运载血细胞,运输养料和废物 C 运输养料和废
- 从下面两个文明文题中任选一题作文。 文题一: 请将题目“与 结缘”补充完整,写一篇文章。 文题二:
- 若函数f(x)为定义在R上的奇函数,且在(0,+∞)内是增函数,又f(2)=0,则不等式xf(x)<0的解集为() A.
- You need __ more vegetables every day. A. toeat B.e
- 阅读下面的文字,完成后面的题。 近年来,“通俗历史热”不断出现于媒体的报道之中。作为一种关涉史学的文化现象,我们有必要从
- 下图反映的是从西周至新中国建立初期黄 土高原森林覆盖率锐减,植被破坏严重的 现象。造成这一变化的社会历史原因有 ①长期大
- 阅读下列材料并回答以下问题:(10分) 材料一 这场战争,自西方人1514年到中国起,是他们积325年窥探之后的一逞。
- _____ to improvingservices, we will provide customers with
- 史书上称“贞观之风,一时复振”,反映的是哪一治世局面? A.文景之治 B.贞观之治 C.开元盛世 D.光武中兴
- 五代以来君主七朝八姓,赵匡嬴“黄袍加身”建立北宋后的百余年间,末发生类似的现象。一般认为,北宋统治体制的变革是重要原因。
- 化简(a≠0)的结果是() A. 0 B. C. D.
- (2009•齐齐哈尔)如图所示电路,电源电压保持不变,闭合开关S,将滑动变阻器的滑片P向右移动过程中(假设灯丝电阻不变)
- 19世纪90年代,清政府与列强签订的条约与19世纪40~60年代签订的条约相比,最显著的不同点是增加了 ( )
- 它“利用‘冷战’的阴影,把‘遏制’共产主义的计划与制造商、出口商的热情融为一体”。这里的“它”是指
- 下面有关瓦特和改良蒸汽机的图片反映的内容对英国政治发展带桌的影响是 ( ) A.
- (12分)下表是元素周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题) 族 周期 ⅠA ⅡA ⅢA
- 已知中心在原点的双曲线C的一个焦点是,一条渐近线的方程是. (Ⅰ)求双曲线C的方程; (Ⅱ)若以为斜率的直线与双曲线C相
- 2009年3月结束的“两会”上,我国“六大核心经济圈带”的概念逐渐浮现,区域竞争越发激烈。回答下列各题。“六大核心经济圈
- (本题满分13分)已知、分别是椭圆的左、右焦点。 (I)若是第一象限内该椭圆上的一点,,求点P的坐标; (II)设过定点
- 将一个物体用两根等长的绳子OA、OB悬挂在半圆形的架子上,B点固定不动,结点O也不移动,悬点A由位置C向位置D缓慢地移动