催化剂 知识点题库
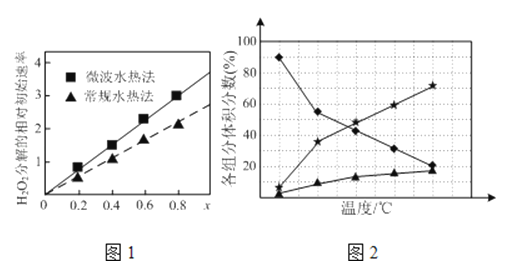
(1)CoxNi(1﹣x)Fe2O4(其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高活性.图1表示两种不同方法制得的催化剂CoxNi(1﹣x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是 。
(2)H2S热分解制氢时[2H2S(g)=2H2(g)+S2(g)△H=+169.8kJ•mol﹣1],常向反应容器中通入一定比例的空气,使部分H2S燃烧,其目的是 。
(3)在纳米钴的催化作用下,肼(N2H4)可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示,则N2H4发生分解反应的化学方程式为;为抑制肼的分解,可采取的合理措施有 (写两种)。
-
(1) 针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大.从影响化学反应速率的因素看,你猜想还可能是的影响。
-
(2) 若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以选择在反应开始前是否加入______(填字母序号)做对比实验.A . 硫酸钾 B . 硫酸锰 C . 氯化锰 D . 水
-
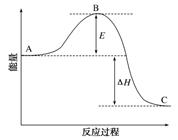
(1) 图中A、C分别表示、,E的大小对该反应的反应热有无影响?(填“有”或“无”)。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,理由是。
-
(2) 图中ΔH=kJ/mol。
-
(3) 如果反应速率v(SO2)为0.05 mol·L-1·min-1 , 则v(O2)= mol·L-1·min-1 , v(SO3)=mol·L-1·min-1。
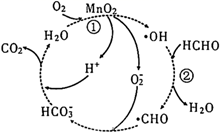
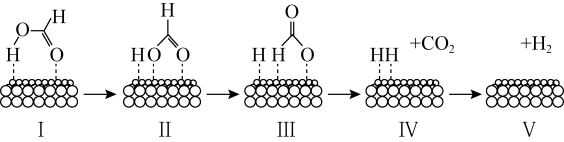
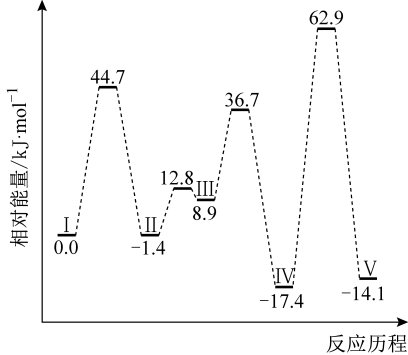
 为中间产物
B .
为中间产物
B .  降低了反应①的活化能
C . 反应②中有碳氧键断裂
D . 该机理的总反应的化学方程式为
降低了反应①的活化能
C . 反应②中有碳氧键断裂
D . 该机理的总反应的化学方程式为 
| 选项 | 实验 | 现象 | 结论 |
| A | 向 | 生成两种沉淀 | |
| B | 向浓度均为 | 先出现浅蓝色沉淀 | |
| C | 向 | 有气体产生,一段时间后, | |
| D | 铜粉加入稀硫酸中,加热;再加入少量硝酸钾固体 | 加热时无明显现象,加入硝酸钾后溶液变蓝 | 硝酸钾起催化作用 |
-
(1) 丙烯(C3H6)是石油化工行业重要的有机原料之一,主要用于生产聚丙烯、二氯丙烷、异丙醇等产品。
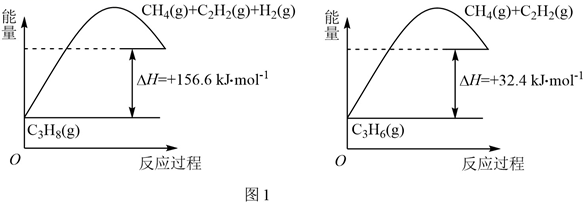 ①丙烷脱氢制备丙烯。由图可得C3H8(g)
①丙烷脱氢制备丙烯。由图可得C3H8(g)  C3H6(g)+H2(g) ∆H=kJ/mol
C3H6(g)+H2(g) ∆H=kJ/mol②目前在丙烷脱氢制丙烯时常通入适量的O2 , 让其同时发生下列反应:2C3H8(g)+O2(g)
 2C3H6(g)+2H2O(g) ∆H=-235kJ/ mol,通入O2的作用是。
2C3H6(g)+2H2O(g) ∆H=-235kJ/ mol,通入O2的作用是。 -
(2) 乙苯催化脱氢制取苯乙烯的反应为:
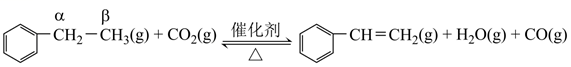 其反应历程如下:
其反应历程如下: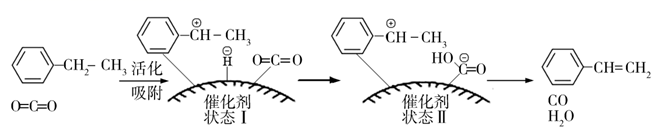 ①关于该反应,下列说法正确的是
①关于该反应,下列说法正确的是A.苯环α位的碳氢键键能小于苯环β位的碳氢键键能
B.催化剂可通过吸附作用,拉近反应物之间的距离,从而增加有效碰撞的概率
C.催化剂的作用是提供反应界面,但不参与化学反应过程。
D.增加催化剂用量可提高反应的平衡转化率
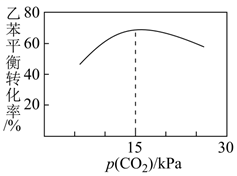
②在相同时间内乙苯的转化率与p(CO2)的关系如图所示,乙苯转化率随着p(CO2)变化的原因是。
-
(3) 工业上可用丙烯加成法制备1,2-二氯丙烷(CH2ClCHClCH3),主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
I.CH2=CHCH3(g)+Cl2(g)
 CH2ClCHClCH3(g)
CH2ClCHClCH3(g)II.CH2=CHCH3(g)+Cl2(g)
 CH2=CHCH2Cl(g)+HCl(g)
CH2=CHCH2Cl(g)+HCl(g)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g)。在催化剂作用下发生反应,容器内气体的压强随时间的变化如表所示。
时间/min
0
60
120
180
240
300
360
压强/kPa
80
74.2
69.2
65.2
61.6
60.0
60.0
①用单位时间内气体分压的变化来表示反应速率,即v=
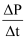 ,则前120min内平均反应速率v(CH2ClCHClCH3)=kPa·min-1。
,则前120min内平均反应速率v(CH2ClCHClCH3)=kPa·min-1。②该温度下,若平衡时HCl的体积分数为12.5%,反应I的平衡常数Kp=kPa-1(Kp为以气体分压表示的平衡常数)。
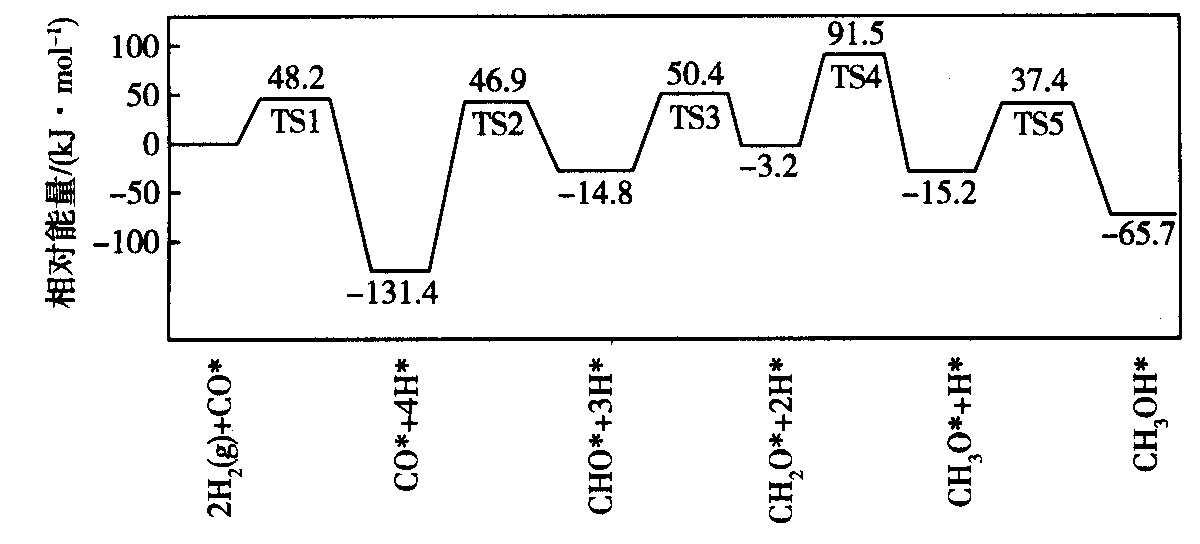
下列说法正确的是( )
 CH3OH(g)+H2O(g),在不同催化剂作用下反应相同时间,CH3OH的浓度随温度变化如图所示。下列说法正确的是( )
CH3OH(g)+H2O(g),在不同催化剂作用下反应相同时间,CH3OH的浓度随温度变化如图所示。下列说法正确的是( )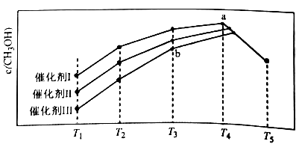
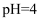 的醋酸溶液稀释10倍,pH<5
B .
的醋酸溶液稀释10倍,pH<5
B .  被
被 氧化为
氧化为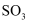 的反应,往往需要使用催化剂
C . 利用
的反应,往往需要使用催化剂
C . 利用 水解制备
水解制备 时,需加入大量水并加热
D . 向
时,需加入大量水并加热
D . 向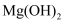 悬浊液中滴加
悬浊液中滴加 溶液,有红褐色沉淀生成
溶液,有红褐色沉淀生成
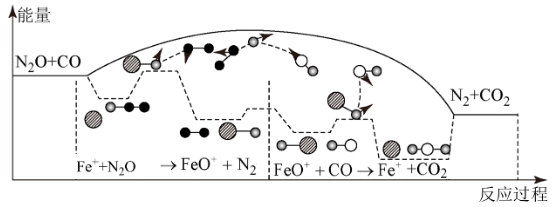
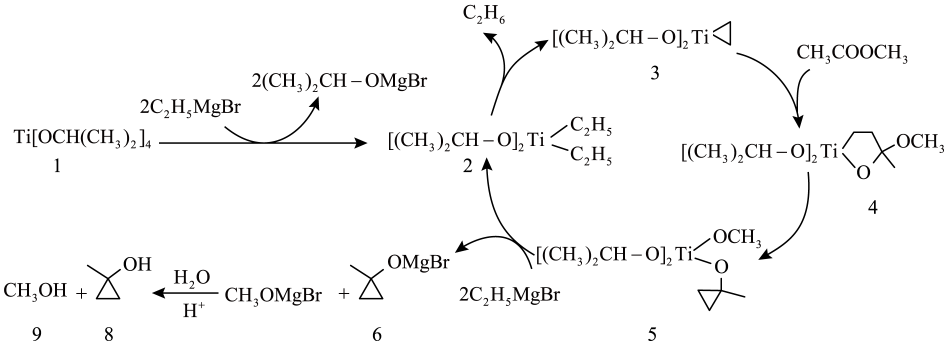
下列叙述错误的是( )
 C2H6+
C2H6+ 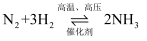 , 在催化剂表面的微观历程及能量变化如图所示,下列说法错误的是( )
, 在催化剂表面的微观历程及能量变化如图所示,下列说法错误的是( )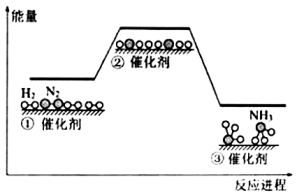
 、
、 化学键的断裂,该过程吸收能量
B . ①→②→③的过程中有非极性键的断裂和形成
C . 合成氨反应属于氮的固定,是放热反应
D . 合成氨过程中催化剂参与了反应
化学键的断裂,该过程吸收能量
B . ①→②→③的过程中有非极性键的断裂和形成
C . 合成氨反应属于氮的固定,是放热反应
D . 合成氨过程中催化剂参与了反应
 、NO
、NO 、NO
、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为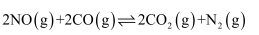 △H=-746.5kJ·mol-1];也可将水体中的NO
△H=-746.5kJ·mol-1];也可将水体中的NO 、NO
、NO 转化为N2。对于反应
转化为N2。对于反应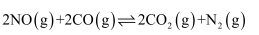 , 下列说法正确的是( )
, 下列说法正确的是( )
 C . 使用高效的催化剂可以降低反应的焓变
D . 其它条件不变,增大
C . 使用高效的催化剂可以降低反应的焓变
D . 其它条件不变,增大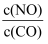 的值,NO的转化率下降
的值,NO的转化率下降
 SO3(1)+NO(g),该反应的 ΔS<0
B . 2CO(g)=2C(s) + O2(g) ΔH>0, 高温下可以自发
C . C(s,金刚石)=C(s,石墨) ΔH= -1.9 kJ·mol-1 , 金刚石比石墨更稳定
D . 选择高效催化剂可以降低反应的焓变,提高化学反应速率
SO3(1)+NO(g),该反应的 ΔS<0
B . 2CO(g)=2C(s) + O2(g) ΔH>0, 高温下可以自发
C . C(s,金刚石)=C(s,石墨) ΔH= -1.9 kJ·mol-1 , 金刚石比石墨更稳定
D . 选择高效催化剂可以降低反应的焓变,提高化学反应速率
- 我们吃的玉米是由下列哪一项发育来的( ) A. 子房壁 B. 花托和子房壁 C. 花托和胚珠
- 2.下列句子中都含通假字的一组是 ①距关,毋内诸侯 ②沛公不胜杯杓 ③愿伯具言臣之不敢倍德 ④范增
- 实验室常用的电磁式打点计时器用的是低压______(填“直流”、“交流”)电源.某次实验连续打了一系列点的纸带如下图,由
- Have one of those days or weeks when everything seems to ann
- 某元素M2+核外电子数为10,该元素是下列原子中的() A. Cr B.
- 切取一段葡萄的枝条,插入湿润的沙土中,不久,枝条下端萌发出新的根,这种繁殖方法叫( ) A.扦插
- Children under six are not ___________to school except those
- 下列各组烃的混合物,只要总质量一定,无论按什么比例混合,完全燃烧后生成的CO2和H2O都是恒量的是( )A.
- ,山色有无中。(王维《汉江临眺》)
- 下图表示从血液中制备核糖体的大致过程,对该过程的叙述中,不合理的是 ① ②
- 16的平方根是 .
- 请将下列植物名称与所属类群用直线连接起来。A.葫芦藓 ①裸子植物 B.水杉
- 已知Si+2NaOH+H2O==Na2SiO3+2H2↑ 2Al+2NaOH+2H2O=2NaAlO2+ 3H2↑,硅
- 函数f(x)=+lg(x+2)的定义域为() A.(﹣2,1) B.(﹣2,1] C.[﹣2,1)
- 如图所示,A、B是一条电场线上的两点,若在A点释放一初速为零的电子,电子仅受电场力作用,沿电场线从A运动到B.则(
- 下列句中加点的成语使用正确的一项是 A耸人听闻的药家鑫故意杀人案引起社会各界的广泛关注,它警示我们要切实加强对青少年的
- p{font-size:10.5pt;line-height:150%;margin:0;padding:0;}td{f
- Bryan、Olga、Scott、Anna、和David正在进行一项“企业家成功秘诀调查”。他们将采访几位企业家,第61
- 史学家陈旭麓指出,19世纪40年代,60年代和90年代是中国社会从古代到近代变革过程中前后相接的三个历史环节。贯穿这三个
- 如图为人体体液物质交换示意图,其中正确的叙述是() ①A、B、C依次为血浆、细胞内液、组织液 ②乙酰胆碱可以存在于B中
 溶液中通入足量的
溶液中通入足量的 
 的氧化性强于S
的氧化性强于S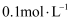 的
的 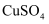 和
和 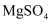 混合溶液中滴加少量
混合溶液中滴加少量  溶液
溶液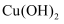 的溶度积比
的溶度积比 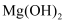 的小
的小 的
的  溶液
溶液 能催化
能催化 


