金属及其化合物 知识点题库
下列关于锂的说法正确的是( )
A . 碱金属中Li的还原性最强
B . 碱金属阳离子,氧化性最强的是Li+
C . 和Li同一主族的都是金属元素
D . Li在空气中加热生成过氧化锂
下列关于碳酸钠和碳酸氢钠的叙述,正确的是( )
A . 常温时,在水中的溶解性:碳酸钠>碳酸氢钠
B . 热稳定性:碳酸钠<碳酸氢钠
C . 质量相同时,分别与同体积同浓度盐酸反应的快慢:碳酸钠>碳酸氢钠
D . 物质的量相同时,分别与足量的盐酸反应,生成CO2的质量:碳酸钠<碳酸氢钠
已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如下图①所示:
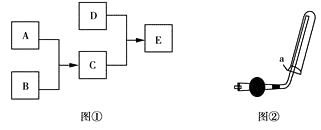
-
(1) 将气体B点燃,把导管伸入盛满气体A的集气瓶,反应过程中的实验现象有(填序号)
①放热 ②黄绿色褪去 ③瓶口有白雾 ④瓶口有白烟
⑤安静燃烧,发出黄色火焰 ⑥安静燃烧,发出苍白色火焰
-
(2) 实验室制D的化学方程式为。
-
(3) 实验室可用如上图②所示装置收集D,下列叙述正确的是(填序号)。
①D气体不能用排水法收集
②干燥管里盛有碱石灰
③图②中的a为棉花团,其作用是防止氨气逸出
-
(4) 气体D催化氧化的化学方程式为。
-
(5) 物质E的化学式是;E在下列物质分类中所属的物质种类是(填序号)。
①电解质;②化合物;③混合物;④纯净物;⑤非电解质;⑥盐
已知A、B、C、D 为气体,其中A 为黄绿色气体。E、F 为固体且均含三种元素,G 是氯化钙,它们之间的转换关系如下图所示:
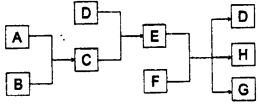
-
(1) D 的化学式是。
-
(2) H 的电子式为。
-
(3) A 和B 反应生成C 的化学方程式是。
-
(4) 将A 通入F 的澄清溶液中所发生反应的离子方程式是。
称取4.00 g氧化铜和氧化铁固体混合物,加入50.0 mL 2.00 mol·Lˉ1的硫酸充分溶解,往所得溶液中加入5.60 g铁粉,充分反应后,得固体的质量为3.04 g。
请计算:
-
(1) 加入铁粉充分反应后,溶液中溶质的物质的量。
-
(2) 固体混合物中氧化铜的质量。
短周期元素W、X、Y、Z的原子序数依次增大,这些元素组成的单质和化合物转化关系如下图所示。其中C是淡黄色固体,B和E的水溶液均具有漂白性。下列说法错误的是( )
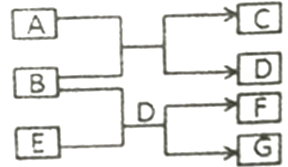
A . 简单离子半径:Y>Z>X
B . 沸点:D<A
C . 气态氢化物稳定性:Z>Y
D . 0.1mol·L-1A溶液中:c(H+)>c(HY-)>c(Y2-)
把少量的金属钠放入CuSO4溶液中,现象,化学方程式是。
某元素X的气态氢化物的分子式为H2X,该元素的最高价氧化物对应的水化物的分子式可能是( )
A . H2XO3
B . H2XO4
C . H4XO4
D . H3XO4
将一定质量的镁铝合金投入400 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
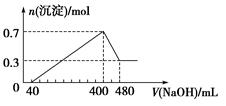
计算:
-
(1) 合金中Mg的质量为g;
-
(2) 硫酸的物质的量浓度为 mol·L−1;
-
(3) NaOH溶液的物质的量浓度为 mol·L−1;
-
(4) 生成H2在标准状况下的体积为L。
下列各组中的两种物质作用,反应条件(温度或者反应物浓度、用量等)改变,不会引起产物改变的是( )
A . Na和O2
B . N2和O2
C . Cu和HNO3
D . Na2CO3和HCl
在溶液中加入过量Na2O2后仍能大量共存的是( )
A . NH4+、Ba2+、Cl-、NO3-
B . K+、CO32-、AlO2-、SO42-
C . Fe2+、Mg2+、SCN-、Cl-
D . Na+、HCO3-、SO32-、I-
向四支试管中分别加入少量不同的无色溶液进行如下操作,则操作、现象、结论均正确的是( )
| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 加CCl4 , 振荡、静置 | 上层溶液显紫色 | 原溶液中有I2 |
| C | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
| D | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
A . A
B . B
C . C
D . D
下列图示中,A、B是金属单质,E、K是非金属单质,其它为化合物,F、G、H、I、J 焰色反应均为黄色,在这些物质中只有C、K是气体,其中K是黄绿色气体,反应⑧⑨是工业由H制I的重要反应。
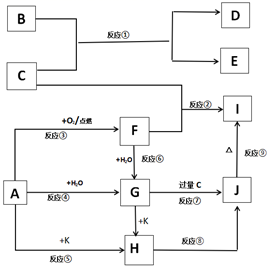
填写下列空白:
-
(1) 写出化学式:B,F。
-
(2) 写出反应①的化学反应方程式:。
-
(3) 写出反应⑦离子反应方程式:。
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):
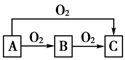
-
(1) 若A是一种金属,C是淡黄色固体,则B的化学式为,A→C反应的化学方程式为。
-
(2) C可用于呼吸面具或潜水艇中氧气的来源,写出所发生的化学方程式从氧化剂和还原剂的角度分析,在这个反应中C的作用是 。
下列有关说法正确的是( )
A . 纯银器表面在空气中因电化学腐蚀渐渐变暗
B . 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
C . 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
D . 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
下列关于金属钠的叙述中,说法正确的是( )
A . 金属钠可以保存在少量水中
B . 钠长时间暴露在空气中,最终产物是Na2CO3
C . 钠是银白色金属,硬度大,熔点高
D . Na与CuSO4溶液反应可以置换出Cu单质
下列有关物质性质与用途具有对应关系的是( )
A .  具有强氧化性,可用于自来水的杀菌消毒
B .
具有强氧化性,可用于自来水的杀菌消毒
B .  熔点高,可用于电解冶炼铝的原料
C .
熔点高,可用于电解冶炼铝的原料
C .  硬度大,可用于制造光导纤维
D .
硬度大,可用于制造光导纤维
D .  易溶于水,可用于作制冷剂
易溶于水,可用于作制冷剂
 具有强氧化性,可用于自来水的杀菌消毒
B .
具有强氧化性,可用于自来水的杀菌消毒
B .  熔点高,可用于电解冶炼铝的原料
C .
熔点高,可用于电解冶炼铝的原料
C .  硬度大,可用于制造光导纤维
D .
硬度大,可用于制造光导纤维
D .  易溶于水,可用于作制冷剂
易溶于水,可用于作制冷剂
碳酸钠和碳酸氢钠各1mol,分别强热后,其产物与足量盐酸反应的结果是( )
A . 放出CO2的量前者为后者的二分之一
B . 放出的CO2的量前者为后者的二倍
C . 消耗盐酸一样多
D . 消耗盐酸后者比前者多
X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是(含硫)化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液能使酚酞溶液变红色。
请回答下列问题:
-
(1) X、Y两种气体按物质的量之比1∶1在水溶液中能发生反应,离子方程式为。
-
(2) 科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式);该反应是氧化还原反应,则其中的氧化剂是(填化学式)。
-
(3) 写出Z与水的反应的化学方程式,此反应中氧化剂与还原剂的物质的量之比。
化学与生活息息相关,下列说法错误的是( )
A . 2021年中国高铁总里程达3.79万公里,举世闻名,其车体为铝合金锻造而成
B . 华为自主研发的“麒麟”芯片与太阳能电池感光板所用材料均为晶体硅
C . 鼓励光伏、风电、水电、核电等新能源的发展,争取在2030年前实现碳达峰
D . 日本福岛核电站事故核废水中含有氚( )和
)和 等放射性同位素,
等放射性同位素, 属于化学变化
属于化学变化
 )和
)和 等放射性同位素,
等放射性同位素, 属于化学变化
属于化学变化
最近更新
- 题目: 我们奔跑着 要求:(1)写一篇600字左右的文章。 (2)不得透露个人相关信息。
- 阅读下面散文,完成18~21题。(18分)沙之聚张抗抗去敦煌不全是为了莫高窟。我明白,却不能说。其实心里惦念了很久的,是
- “它排除了丞相个人专断,相权过大威胁皇权而出现的政治危机,而且增强了决策施政的程序性和合理性,提高了行政效率。”材料中的
- 临床使用抗生素前,有时需要做细菌耐药实验.实验时,首先要从病人身上获取少量样本,然后按照一定的实验步骤操作,以确定某致病
- 水是生命之源,下列有关水的说法错误的是 ( ) A.通过过滤的方法可以除去水中所有的杂质 B.生活中可用煮
- 若a>0,b>0,则不等式-b<<a等价于 A.<x<0或0<x<
- 真正被打败的人,不是行动而是心;行动被打败了,可以重新站起来;而心被打败了,那就永远倒下了。这给我们的哲学启示是 A.实
- 下列各组离子一定能大量共存的是 A.使石蕊试液变蓝色的溶液:Na+、K+、、 B.在强碱溶液中:Na+、ClO-、AlO
- 下列图示的实验中,正确的是( ) A. B. C. D.
- 若tan =-2,则 =A. B. C. D.
- ( )30. It was not until the 18th century that man realized
- 在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(
- Last spring, Michellefell in love with kite-boarding, an adv
- 对于四面体ABCD ,给出下列四个命题:①若AB=AC,BD=CD,则BC⊥AD;②若AB=CD,AC=BD,则BC⊥A
- 已知:如图,在四边形ABCD中,E为AB上一点,△ADE和△BCE都是等边三 角形,AB、BC、CD、DA的中点分别为P
- 宇宙中存在着大量的射线,其中有许多都是高速运动的带电粒子,如电子、质子、氦原子核等。我们生活的地球表面上每时每刻都会接受
- 设U={1,2,3,4,5}, A={1,2,3}, B={2,4},则A∪ =
- 尼泊金甲酯可在化妆品中作防腐剂。结构简式为下列说法中正确的是 A.在一定条件下,1 mol该物质最多能和2 m
- D......
- 根据下图中信息回答下列问题。 (1)下图中三种碱溶于水时解离出的阴离子全部是________。(2)由上图可推测出,这三



