金属及其化合物 知识点题库
-
(1) 实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是;
-
(2) 实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——;
-
(3) 实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是_________A . 火焰温度太低不能使铝燃烧 B . 铝在空气中能很快形成氧化膜 C . 氧化铝的熔点比铝的熔点高 D . 用砂纸打磨不能除去表面的氧化膜
-
(4) 实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验生成的气体,向反应后的溶液中加入酚酞试液,溶液中可以看到
-
(5) 实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是,该反应每消耗1mol铁,转移电子的物质的量为。
-
(6) 实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜色变化的原因是(用化学方程式表示):。
-
(1) 关于铝热反应有以下两种认识,其中正确的是(填字母号)。
a .该反应需在高温下发生,所以该反应吸热
b.因为铝的还原性较强,所以铝能将相对不活泼的金属从其化合物中置换出来
-
(2) 铝和氧化铁反应的化学方程式是。
-
(3) 铝和氧化铁反应所得固体成分的初步确定。
实验序号
操作及现象
i
取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色
ii
向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色
①由上述实验可知:溶液中Fe元素的存在形式有。
②i中产生H2的原因是样品中除含Fe外,可能有未反应的Al,为检验样品中是否含Al单质,可选用的试剂是。
③ii中生成O2的化学方程式是。进一步的实验表明,上述固体样品中Fe元素的存在形式有Fe、Fe2O3、Fe3O4
-
(1) 苏打水溶液中滴加酚酞溶液后,溶液呈(填“无”或“红”)色;
-
(2) 检验某补铁剂中的Fe2+是否被氧化成Fe3+ , 可向该补铁剂溶液中加入KSCN溶液,若溶液(填“变红色“或“产生红褐色沉淀”),则Fe2+已被氧化成Fe3+;
-
(3) 铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以整装浓硫酸,是由于铝在冷的浓硫酸中(填“不反应“或“钝化”),
-
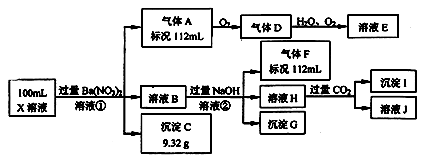
(1) 仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是。为证明该阴离子是否存在,需要加入试剂(写化学式)。
-
(2) 用离子方程表达下列反应:
①中生成气体A:。
②中生成溶液H:。
-
(3) 若②中所用氢氧化钠浓度为2mol/L,当加入l0ml时开始产生沉淀,55ml时沉淀的量达到最大值0.03mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025mol且保持不变,则原溶液中c(Fe2+)为mol/L、c(Cl﹣)为mol/L。(若离子不存在,请填0mol/L)
 CaSO3
CaSO3  CaSO4
B . Fe
CaSO4
B . Fe  Fe2O3
Fe2O3  FeCl3
C . HCl(aq)
FeCl3
C . HCl(aq)  Cl2
Cl2  Ca(ClO)2
D . Cu2(OH)2CO3
Ca(ClO)2
D . Cu2(OH)2CO3  CuO
CuO  CuCl2(aq)
CuCl2(aq)
①A不溶于水和盐酸;
②B不溶于水,但洛于盐酸,并放出无色无刺敬性气味的气体E;
③C的水溶液呈破性,与硫酸反应生成A;
④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
-
(1) 推断A、D的化学式:A、, D、。
-
(2) 写出下列反应的离子方程式。
B与盐酸反应:。
C与硫酸反应:。
E(少量)与澄清石灰水反应:。
-
(3) 用单线桥法表示反应Cu+2H2SO4(浓)
 CuSO4+2H2O+SO2↑电子转移的方向和数目(在化学方程式上标出)。
CuSO4+2H2O+SO2↑电子转移的方向和数目(在化学方程式上标出)。
 、CO
、CO  、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
-
(1) 推断A、C的化学式:A ;C ;
-
(2) 写出下列反应的离子方程式。
①D与氯化钙反应:。
②B与盐酸反应: 。
③C与稀硫酸反应:。
-
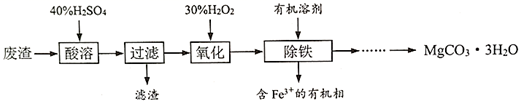
(1) “酸溶”过程中加入的H2SO4不宜过量太多,原因是。
-
(2) 加入H2O2 “氧化”时反应的离子方程式为。反应温度一般控制在40℃~50℃,目的是。
-
(3) 用下图所示的实验装置以除去氧化后溶液中的Fe3+。
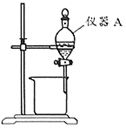
①实验装置图中仪器A的名称为。
②常用来检验水溶液中的Fe3+是否除净。
-
(4) 请补充完整由(3)中得到的水溶液来制备MgCO3·3H2O的实验方案:边搅拌边,在50℃下干燥,得到MgCO3·3H2O。
[可供选用的试剂:氨水、Na2CO3溶液、蒸馏水;已知该溶液中pH=5.0时Al(OH)3沉淀完全;pH=8.5时Mg(OH)2开始沉淀。]
| 选项 | 实验操作和现象 | 结论 |
| A | 将湿润的红色石蕊试纸置于集气瓶口,试纸变蓝 | 集气瓶内的气体为NH3 |
| B | 常温时向盛有浓硝酸的两支试管中分别投入铜片与铁片后,铜片逐渐溶解而铁片不溶解 | 金属性:Cu>Fe |
| C | 向鸡蛋清溶液中加入少量CuSO4溶液,出现浑浊,分离沉淀后加足量水,沉淀不溶解 | 蛋白质发生了盐析 |
| D | 向某乙醇中加入一小块金属钠,有气泡生成 | 该乙醇中一定含有水 |
| 实验操作及现象 | 实验结论 | |
| A | 将一块表面打磨过的铝箔在酒精灯上加热至熔化,液态铝不会滴落 | Al2O3的熔点高于Al |
| B | 向无色溶液中滴入BaCl2溶液,出现白色沉淀 | 该溶液一定含SO |
| C | 某气体能使湿润的淀粉KI试纸变蓝 | 该气体一定是Cl2 |
| D | 蘸有浓氨水的玻璃棒放在某溶液上方,产生白烟 | 该溶液一定为浓盐酸 |
 B . 乙图:可以检验溶液中的
B . 乙图:可以检验溶液中的 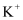 C . 丙图:可以验证碳酸钠和碳酸氢钠的稳定性
D . 丁图:可以制取碳酸氢钠
C . 丙图:可以验证碳酸钠和碳酸氢钠的稳定性
D . 丁图:可以制取碳酸氢钠
- 下列反应中,属于吸热反应的是 A.活泼金属跟酸反应 B.制造水煤气
- 合成氨的反应是:N2(g)+3H2(g) 2NH3(g) △H<0。使反应进行程度增大的方法是A.升高温度 B
- 2014年9月16日省运会在我市开幕,为响应市委“办好省运会,当好东道主”的号召,园艺工人在美化、绿化济宁城时。为提高苗
- 大气中二氧化碳含量一般保持不变,主要原因是自然界中有消耗二氧化碳的途径,也有产生二氧化碳的途径。如自然界中含碳燃料的燃烧
- 决定元素化学性质的是 A、核外电子数 B、核电荷数 C、最外层电子数 D、中子数
- 某化学兴趣小组选用如图所示装置,进行CO2制取和性质实验,请你根据所学知识,依图回答下列问题:(1)仪器①的名称为
- .(重庆卷 21).You park here! It’s an emergency exit. A. wo
- 先化简,再求值:,其中a=﹣1.
- 已知甲、乙、丙三种食物的维生素A、B含量及成本如下表: 甲 乙 丙 维生素A(单位/kg) 60 70 40 维生素B(
- 已知数列的各项为正数,且则等于( ) A. B. C. D.
- 人体在短暂禁食(如一天左右)和安静条件下,三种物质含量变化如图。图中描绘的血糖和血游离脂肪酸含量的变化,不正确的是 (
- 化学学习让我们有了很多收获,下列归纳总结完全正确的一组是()选项 实验目的 方案 A 鉴别稀盐酸和稀硫酸 取样,滴加紫色
- 睾丸和卵巢分别是男女最主要的生殖器官,是因为 ( ) A.他们能产生生殖细胞 B.它们能产生
- (四)[古典文学] 阅读下面甲、乙两段文言文,回答文后问题。(14分)【甲】 至于负者歌于途,行者休于树,前者呼,后者应
- 已知:关于x的不等式组无解,则m的取值范围是( )A.m<7 B.m≥7
- 实验桌上放着晶体二极管、电阻、电容器各一只,性能均正常,外形十分相似.现将多用电表转换开关拨到×挡,分别测它们的正负电阻
- 2.下列各句中,没有错别字的一项是 ( ) A.
- (2009浙江文综卷11)图5中,当a、c.值相差 时,该地的纬度值是 A.N B.N C.N
- “推动哲学家前进的,绝不像他们所想象的那样,只是纯粹思想的力量。恰恰相反,真正推动他们前进的,主要是自然科学和工业的强大
- 下列说法错误的是( ) A.若命题p:∃x∈R,x2﹣x+1=0,则¬p:∀x∈R,x2﹣x+1≠0 B.“sinθ=”



