金属及其化合物 知识点题库
下列说法不正确的是( )
A . 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移电子总数为0.1mol
B . 明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,所以明矾可用于水的净化
C . 向Na2CO3溶液中滴加盐酸溶液,一定有CO2气体生成
D . Na2O2常用于潜水艇或呼吸面具的供氧剂
以下物质间的每步转化通过一步反应能实现的是( )
A . Al→Al2O3→Al(OH)3→Na[Al(OH)4]
B . N2→NO→NO2→HNO3
C . Si→SiO2→H2SiO3→Na2SiO3
D . S→SO3→H2SO4→MgSO4
有关下列化合物的说法正确的是( )
A . SO2可大量用于漂白食品
B . 干冰、AgI均可用于人工降雨
C . 四氧化三铁常用作红色油漆和涂料
D . 小苏打的主要成分是Na2CO3
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
-
(1) 人体正常的血红蛋白含有Fe2+ , 若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述错误的是________(填字母编号).A . 亚硝酸盐被还原 B . 维生素C是还原剂 C . 维生素C将Fe3+还原为Fe2+ D . 亚硝酸盐是还原剂
-
(2) 下列方法中,不能用来区分NaNO2和NaCl的是__________(填字母编号).A . 测定这两种溶液的pH B . 分别在两种溶液中滴加甲基橙 C . 在酸性条件下加入KI﹣淀粉溶液来区别 D . 用AgNO3和HNO3两种试剂来区别
-
(3) 单质铁与过量稀硫酸反应可以制取FeSO4 . 若用反应所得的酸性溶液,将Fe2+转化为Fe3+ , 要求不引入新的杂质,可选用的最佳试剂是___________(填字母编号).A . Cl2 B . Fe C . H2O2 D . HNO3
-
(4) 某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出该反应的离子方程式:。
向含1mol HCl和1mol MgSO4的混合溶液中加入1mol/L Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图是( )
A . 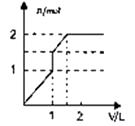 B .
B . 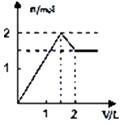 C .
C . 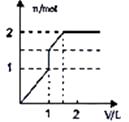 D .
D . 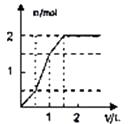
 B .
B .  C .
C .  D .
D . 
将露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的 CO2(标准状况)与加入的盐酸的体积有如图所示的关系(不考虑 CO2 在水中的溶解)。下列说法不正确的是( )
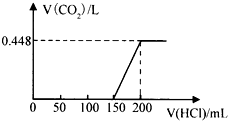
A . 滴加盐酸 0→150mL 段发生的反应依次为 OH-+H+=H2O CO32-+H+=HCO3-
B . 所用盐酸的物质的量浓度为 0.4 mol•L﹣1
C . CO2体积不再改变时,溶液中的溶质为 NaCl
D . 该样品中 NaOH 与 Na2CO3 物质的量之比为1:2
以下物质之间的每步转化中,都能通过一步实现的是( )
① Fe→FeCl2→Fe(OH)2→Fe(OH)3
② Na→Na2O→Na2CO3→NaHCO3→NaOH
③ Mg→MgCl2→Mg(OH)2
④ Al→Al2O3→Al(OH)3
⑤ Al→NaAlO2→Na2CO3
A . ②③④
B . ①③④⑤
C . ①②③⑤
D . ①②③④⑤
下列化学方程式中,不能正确表达反应颜色变化的是( )
A . 向CuSO4溶液中加入足量Zn粉,溶液蓝色消失Zn+CuSO4=Cu+ZnSO4
B . 澄清的石灰水久置后出现白色固体Ca(OH)2+CO2=CaCO3↓+H2O
C . Na2O2在空气中放置后由淡黄色变为白色2Na2O2=2Na2O+O2↑
D . 向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3=2Fe(OH)3+3MgCl2
已知电离常数:H2CO3>HCN>HCO3- , 氧化性:Cl2>Br2>Fe3+>I2。下列有关叙述中正确的是( )
A . 向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-
B . 向NaCN溶液中通入少量CO2的离子方程式:CN-+CO2+H2O=HCN+HCO3-
C . 向溴水中加入足量氯化亚铁溶液,混合溶液变为无色
D . 0.1mol/L HCN溶液,加水稀释,c(H+)/(HCN)将变小
将m g镁铝合金投入到500 ml 2 mol/L的盐酸中,固体完全溶解,收集到气体5.6L (标准状况下)。向反应所得溶液中加入4mol/L的氢氧化钠溶液,沉淀达到最大值为13.60 g,则m的值为( )
A . 11.48
B . 9.35
C . 8.50
D . 5.10
-
(1) I.治疗胃酸过多的药物达喜(其式量不超过 700)由五种短周期元素组成,按如下流程进行实验以确定其组成。
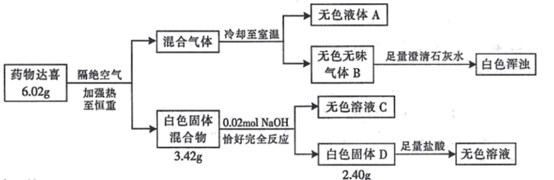
请回答:
达喜的化学式是。
-
(2) 达喜与胃酸(含稀盐酸)反应的化学方程式是。
-
(3) 气体 B 与环氧丙烷(
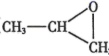 )可制得一种可降解高聚物,该反应的化学方程式是(有机物用结构简式表示)。
)可制得一种可降解高聚物,该反应的化学方程式是(有机物用结构简式表示)。
-
(4) II.将 NaClO3 溶液逐滴加入到碘单质和过量盐酸的混合液中可制备液态 ICl,实验装置如下图:
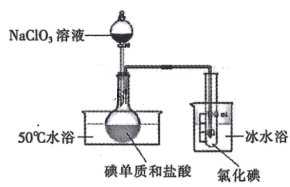
请回答:
圆底烧瓶中发生的化学反应是( 用化学方程式表示)。
-
(5) 若加入的 NaClO3 溶液已足量,请设计实验方案证明该反应已完全:。
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3 , 再用副产品FeCl3溶液吸收有毒的H2S
I.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
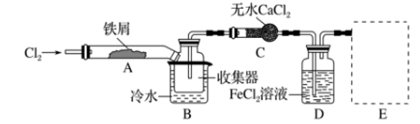
①检验装置的气密性
②通入干燥的Cl2 , 赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成
④……
⑤体系冷却后,停止通入Cl2 , 并用干燥的赶尽Cl2 , 将收集器密封
请回答下列问题:
-
(1) 写出实验室制取氯气的离子方程式。
装置A中反应的化学方程式为。
-
(2) 第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是。
-
(3) 操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)
-
(4) 装置B中冷水浴的作用为;装置C的名称为;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂
-
(5) FeCl3与H2S反应离子方程式为
-
(6) 综合分析实验II的两个反应,可知实验有两个显著优点:
①H2S的原子利用率为100%
②。
在某些月饼的包装盒内有个小纸袋,将小纸袋打开,可看到灰黑色粉末,其中有些已变成棕褐色。将灰黑色粉末溶于盐酸,溶液呈浅绿色,滴入几滴氯水,溶液变棕黄色。以下结论错误的是( )
A . 该灰黑色粉末用作抗氧化剂
B . 小纸袋中的原装粉末是Fe2O3
C . 小纸袋中可能装有活性铁粉
D . 该灰黑色粉末不可食用
某同学用含结晶水的正盐X(四种短周期元素组成的纯净物)进行了如下实验:
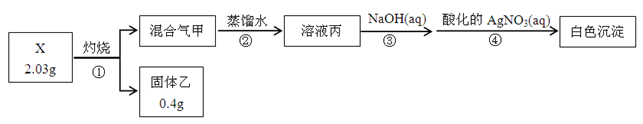
实验中观测到:混合气甲呈无色并被蒸馏水全部吸收;固体乙为纯净物;在步骤③中,取 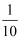 溶液丙,恰好中和需消耗0.00200molNaOH;另取一定量的溶液丙,加入少量K2FeO4固体,产生黄绿色气体。
溶液丙,恰好中和需消耗0.00200molNaOH;另取一定量的溶液丙,加入少量K2FeO4固体,产生黄绿色气体。
请回答:
-
(1) X的化学式是,步骤①的化学方程式是。
-
(2) 溶液丙与K2FeO4固体反应的化学方程式是。
人类的生产和生活中离不开金属材料。通常所说的“金属材料”,既包括纯金属,也包括各种合金。下列材料不属于合金的是( )
A . 青铜
B . 硬铝
C . 生铁
D . 磁铁矿
电视剧《三十而已》中多次提及的“蓝色烟花”,是烟花设计师心中的最高梦想。制作“蓝色烟花”的盐不常见,且稳定性差,该盐可能是( )
A . NaCl
B . KOH
C . Na2CO3
D . CuCl
化合物AgMnAs2在磁记录材料领域有着广泛的应用前景,回答下列问题:
-
(1) Ag的焰色反应与铁相似,接近无色,下列有关焰色反应原理的分析正确的是(填字母)。
a.电子从基态跃迁到较高的激发态
b.电子从较高的激发态跃迁回基态
c.焰色反应的光谱属于吸收光谱
d.焰色反应的光谱属于发射光谱
-
(2) 基态Mn原子中核外电子占据的最高能层符号。其核外未成对电子数为个。
-
(3) Mn(NO3)2中阴离子的空间构型是,Mn、N、O中第一电离能最大的元素是(填元素符号)。
-
(4) NH3、PH3、AsH3的沸点由高到低的顺序为(填化学式,下同),键角由大到小的顺序为。
-
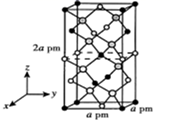
(5) 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系 AgMnAs2的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标
原子
x
y
z
Ag
0
0
0
Mn
0
0
0.5
As
0.25
0.25
0.125
找出距离 Ag(0,0,0)最近的Mn(用分数坐标表示)。AgMnAs2晶体中与单个Mn键合的As有个。
将一粒绿豆大小的金属钠,投入硫酸铜溶液的烧杯中,下列实验现象错误的是( )
A . 溶液中有蓝色沉淀生成
B . 反应放出热量,发出嘶嘶声
C . 钠熔成一个闪亮的小球,并在液面上向各方向迅速游动最后消失
D . 有红色物质生成
书写有关化学方程式
-
(1) 过氧化钠与二氧化碳反应的化学方程式。
-
(2) 制取漂白粉的化学方程式。
-
(3) 氯气与氢氧化钠溶液反应的化学方程式。
-
(4) 漂白粉长时间暴露在空气中就会失去效用,失效原因是(写出2个化学方程式);。
-
(5) 将钠投入到CuSO4溶液中,写出化学方程式。
以废旧锂离子电池正极材料(主要成分为镍钴锰酸锂,还有少量铝箔和含铁化合物)为原料,回收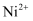 、
、 、
、 的过程可表示为:
的过程可表示为:
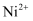 、
、 、
、 的过程可表示为:
的过程可表示为: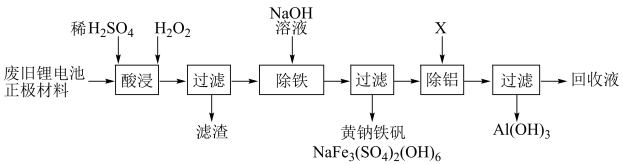
-
(1) “酸浸”时,三价镍、三价钴、四价锰转化为
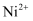 、
、 、
、 进入溶液。该过程中
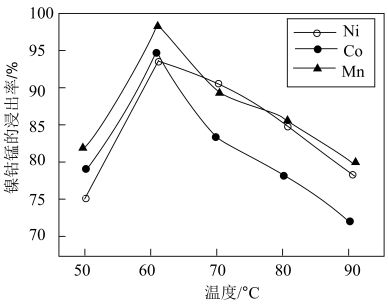
进入溶液。该过程中 的作用是。保持其他条件相同,搅拌相同时间,测得不同温度下镍、钴、锰的浸出率如图所示。60℃时浸出率达到最大,可能的原因是。
的作用是。保持其他条件相同,搅拌相同时间,测得不同温度下镍、钴、锰的浸出率如图所示。60℃时浸出率达到最大,可能的原因是。
-
(2) “除铁”生成黄钠铁矾沉淀时需控制溶液的
 为15~18.该过程中需不断加入
为15~18.该过程中需不断加入 溶液,其作用是。
溶液,其作用是。
-
(3) 物质X可调节溶液的
 , X为____(填序号)
A .
, X为____(填序号)
A . B .
B .  C .
C . 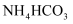
-
(4) 回收液可用于合成锂离子电池正极材料,合成前需测定其中
 等离子的浓度。
等离子的浓度。测定原理:用过量标准
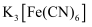 溶液氧化经预处理的回收液样品中的
溶液氧化经预处理的回收液样品中的 , 再用标准
, 再用标准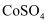 溶液滴定过量的
溶液滴定过量的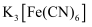 。
。反应方程式为:
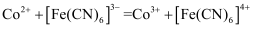 。
。测定过程:取预处理后的回收液样品
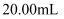 , 向其中加入
, 向其中加入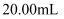
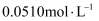
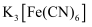 溶液,充分反应;再用
溶液,充分反应;再用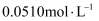
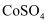 溶液滴定反应后的溶液,消耗
溶液滴定反应后的溶液,消耗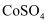 溶液
溶液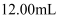 。
。数据分析:计算预处理后的回收液样品中
 的物质的量浓度。(写出计算过程)
的物质的量浓度。(写出计算过程)
最近更新
- 关于下列图示的说法中正确的① ② ③
- The little boy won’t go to sleep__________his mother tells h
- 关于x的方程有三个不等的实数解,则实数的值是 ▲ .
- 分别从集合和集合中各取一个数,则这两数之积为偶数的概率是_________.
- 将一条形磁铁从相同位置插入到闭合线圈中的同一位置,第一次缓慢插入,第二次快速插入,两次插入过程中不发生变化的物理量是 A
- Should the wallet, found in the street, be put into a pocket
- 如果与3互为倒数,那么是( ) A. B. C. D.
- 向25 mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,得到曲线如下图所示 (1)写出氢氧化钠溶液与醋酸溶液反应的
- 游泳池深水区的水深为2m,则深水区池底受到水的压强为 Pa。
- 某文化遗址出土的同一时期的文物有:(1)陶器、玉器、石器、象牙器、骨器;(2)有刻画符号的陶尊;(3)随葬品数量相差悬殊
- 下列物质在一定条件下都能导电,属于电解质的是 A.铜 B.NaOH C.SO3
- 设NA为阿伏加德罗常数的数值,则下列说法正确的是 ( ) A.在9.5g离子化
- 下列有关实验装置的说法中正确的是 A.用图1装置制取干燥纯净的NH3 B.用图2装置实验室制备Fe(OH
- -2的绝对值等于 A.2 B.-2 C. D.4
- 下列大洲中只濒临两个大洋的是( ) A .亚洲 B.欧洲 C.北美洲
- 假设甲国化妆品市场高档品牌被进口品牌垄断,为保护国内产业发展,甲国对进口化妆品提高关税,致其价格飘升;受此影响,消费者转
- 已知定义在R上的函数 , 其中函数的图象是一条连续曲线,则方程在下面哪个范围内必有实数根
- 下列词语中没有错别字的一项是 A、慰藉 悬虚 笑吟吟 B、莲漪 天
- 为节约资源、保护环境,引导公众科学合理使用塑料购物袋,国务院办公厅下发通知规定,从2008年6月1日起在全国范围内禁止生
- 小鼠毛皮中黑色素的形成是一个连锁反应,当R、C基因(两对等位基因位于两对同源染色体上)同时存在时,才能产生黑色素,如图所



