金属及其化合物 知识点题库
-
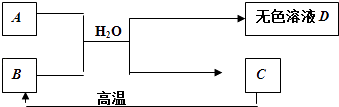
(1) C的化学式.
-
(2) D中一定含有的溶质是.理由是(用化学方程式表示).
-
(3) B用作食品干燥剂的原理:.(用化学方程式表示)
①将干燥的pH试纸浸到某溶液中,过一会取出与标准比色卡比较,测得该溶液的pH;
②用铂丝蘸取某溶液在酒精灯外焰上灼烧,直接观察火焰颜色来确认是否含有钾元素;
③通过丁达尔现象来区别硫酸铜溶液和氢氧化铁胶体;
④配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑤检验红砖中的氧化铁成分时,向红砖粉末中加入盐酸,放置至充分沉淀后,取上层清液于试管中,滴加KSCN溶液即可.
请回答:
-
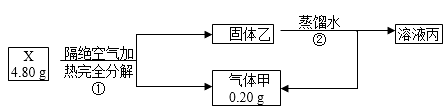
(1) X的电子式是
-
(2) 写出X与水反应的化学方程式。
-
(3) X在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式。
-
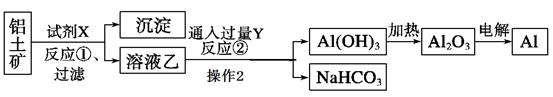
(1) 试剂X应选择(选填“氢氧化钠溶液”、“盐酸”),反应①过滤后所得沉淀为 ;反应①的离子方程式;
-
(2) 反应②中Y是(写化学式);
-
(3) 写出由Al(OH)3加热为Al2O3的反应方程式
 B .
B . 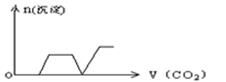 C .
C . 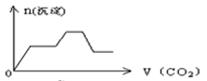 D .
D . 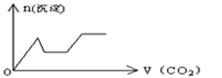
 lO2-、Al(OH)3
D .
lO2-、Al(OH)3
D . 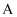 lO2-
lO2-
-
(1) (一)碳酸钙的制备

步骤①加入氨水的目的是。小火煮沸的作用是使沉淀颗粒长大,有利于。
-
(2) 下图是某学生的过滤操作示意图,其操作不规范的是(填标号)。
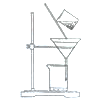
a. 漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
-
(3) (二)过氧化钙的制备
CaCO
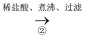 滤液
滤液 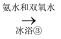
 白色晶体
白色晶体步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈性(填“酸”、“碱”或“中”。将溶液煮沸,趁热过滤。将溶液煮沸的作用是。
-
(4) 步骤③中反应的化学方程式为,该反应需要在冰浴下进行,原因是。
-
(5) 将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是。
-
(6) 制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是,产品的缺点是。
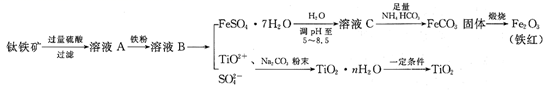
已知:TiO2+易水解,只能存在于强酸性溶液中。
回答下列问题:
-
(1) 钛铁矿用硫酸溶解时,过滤所得滤渣的成分是 (填化学式)。
-
(2) 从溶液B中得到FeSO4·7H2O晶体的操作是、过滤、洗涤、干燥。
-
(3) 溶液C中加入NH4HCO3 , 发生反应的离子方程式是。
-
(4) 煅烧FeCO3 , 发生反应的化学方程式是。
-
(5) 流程中加入Na2CO3粉末得到固体TiO2·nH2O。请结合TiO2+的水解平衡原理解释其原因:。
-
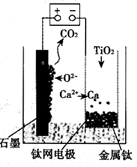
(6) 用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制取金属钛。阳极反应式是,反应过程中CaO的物质的量 (填“减小”“不变”或“增大”)。
-
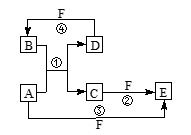
(1) 若A为短周期元素的金属单质,D为短周期元素的非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为,反应④的化学方程式为。
-
(2) 若A是常见的金属单质,D、F是气体单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是。已知1g D与F反应生成B(气态)时放出92.3kJ热量,写出该反应的热化学方程式:。
-
(3) 若A、D、F都是短周期非金属元素的单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为,B固体属于晶体。
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合生成Na2CO3 , Na2O2与CO2发生置换生成O2
③Na2O是淡黄色物质,Na2O2是白色物质
④Na2O2可作供氧剂,而Na2O不行
⑤Na2O2和Na2O焰色反应均为黄色
| 选项 | 操作 | 现象 | 结论 |
| A | 向NaAlO2溶液中滴加NaHCO3溶液 | 产生白色沉淀 | AlO |
| B | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X一定是浓盐酸 |
| C | 向某溶液中滴加几滴FeCl3溶液 | 溶液变红 | 溶液中一定含有KSCN |
| D | 用玻璃棒蘸取未知溶液进行焰色反应 | 火焰为黄色 | 说明一定含有钠元素 |
 、Cl-、OH-、HCO
、Cl-、OH-、HCO  中的多种离子。对此混合溶液进行以下分析。
中的多种离子。对此混合溶液进行以下分析。 ①取250mL该混合溶液,加入过量盐酸,收集到标准状况下气体5.6L;
②在操作①后的溶液中加入过量的NaOH溶液,过滤、洗涤、干燥得到白色沉淀5.8g;
③在操作②后的溶液中加入过量的BaCl2溶液,过滤、洗涤、干燥得到白色沉淀23.3g;
④在操作③后的溶液中加入过量的稀硝酸酸化的硝酸银溶液,产生大量的白色沉淀。
回答下列问题:
-
(1) 不做实验就可确定一定不含有的离子是。收集到的气体的化学式为。通过实验①确定一定不含有的离子是。
-
(2) 通过实验②确定一定含有的离子是。通过实验③确定一定含有的离子是。
-
(3) 写出操作②涉及的化学反应的离子方程式。
-
(4) 通过上述实验分析不能确定是否存在的离子是;K+的物质的量浓度至少为。
-
(5) 在操作③的过程中判断加入的BaCl2溶液过量的操作是。
 ,含
,含  和
和  等杂质)为原料制备铝的一种工艺流程如图所示:
等杂质)为原料制备铝的一种工艺流程如图所示: 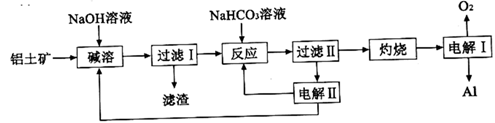
注:  在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
-
(1) 铝土矿“碱溶”时,氧化铝转化为进入溶液,提高铝土矿浸取速率的措施有(任答两点)。
-
(2) 向“过滤Ⅰ”所得滤液中加入
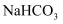 溶液,溶液的pH(填“增大”“减小”或“不变”),发生反应的离子方程式为。
溶液,溶液的pH(填“增大”“减小”或“不变”),发生反应的离子方程式为。
-
(3) “电解Ⅰ”是电解熔融的
 ,标准状况下每产生
,标准状况下每产生 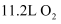 转移的电子数为。
转移的电子数为。
-
(4) “电解Ⅱ”是电解
 溶液,其原理如图所示,阳极的电极反应式为。
溶液,其原理如图所示,阳极的电极反应式为。 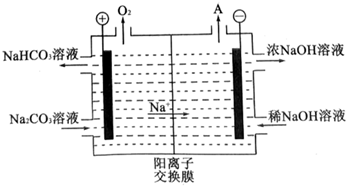
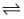 2SO3(g) ΔH=-196.6 kJ·mol-1。在生产过程中,充分利用反应放出的热量对SO2和O2进行加热,并将尾气进行循环利用。下列有关物质的性质与用途具有对应关系的是( )
2SO3(g) ΔH=-196.6 kJ·mol-1。在生产过程中,充分利用反应放出的热量对SO2和O2进行加热,并将尾气进行循环利用。下列有关物质的性质与用途具有对应关系的是( )
- --Mum, I am hungry! --- You can getsomething ______ in the
- 观察社会,融入社会(16分)㈠ 我们通过自身的观察、体会,通过浏览报刊杂志的介绍,知道了许多令人感动的事件,也知道了社会
- 阅读下面的文字,完成(1)~(4)题。 提 琴 [美国]保·琼斯 从我幼年时一直到长大离开家上大学,甚至在那之后,我舅舅
- —Will you be able to come and help us clean the room? — ___
- .小明在超市帮妈妈买回一袋纸杯,他把纸杯整齐地叠放在一起,如图请你根据图中的信息,若小明把100个纸杯整齐叠放在一起时,
- 2009年10月8日,德国女作家赫塔·缪勒获得诺贝尔文学奖。评审委员会称其“以诗歌的凝练和散文的率直,描写了失业人群的生
- 阅读下面的文言文,完成下面试题。(9分,每题3分) 杜乔字叔荣,河内林虑人也。少为诸生,举孝廉。汉安元年,以乔守光禄大夫
- 瘦肉精被认为是肉制品业的“三聚氰胺”,属食品行业的违禁药品,瘦肉精的化学式为C12H19ON2Cl3。则下列有关瘦肉精的
- 如图所示,在场强为E的匀强电场中有相距为l的A、B两点,连线AB与电场线的夹角为θ,将一电量为q的正电荷从A点移到B点.
- 已知豌豆红花对白花、高茎对矮茎、子粒饱满对子粒皱缩为显性,控制它们的三对基因自由组合。以纯合的红花高茎子粒皱缩与纯合的白
- 综合性学习 “铸剑为犁”的雕塑在联合国总部前已矗立了几十个春秋,可是和平的钟声并未向全世界渴望和平的人们敲响
- 下表给出了某校500名12岁男孩的身高资料(单位:cm):身高[122,126)[126,130)[130,134)[1
- 三打白骨精 《西游记》
- 依次填入下列各句横线上的词语,最恰当的一组是:( ) ① “9·11”事件后,以色列军方仔细核查了安全防卫系统可能出
- 结核杆菌是结核病的病原体,近年来因抗药菌株增多等原因,使人类结核病的发病率和死亡率上升,下列有关结核杆菌的叙述,正确的是
- 在由数字1,2,3,4,5组成的所有没有重复数字的5位数中,大于23145且小于43521的数共有……………………………
- 近年来,中央电视台播出的《星光大道》《我要上春晚》等节目,凭借其强大的媒体优势及创新赢得了广大观众的喜爱,成为了商家必争
- “今我朝罢丞相,设五府、六部、都察院、通政司、大理寺等衙门,分理天下庶务,彼此颉颃,不敢相压。事皆朝廷总之,所以稳当。”
- 某化学探究小组的同学准备用碳酸钠溶液与石灰水反应来制取氢氧化钠。请你与他们一起踏上实验之旅。(1)实验过程:①把石灰水加
- 四川汶川地震发生以来,截止2009年6月4日12时,已接受国内外社会各界捐款436亿元,用科学计数法记为( ) .
 结合H+的能力比CO
结合H+的能力比CO  强
强


