含硫物质的性质及综合应用 知识点题库
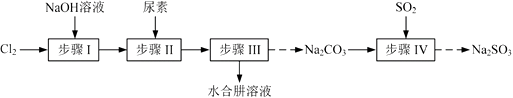
已知:①Cl2+2OH−=ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
-
(1) 步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为;实验中控制温度除用冰水浴外,还需采取的措施是。
-
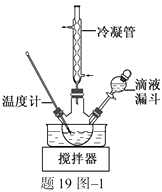
(2) 步骤Ⅱ合成N2H4·H2O的装置如题19图−1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是;使用冷凝管的目的是。
-
(3) 步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、
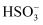 、
、  随pH的分布如题19图−2所示,Na2SO3的溶解度曲线如题19图−3所示)。
随pH的分布如题19图−2所示,Na2SO3的溶解度曲线如题19图−3所示)。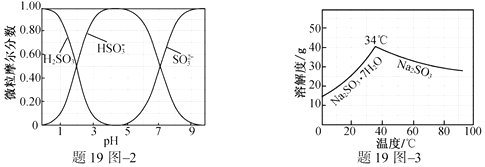
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: ,用少量无水乙醇洗涤,干燥,密封包装。
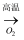 SO2
SO2 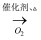 SO3
B . NaCl
SO3
B . NaCl 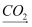 NaHCO3(s)
NaHCO3(s)  Na2CO3(s)
C . HClO
Na2CO3(s)
C . HClO  Cl2
Cl2 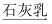 Ca(ClO)2
D . Al
Ca(ClO)2
D . Al 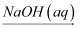 Al(OH)3
Al(OH)3  Al2O3
Al2O3
①Na2O2﹣供氧剂 ②晶体Si﹣太阳能电池 ③AgI﹣人工降雨 ④NaCl﹣制纯碱 ⑤Al2O3﹣焊接钢轨 ⑥NaClO﹣消毒剂 ⑦Fe2O3﹣红色油漆或涂料 ⑧SO2﹣食品防腐剂 ⑨NH3﹣制冷剂
⑩水玻璃﹣木材防火剂
① 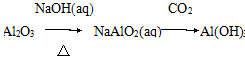
② ![]()
③ ![]()
④ 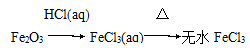
⑤ 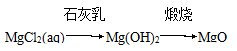
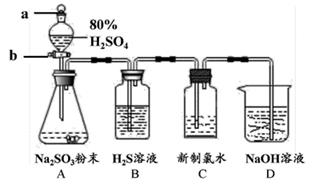
回答下列问题:
-
(1) 装置 A 用于制取SO2气体,其中发生反应的化学方程式为;
-
(2) 实验开始时,先打开分液漏斗的(填“玻璃塞 a”或“活塞 b”,下同),再打开,逐滴加入80%的H2SO4;
-
(3) 一段时间后,装置 B 中出现淡黄色(S)沉淀,可证明SO2具有(填“氧化性”或“还原性”);
-
(4) 充分反应后取装置 C 中溶液,加入(填“AgNO3溶液”、“品红溶液”或“BaCl2溶液”),出现现象,可证明SO2具有还原性;
-
(5) 装置 D 的作用是。
| 选项 | 类比 | 推理 |
| A | CO2能使澄清石灰水变浑浊 | SO2也能使澄清石灰水变浑浊 |
| B | Fe与S能直接化合生成FeS | Cu和S也能直接化合生成CuS |
| C | Fe能置换出CuSO4溶液中的Cu | Na也能置换出CuSO4溶液中的Cu |
| D | Cu与O2在加热条件下生成CuO | Na与O2在加热条件下生成Na₂O |
实验 | 实验操作和现象 |
1 | 用pH试纸测定0.1mol·L-1Na2SO3溶液的pH,测得pH约为10 |
2 | 向0.1mol·L-1Na2SO3溶液中通入少量SO2 , 测得溶液pH约为8 |
3 | 用pH试纸测定0.1mol·L-1NaHSO3溶液的pH,测得pH约为5 |
4 | 向0.1mol·L-1Na2SO3溶液中通入少量Cl2 , 无明显现象 |
下列说法不正确的是( )
 )
B . 实验2得到的溶液中存在:c(Na+) > c(HSO
)
B . 实验2得到的溶液中存在:c(Na+) > c(HSO )+2c(SO
)+2c(SO )
C . 实验3可以得出:Ka1(H2SO3)·Ka2(H2SO3) > Kw
D . 实验4中反应后的溶液中存在:c(SO
)
C . 实验3可以得出:Ka1(H2SO3)·Ka2(H2SO3) > Kw
D . 实验4中反应后的溶液中存在:c(SO )+3c(SO
)+3c(SO )=c(H2SO3)
)=c(H2SO3)
 CuSO4(aq)
CuSO4(aq) Cu
B . 饱和食盐水
Cu
B . 饱和食盐水 NaHCO3
NaHCO3 Na2CO3
C . H2S
Na2CO3
C . H2S S
S SO3
SO3 H2SO4
D . Si
H2SO4
D . Si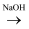 Na2SiO3
Na2SiO3 SiO2
SiO2 H2SiO3
H2SiO3
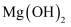 悬浊液中加入几滴
悬浊液中加入几滴 溶液,沉淀变为红褐色:
溶液,沉淀变为红褐色: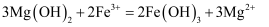 B . 过氧化钠用作潜水艇中的供氧剂:
B . 过氧化钠用作潜水艇中的供氧剂: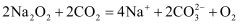 C . 收集的酸雨过一段时间后pH值会减小:
C . 收集的酸雨过一段时间后pH值会减小: D . 工业上用情性电极电解饱和氯化钠溶液生产氢氧化钠:
D . 工业上用情性电极电解饱和氯化钠溶液生产氢氧化钠:
-
(1) M的化学式为,除去
 中少量的
中少量的 杂质可选择的试剂有(填正确答案标号)。
杂质可选择的试剂有(填正确答案标号)。A.饱和
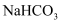 溶液 B.碱石灰 C.饱和
溶液 B.碱石灰 C.饱和 溶液 D.酸性高锰酸钾溶液
溶液 D.酸性高锰酸钾溶液 -
(2) 工业上实现①过程生产
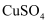 常采用废铜料与稀硫酸在通入空气并加热的条件下反应制取,其反应的离子方程式为。
常采用废铜料与稀硫酸在通入空气并加热的条件下反应制取,其反应的离子方程式为。
-
(3)
 的水溶液中各离子的浓度大小关系是,检验
的水溶液中各离子的浓度大小关系是,检验 溶液是否变质的方法是。
溶液是否变质的方法是。
-
(4) 实验室欲制备
 , 从氧化还原角度分析,下列合理的药品选择是____(填正确答案标号)。
A .
, 从氧化还原角度分析,下列合理的药品选择是____(填正确答案标号)。
A . 和
和 B .
B .  和
和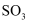 C .
C .  和S
D .
和S
D .  和
和
-
(5) 已知:常温下
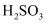 的电离平衡常数
的电离平衡常数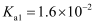 ,
, 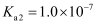 ,
, 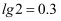 , 忽略第二步电离,则
, 忽略第二步电离,则 溶液的pH约为(保留1位小数)。
溶液的pH约为(保留1位小数)。
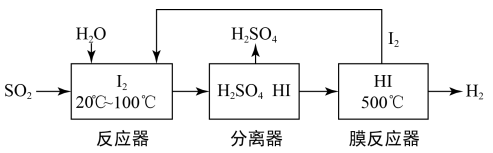
下列说法正确的是( )
 和
和 都是大气污染物,研究硫、氮及其化合物的性质,可以有效改善人类的生存环境。
都是大气污染物,研究硫、氮及其化合物的性质,可以有效改善人类的生存环境。
-
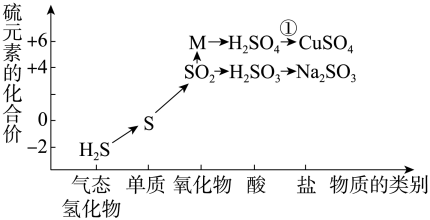
(1) Ⅰ.以下是硫元素形成物质的价类二维图及含硫物质相互转化的部分信息。
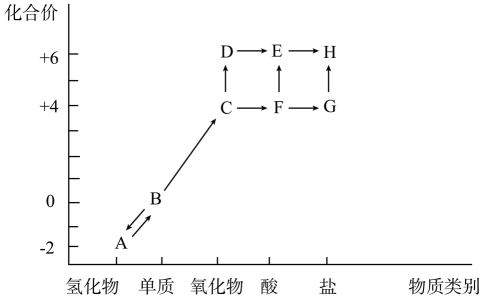
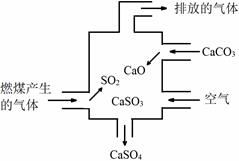
C有毒,实验室可以用NaOH溶液吸收,反应的离子方程式是。
-
(2) 检验H中阴离子所用的试剂为。
-
(3) 燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到
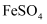 溶液。其过程如图所示:
溶液。其过程如图所示: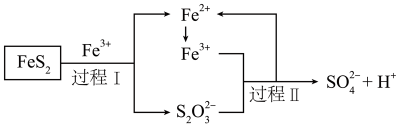
已知总反应为:
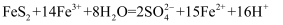 , 则过程Ⅱ反应的离子方程式。
, 则过程Ⅱ反应的离子方程式。 -
(4) 某小组同学设计实验实现几种价态硫元素的转化。

①欲制备
 , 从氧化还原角度分析,合理的是(填字母)。
, 从氧化还原角度分析,合理的是(填字母)。A.
 B.
B.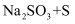 C.
C. D.
D.
②转化Ⅲ可以通入氧气来实现,写出相应化学反应方程式。
- 有关东北地区人工林的叙述,正确的是( )A.人工林是天然林区被毁后人工栽的树 B.人工林分布于东北平原中部 C.人
- 十七届三中全会强调“推进农村改革发展,关键在党”。这蕴涵的哲理是 A.要集中力量办大事
- 以旧材料纪念过去,同时又采用现代形式的中国建筑师 于2012年2月27日获得了2012年普里兹克建筑学奖,
- 植物学家在培育抗虫棉时,对目的基因作了适当的修饰,使得目的基因在棉花植株的整个生长发育期都能表达,以防止害虫侵害,这种对
- 将成熟的植物细胞放在溶液中能构成一个渗透系统,主要原因是() A.液泡膜内外溶液有浓度差 B.细胞内原生质层可看做一层选
- 如图4-2所示,吊篮P悬挂在天花板上,与吊篮质量相等的物体Q被固定在吊篮中的轻弹簧托住,当悬挂吊篮的细绳烧断的瞬间,吊篮
- 已知椭圆:,直线过点. (Ⅰ)若直线交轴于点,当时,中点恰在椭圆上,求直线的方程; (Ⅱ)如图,若直线交椭圆于两点,当时
- 按要求进行书写:(1)氯化铝溶液与足量的氨水反应的离子方程式:(2)用氯化铁溶液蚀刻印刷铜电路板反应的离子方程式: (3
- You will your dream one day if you work hard.A. climb
- 清顺治二年(1644年)浙江发生反对清朝统治的风潮,总督张存仁建议说:“速谴提学,开科取士,则读书人有出仕之望,而从逆之
- 如果△+△=*,○=□+□,△=○+○+○+○,则*÷□=( ). A. 2 B.4
- 国家卫星海洋应用中心近日透露,2020年前,我国将发射8颗海洋系列卫星,加强对我国黄岩岛、钓鱼岛以及西沙、中沙和南沙群岛
- 请回答以下生活中的问题: (1)“沙里淘金”说明黄金在自然界中能够以 (填:“单质”、“化合物”)形式存在. (2)通常
- 下表是某城市空气质量某日公布的内容: 项 目 空气污染指数 空气质量级别 空气质量 总悬浮颗粒 52 Ⅱ 良 二氧
- (本小题满分8分)2011年3月16日上午10时福岛第一核电站第3号反应堆发生了爆炸。为了抑制核辐射进一步扩散,日本决定
- 为了获得pH=9的溶液中,可以向pH=13的溶液中,添加( )的液体。A.pH=4B.pH=7C.pH=9D.pH=1
- (本小题满分15分) 已知定点A、B间的距离为2,以B为圆心作半径为2的圆,P为圆上一点,线段AP的垂直平分线l与直线
- “城市,让生活更美好”——2010年上海世博会主题,反映了当今世界各国对城市化进程中遇到的共同问题的关切,引领人们更多的
- 晓晓家的宠物狗“乐乐”在外遛完一圈后,在它的皮毛上粘了很多苍耳的果实,这一实例说明动物在自然界中能( ) A.帮助
- 下列各组词语中,只有一个错别字的一组是 A.惦量 精神涣散 销毁 莫衷一是 B.慰藉 打报不平



