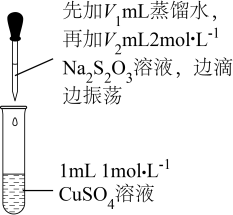含硫物质的性质及综合应用 知识点题库
下列氧化物中,能与水反应生成酸的是( )
A . SiO2
B . NO
C . Al2O3
D . SO3
下列说法正确的是( )
A . S在纯氧中燃烧可生成SO3
B . 用澄清石灰水可鉴别CO2和SO2
C . SO2能使KMnO4溶液褪色
D . CO2通入CaCl2溶液中能产生白色沉淀
用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是( )
A . 20 mL 2 mol/L FeCl3溶液
B . 40 mL 1 mol/L NaHCO3溶液
C . 20 mL 1 mol/L Na2SO3溶液
D . 40 mL 2 mol/L NH4HCO3溶液
下列化合物可由两种单质直接化合得到的是( )
A . SO3
B . NO2
C . CuS
D . FeS
自然界中能以游离态存在的元素是( )
A . 硫
B . 氯
C . 溴
D . 氢
将导出H2S气体的导管点燃后伸入盛有一定量O2的集气瓶内,下列3个反应发生的先后顺序是( )
① 2H2S + O2→ 2S + 2H2O ② 2H2S + SO2→ 3S + 2H2O ③ 2H2S + 3O2→ 2SO2+ 2H2O
A . ①②③
B . ③①②
C . ①③②
D . ③②①
在给定条件下,下列选项所示的物质间转化一步均能实现的是( )
A . NaCl(aq)  Cl2(g)
Cl2(g)  FeCl2(s)
B . MgCl2(aq)
FeCl2(s)
B . MgCl2(aq) 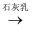 Mg(OH)2(s)
Mg(OH)2(s)  MgO (s)
C . S(s)
MgO (s)
C . S(s) 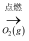 SO3(g)
SO3(g)  H2SO4(aq)
D . N2(g)
H2SO4(aq)
D . N2(g) 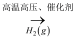 NH3(g)
NH3(g) 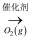 NO2(g)
NO2(g)
 Cl2(g)
Cl2(g)  FeCl2(s)
B . MgCl2(aq)
FeCl2(s)
B . MgCl2(aq) 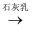 Mg(OH)2(s)
Mg(OH)2(s)  MgO (s)
C . S(s)
MgO (s)
C . S(s) 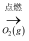 SO3(g)
SO3(g)  H2SO4(aq)
D . N2(g)
H2SO4(aq)
D . N2(g) 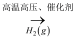 NH3(g)
NH3(g) 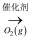 NO2(g)
NO2(g)
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A . MgCl2(熔融)  Mg(s)
Mg(s) 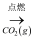 MgO(s)
B . CaC2(s)
MgO(s)
B . CaC2(s)  C2H4(g)
C2H4(g) 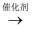
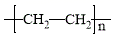 C . FeS2(s)
C . FeS2(s) 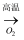 SO2(g)
SO2(g) 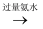 (NH4)2SO4(aq)
D . Al(OH)3(s)
(NH4)2SO4(aq)
D . Al(OH)3(s)  NaAlO2(aq)
NaAlO2(aq)  AlCl3(aq)
AlCl3(aq)
 Mg(s)
Mg(s) 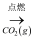 MgO(s)
B . CaC2(s)
MgO(s)
B . CaC2(s)  C2H4(g)
C2H4(g) 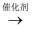
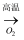 SO2(g)
SO2(g) 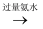 (NH4)2SO4(aq)
D . Al(OH)3(s)
(NH4)2SO4(aq)
D . Al(OH)3(s)  NaAlO2(aq)
NaAlO2(aq)  AlCl3(aq)
AlCl3(aq)
空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是( )
A . 推广使用燃煤脱硫技术,防治SO2污染
B . 实施绿化工程,防止扬尘污染
C . 研制开发燃料电池汽车,消除机动车尾气污染
D . 加大石油、煤炭的开采速度,增加化石燃料的供应量
下列说法错误的是( )
A . “爆竹声中一岁除”,爆竹中的火药含有硫黄
B . 浓硫酸可用铁制容器装运
C . 液氨可用作制冷剂
D . “雷雨发庄稼”,该过程没有硝酸生成
下列物质的转化在给定条件下能实现的是( )
①SO2  Na2SO3
Na2SO3  Na2SO4
Na2SO4
②Fe  Fe2O3
Fe2O3  Fe2(SO4)3
Fe2(SO4)3
③Al  Al2O3
Al2O3 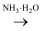 NaAlO2
NaAlO2
④N2  NO
NO  NO2
NO2  HNO3
HNO3
A . ①
B . ①②
C . ③④
D . 全部
在给定条件下,下列物质间转化能实现的是( )
A . S  SO2
SO2  H2SO3
B . NH3
H2SO3
B . NH3 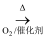 NO2
NO2  HNO3
C . Fe2O3
HNO3
C . Fe2O3 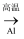 Fe
Fe  FeCl3
D . Al
FeCl3
D . Al  NaAlO2
NaAlO2 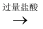 Al(OH)3
Al(OH)3
 SO2
SO2  H2SO3
B . NH3
H2SO3
B . NH3 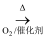 NO2
NO2  HNO3
C . Fe2O3
HNO3
C . Fe2O3 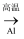 Fe
Fe  FeCl3
D . Al
FeCl3
D . Al  NaAlO2
NaAlO2 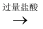 Al(OH)3
Al(OH)3
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A .  B .
B .  C .
C . 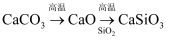 D .
D . 
 B .
B .  C .
C . 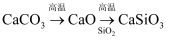 D .
D . 
下列“类推”合理的是( )
A . Na与H2O反应生成NaOH和H2 , 则Fe与H2O反应生成Fe(OH)3和H2
B . CO2可与水反应生成H2CO3 , 则SiO2可与水反应生成H2SiO3
C . 铁与硫加热反应生成FeS,则铜与硫加热反应生成Cu2S
D . Cl2与H2O反应生成HCl和HClO,则F2与H2O反应生成HF和HFO
按要求回答下列问题。
-
(1) 写出漂白粉中有效成分的化学式。
-
(2) 考古学上常用中子数为8的碳原子来测定文物的年代,写出该碳原子符号。
-
(3) 写出氢氧化钡与硫酸反应的离子方程式。
-
(4) 写出白色氢氧化亚铁被氧气氧化成红褐色氢氧化铁的化学方程式。
物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。某短周期元素的单质及其部分化合物的价类二维图如图所示。下列推断合理的是( )
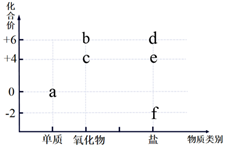
A . a到b、c、d、e、f均可直接转化
B . 标准状况下,1molb和c的混合物体积为22.4L
C . 可先加盐酸,再加氯化钡溶液检验e的钠盐是否变质
D . f的水溶液在空气中放置,不易被氧化
不能实现下列物质间直接转化的元素是( )
单质  氧化物
氧化物  酸(或碱)
酸(或碱)  盐
盐
A . N
B . S
C . C
D . Na
某课外小组探究含Cu2+的盐与Na2S2O3溶液的反应。
查阅资料:
i.2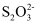 +Cu2+
+Cu2+ [Cu(S2O3)2]2-(绿色),2
[Cu(S2O3)2]2-(绿色),2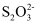 +Cu+
+Cu+ [Cu(S2O3)2]3-(无色);
[Cu(S2O3)2]3-(无色);
ii.相比较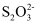 , Cu+更易与NH3络合为[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+(蓝色);
, Cu+更易与NH3络合为[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+(蓝色);
iii. 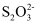 易被氧化为
易被氧化为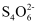 。
。
提出假设:
假设1:Cu2+与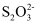 在溶液中发生络合反应生成[Cu(S2O3)2]2-;
在溶液中发生络合反应生成[Cu(S2O3)2]2-;
假设2:Cu2+与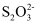 在溶液中发生氧化还原反应。
在溶液中发生氧化还原反应。
实验探究一:探究CuSO4与Na2S2O3溶液的反应。
实验操作 | 序号 | V1/mL | V2/mL | 逐滴加入Na2S2O3溶液时的实验现象 |
| a | 1.5 | 0.5 | 溶液逐渐变为绿色,静置无变化 |
b | 1.0 | 1.0 | 溶液先变为绿色,后逐渐变成浅绿色,静置无变化 | |
c | 0 | x | 溶液先变为绿色,后逐渐变浅至无色,静置无变化 |
-
(1) 假设2的推测是因为Cu2+具有性。实验c中x=。
-
(2) 根据实验a的现象可推测溶液中生成的含Cu微粒为(填化学符号)。
-
(3) 某同学认为上述实验探究一可证明假设2成立,判断理由为。
实验探究二:探究CuCl2与Na2S2O3溶液的反应。

-
(4) 经检验白色沉淀为CuCl,从化学平衡的角度解释继续加Na2S2O3溶液后CuCl沉淀溶解的原因:。
-
(5) 设计实验证明上述无色溶液中存在Cu+:。
-
(6) 经检验氧化产物以
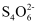 形式存在。写出Cu2+与
形式存在。写出Cu2+与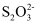 发生氧化还原反应得到无色溶液的离子方程式:。
发生氧化还原反应得到无色溶液的离子方程式:。
-
(7) 综合上述实验,可得出假设成立,试分析随着n(
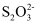 ):n(Cu2+)变化时,反应的趋势为。
):n(Cu2+)变化时,反应的趋势为。
非金属元素在化工生产中扮演着重要的角色。在众多的化工原料和产品中,都能见到硫和氮等元素的踪迹。
-
(1) Ⅰ.利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:
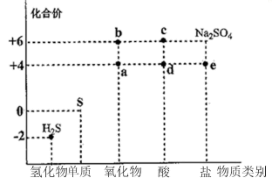
质量相同的a和b,物质的量之比为。
-
(2) 将足量的a气体通入下列溶液中,始终没有明显反应现象的是____。A .
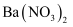 溶液
B .
溶液
B . 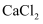 溶液
C . H2O2溶液
D . Na2CO3溶液
溶液
C . H2O2溶液
D . Na2CO3溶液
-
(3) 已知e为正盐,且能被酸性K2Cr2O7氧化为Na2SO4 ,
 被还原为
被还原为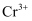 , 写出此反应的离子方程式:。
, 写出此反应的离子方程式:。
-
(4) Ⅱ.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
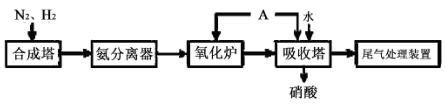
写出氧化炉中的化学反应方程式。
-
(5) 向吸收塔中通入A的作用。
-
(6) 工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用(填化学式)溶液吸收。
下列转化关系不能一步实现的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
最近更新
- 燃料电池不是把还原剂、氧化剂物质全部贮藏在电池内,而是在工作时,不断从外界输入,同时将电极反应产物不断排出电池。下面有4
- Whenwe’re young and we dream of love and fulfillment, we thi
- 分解因式:【小题1】ax2-4ax+4a【小题2】(a2+b2-c2)2-4a2b2【小题3】m2n2-3mn+2【小题
- 有关细胞的全能性说法不正确的是 ( ) A.植物组织培养成功表明高度分
- The suggestion has been made _____ the basketball game _____
- 下列词语中没有错别字的一组是() A.寒喧讴歌猩红热省吃减用 B.鞭苔偏僻销锋镝礼上往来 C.沧桑磐石号码簿一愁莫展 D
- 元朝的行省“凡钱粮、兵甲、屯种、漕运、军国重事,无不领之。”在元代以前中国主要以“山川形便”来划分行政区,行政区的自然属
- (湖北卷理7)若上是减函数,则的取值范围是( ) A. B. C. D.
- 假设你是李华,昨天收到了笔友Nick的e-mail, 得知他马上要参加期中考试,但是他在每次考试前会莫名的紧张,不知道该
- There __________ still some milk in the fridge. It’s not nec
- 2010年6月25日下午,十一届全国人大常委会第十五次会议经表决,通过了《关于修改行政监察法的决定》。修改后的《行政监察
- .He suggested the person referred _______ put into prison.
- 工业上生产MnO2和Zn的主要反应有:① MnO2+ZnS+2H2SO4= MnSO4+ZnSO4+S+2H2O;
- 高度集中的计划经济体制的特点是 ①国家运用指令性计划,直接掌握、控制人财物资源; ②权力主要集中在中央;③经济管理权限过
- 假如英语课上老师要求同学们交换修改作文,请你修改你同学写的以下作文。文中有10处错误,每句中最多有两处。错误涉及一个单词
- Boysneed friends, suffer when they don’t believe they have a
- .二战后期,美国积极推动联合国和布雷顿森林体系的建立;1949年组建北大西洋公约组织;1951年签订《日美安全保障条约》
- 下图人物被誉为无产阶级艺术最伟大的代表者,社会主义现代文学的奠基者以及无产阶级文学的导师。他是()A.鲁迅
- —I must say you really helped us out when we lost those pass
- 57号镧元素(La)是一种活泼性比铁还强的金属元素,La的氧化物的化学式为La2O3,La(OH)3是不溶于水的碱,La