物质的鉴别、推断 知识点题库
“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气,二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
①铁与氯化铁溶液在常温下发生反应生成氯化亚铁.Fe+2FeCl3═3FeCl2
②碱性的Na2CO3溶液可以和中性的CaCl2溶液发生复分解反应.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
-
(1) 【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整:
实验操作
实验现象
实验结论
①取少量固体放于试管中,滴加一定量的 , 用带导管的单孔橡皮塞塞紧试管口,导管另一端伸入澄清石灰水中.
试管中固体逐渐减少,有大量无色气体产生,得到浅绿色溶液,澄清的石灰水变浑浊.
样品中一定含有 ,不含Fe2O3
②取少量样品放入试管中,加水溶解,静置后取上层清液滴加无色酚酞试液.
试管底部有不溶物,上层清液由无色变为红色
样品中含有
【实验质疑】
小组同学通过讨论认为实验中并不能得出一定含Fe2O3的结论,理由是 (用化学方程式表示).
为进一步确定这包久置的“双吸剂”固体的成分进行如下定量试验.
-
(2)
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照如图流程进行实验,请回答相关问题:
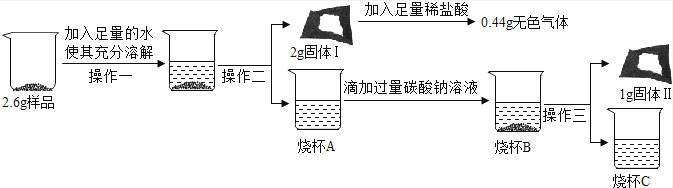
(1)操作二、操作三名称是;
(2)固体Ⅰ的成分是 (填物质化学式,下同);
(3)烧杯A中溶液和加入的碳酸钠溶液反应化学方程式为 ;
(4)依据实验探究1,2中现象的分析及数据计算判断,这包久置“双吸剂”固体的成分是 .
【实验反思】
下列对实验探究1、2的反思,不正确的是 (填字母序号).
A.对物质成分的探究有时需要定性与定量实验的结合
B.实验探究2烧杯C中的溶质为Na2CO3和NaOH
C.实验探究1、2中都有气体产生,但生成的气体成分不同
D.在原样品中加入足量盐酸有4个反应发生.
a | b | c | d | e | |
A | S | O2 | CO | H2O | CO2 |
B | H2 | O2 | Cu | 稀盐酸 | CaCO3 |
C | CuSO4 | Mg | 稀盐酸 | Zn | NaCl |
D | Al | O2 | C | CuO | H2 |


-
(1) 若甲是一种蓝色溶液,丙是一种浅绿色溶液.请写出丁的化学式.
-
(2) 若甲、乙均为黑色固体,请举出一个符合上述要求的例子,写出反应的化学方程式.
-
(3) 若丙为最清洁的气体燃料,请举出一个符合上述要求的例子,写出反应的化学方程式.
| 加入物质 | NaOH 溶液 | 氯化钡溶液 | HCl 溶液 |
| 现象 | 产生蓝色沉淀 | 产生白色沉淀 | 无明显现象 |


分析实验过程,回答;
-
(1) 白色粉末中一定有的盐是;
-
(2) 白色粉末的成分的可能组合为。
-
(1) D俗称;
-
(2) 袋装食品中常放入小袋装(透气)C,其作用是;
-
(3) 写出B与D的水溶液反应的化学方程式;该反应产生的现象是.
 、Ba2+、
、Ba2+、 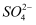 、
、  、Cl-。现取两份等质量的溶液进行如下实验:(1)第一份加足量NaOH溶液,加热,收集到气体0.68g;(2)第二份加足量BaCl2溶液后,过滤、干燥后得6.27g沉淀,将沉淀用足量盐酸洗涤、干燥后,称得不溶性固体的质量为2.33g。根据上述实验,以下推测正确的是( )
、Cl-。现取两份等质量的溶液进行如下实验:(1)第一份加足量NaOH溶液,加热,收集到气体0.68g;(2)第二份加足量BaCl2溶液后,过滤、干燥后得6.27g沉淀,将沉淀用足量盐酸洗涤、干燥后,称得不溶性固体的质量为2.33g。根据上述实验,以下推测正确的是( )
 B . 一定存在
B . 一定存在  与
与  C . 一定不存在Na+
D . 一定不存在Cl-
C . 一定不存在Na+
D . 一定不存在Cl-

|
选项 |
实验目的 |
试剂或方法 |
|
A |
鉴别FeCl3、NaCl、NaOH、MgCl2四种溶液 |
不另加试剂 |
|
B |
鉴别CaCO2、NaOH、NaCl、NH4NO3四种固体 |
水 |
|
C |
除去MgCl2溶液中少量的CuCl2 |
加入过量铁粉、充分反应、过滤 |
|
D |
除去N2中的少量O2 |
将气体缓缓通过灼热的铜网 |

-
(1) 能否依据现象②得出结论:原固体样品中一定不含Na2SO4和BaCl2 , (填“能”或“不能”) ;
-
(2) 无色溶液A中一定含有的溶质成分是;
-
(3) 下列对上述实验过程的分析,判断正确的是 。A . 白色固体a中可能含有2种物质 B . 白色固体b中滴加稀硫酸沉淀全部溶解 C . 向红色溶液中加入氯化钡溶液即可确定其成分
 、
、 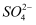 中的若干种。现取100毫升此溶液进行如下实验:①加足量BaCl2溶液后,过滤,得干燥沉淀6.27克;②在沉淀中加足量盐酸,过滤、洗涤、干燥后,称得沉淀质量为2.33克;③在滤液中滴加AgNO3溶液,产生白色沉淀。根据上述实验,下列推测中,正确的是()
中的若干种。现取100毫升此溶液进行如下实验:①加足量BaCl2溶液后,过滤,得干燥沉淀6.27克;②在沉淀中加足量盐酸,过滤、洗涤、干燥后,称得沉淀质量为2.33克;③在滤液中滴加AgNO3溶液,产生白色沉淀。根据上述实验,下列推测中,正确的是()
 、
、 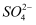 、Na+和Cl- , 一定不含Ba2+
B . 一定含
、Na+和Cl- , 一定不含Ba2+
B . 一定含  、
、 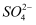 和Na+,一定不含Ba2+ , 可能含Cl-
C . 一定含
和Na+,一定不含Ba2+ , 可能含Cl-
C . 一定含  和
和 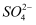 ,一定不含Ba2+ , 可能含Na+和Cl-
D . 一定含
,一定不含Ba2+ , 可能含Na+和Cl-
D . 一定含 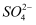 ,一定不含Ba2+和
,一定不含Ba2+和  ,可能含Cl-和Na+
,可能含Cl-和Na+


-
(1) 白色沉淀A与稀盐酸反应的化学方程式为。
-
(2) 白色沉淀C的化学式为。
-
(3) 这包白色固体是由(填化学式)组成的。

-
(1) 操作1是。
-
(2) 步骤②的现象中出现了气泡,请判断原白色固体一定含有的成分是。

-
(1) 用化学式写出: B,D
-
(2) 若无色中性液体是只含一种溶质的溶液, 则溶质可能是。(写出所有可 能的化学式)
- 下列各句中,标点符号使用正确的一项是( ) A.京剧的生态环境,包括传统审美观念、表现手段等如今已发生了巨大变化;而
- 下图示意我国及东部、中部、西部三大地带能源自给率的变化情况。完成22—23题。22.图中四条曲线代表中部地带的是 A.I
- 1943年3月为祭奠戴安澜,蒋介石在重庆献赠挽联。在延安作诗道:“外侮需人御,将军赋采薇。师称机械化,勇夺虎罴威。浴血东
- 将Cu、CuO、Cu(OH)2的混合物12g加入到稀硫酸中,恰好完全反应后,过滤,得到含硫元素的3.2%的溶液50g和滤
- —Do you think it will stop _____ noon? --- Well, it is reall
- 近年,北京市政府出台了《进一步优化发展环境的意见》。意见的要旨是“建立行政补偿制度”,即由于政府的法规、政策的修改或撤销
- 如图,△ABC中,E是AC上一点,且AE=AB,, 以AB为直径的⊙交AC于点D,交EB于点F. (1)求证:BC与⊙O
- (08年江苏卷)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一
- 荠菜果实性状——三角形和卵圆形由位于两对染色体上的基因A、a和B、b决定。AaBb个体自交,F1中三角形:卵圆形= 30
- 设NA为阿伏加德罗常数。下列叙述正确的是 ( ) A.物质的量相等的Na2O和Na2O2晶体
- 从2016年底以来,共享单车突然就在国内火爆起来。重庆的街头巷尾也随处可见小黄车的身影,确为大家带来了许多便利。可存取不
- 已知:a、b、c是△ABC的三边,化简=( ) A.2a﹣2b B.2b﹣2a C.2c
- 韩城是我国历史文化名人司马迁的故乡。司马迁的最大贡献是写成了 A. 《史记》 B。《缀术》
- 下列划线词与现代汉语意思相同的一项是( )。 (2分)A.阡陌交通,鸡犬相闻B.每三公有所选举C.清荣峻茂,良多趣味D.
- 下列说法有误的一项是( ) A.《野望》是一首描写秋天山野景致的五言律诗。诗风疏朴、自然,于平淡中表现出诗人“相顾无
- 如果某一物种缺乏适应变化着的环境所需要的变异,它可能( ) A.进化为另一新物种 B.进化到更高等形式 C.退化到低级
- 依次填入下列各句横线处的词语,恰当的一组是( ) ①我国确立的人民代表大会制度,是实现人民当家作主和保障公民政治____
- 下列词语中加点的字读音有错误的一项是( )(2分) A、伫(chù)立 憎(zēng)恶 干涸(h
- 下列语句正确的是( ) A.对角线互相垂直的的四边形是菱形 B.有两边及一角对应相等的两个三角形全等
- 碳的化合物多为共价化合物的原因是( ) A.碳属于非金属元素 B



