物质的鉴别、推断 知识点题库
A~H是初中化学常见物质,已知:A,E是红色固体;C,G是黑色粉末;B,H是气体且B为化合物;D溶液呈蓝色,可用于配制农药波尔多液,它们之间的转化关系如图所示(各步均恰好完全反应,部分生成物已略去),请回答下列问题:

(1)F溶液的溶质是 ,G是 ;
(2)反应①的化学方程式是 ;
(3)反应③的基本反应类型是 ;
(4)写出B物质的一种用途 .
-
(1) 写出物质的名称 D:.E:.在实验室物质A通常保存在
中,点燃E时,E装在 中.
-
(2) 写出①过程发生反应的文字表达式.反应的基本类型是反应.
-
(3) 写出③过程发生反应的文字表达式.反应的基本类型是反应.
①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀。
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。则该固体中一定含有( )
Ⅰ.称取15克固体于烧杯中,加入足量水充分溶解,过滤得到白色沉淀4.3克和无色滤液。
Ⅱ.往Ⅰ中所得4.3克白色沉淀中加入足量稀盐酸,沉淀部分溶解并有无色气体产生,测得剩余沉淀质量为2.33克。
Ⅲ.把Ⅰ中所得滤液等分成两份,第一份滤液加入足量的稀硫酸,既没有产生气体,也没有产生沉淀,第二份滤液中加入足量的氯化钡溶液,没有产生沉淀。
根据上述实验,回答下列问题:
-
(1) 仅根据第Ⅲ步实验现象可以得到的结论是:滤液中一定不存在的离子是。
-
(2) 写出原白色固体所有可能组成。
①将固体混合物溶于足量的水中,过滤得到白色沉淀和无色透明的溶液;
② 在白色沉淀中加入适量的稀硝酸,沉淀部分溶解并产生气泡。由以上实验可知:
-
(1) 该固体混合物中一定不存在的物质是;
-
(2) 根据以上实验现象还有一种物质不能确定是否存在。为了进一步确定该物质是否存在,小明取第②步沉淀部分溶解后的溶液少量,加入一定量的“某种溶液”:若产生白色沉淀,则有该物质;若无现象,则不含该物质。加入的一定量的则“某种溶液”应该是 。A . Na2CO3 B . Na2SO4 C . NaOH D . BaCl2
![]()
用所学化学知识判断,下列说法正确的是( )

-
(1) A的化学式。
-
(2) 白色沉淀D的化学式
①取少量固体于试管中,加适量蒸馏水,固体完全溶解得透明溶液;
②在①所得溶液中,滴加足量BaCl2溶液,产生白色沉淀.过滤后,在白色沉淀中加过量稀盐酸,沉淀部分溶解,且有气泡产生.
下列对原固体成分的说法正确的是( )

资料:BaSO4、CuS难溶于水且不与稀硫酸反应;Cu(OH)2难溶于水,可与稀硫酸反应。
-
(1) 从过滤器中分离出滤渣的成分为。
-
(2) 反应釜3中发生复分解反应的化学方程式为。
【查阅资料】①糯米中加入食用碱可起到中和微生物生成的酸、软化食物纤维等作用;
②草木灰中富含钾盐,主要成分是K2CO3 , 还含有少量K2SO4和KCl。
【实验探究】检验草木灰的成分,并测定草木灰中K2CO3的质量分数。
-
(1) 取适量草木灰于烧杯中,加足量水浸泡,过滤得到草木灰的浸出液;取少量浸出液于试管中,滴加几滴酚酞试液,观察到酚酞试液,则说明草木灰的浸出液呈碱性。
-
(2) 为了检验草木灰的浸出液中存在Cl- , 请写出实验方法:。
-
(3) 小柯用图示装置测定草木灰中K2CO3的质量分数,通过测定C装置质量的增加量来计算K2CO3的质量(草木灰中其他成分遇稀盐酸不产生气体),实验过程中需持续缓缓通入空气,其作用除搅拌B、C中的反应物外,还可以。

-
(4) 有人认为通过C装置质量增加量来计算K2CO3的质量,结果会偏大,理由是。
-
(1) 根据亚硝酸钠的化学式,你能否确定它的什么组成成分是有毒的?写出你的理由。
-
(2) 请你阅读下表有关资料,并结合已有的化学知识,设计实验:用两种方法鉴别食盐和亚硝酸钠。
项目
亚硝酸钠
氯化钠
溶解性
15℃时溶解度为81.5g
15℃时溶解度为35.8g
熔点
271℃
801℃
水溶液酸碱性
碱性
中性
跟稀盐酸作用
放出红棕色气体NO2
无现象
跟硝酸银溶液作用
生成白色沉淀
生成白色沉淀

已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物。请回答:
-
(1) G的化学式为,写出物质B的一种用途。
-
(2) C、D发生反应的化学方程式可能为。
| 选项 | 实验目的 | 实验操作 |
| A | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| B | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在足量的稀硫酸中 |
| C | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| D | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、蒸发 |

-
(1) 该反应在反应过程中(选填“吸热”或“放热”或“先放热后吸热”)。
-
(2) 40s时溶液中的溶质为。
Ⅰ.第一份加入AgNO3溶液,有沉淀生成;
Ⅱ.第二份加入足量BaCl2溶液后,得沉淀物6.63g,再经足量稀硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀生成。根据上述实验,回答下列问题:
-
(1) 第Ⅱ步中得到的沉淀物6.63g,其中的成分有(用化学式表示)。
-
(2) 根据第Ⅰ、Ⅱ步实验操作能否判断原溶液中存在Cl-。
-
(3) 原溶液中一定存在的金属阳离子是:。

-
(1) 请写出B点对应溶液的溶质是(写化学式)。
-
(2) 乙图是甲图中O点到A点的反应微观实质模型图。则“
 ”表示(写化学符号)。
”表示(写化学符号)。
-
(1) 小明最初认为试管底部的沉淀可能是镁与稀盐酸反应生成大量的MgCl2不能完全溶于水所致。但随后小明通过实验证实了沉淀不是MgCl2。你认为小明的实验操作是 。
-
(2) 小明查阅资料知道镁与水在加热的条件下能生成氢氧化镁(难溶性物质)和氢气。于是,他进行了实验验证:将去除氧化膜的镁条和水放在试管中加热,发现镁条表面有少量气泡生成。停止加热后,却始终没有观察到沉淀。请对“没有观察到沉淀”这一结果作出合理的解释。。
-
(3) 镁与水反应没有观察到沉淀,而镁与稀盐酸混合却有沉淀。小明经过思考,认为沉淀的产生与氯离子有关。后来查阅资料得知,沉淀的主要成分是一种可溶于稀硝酸,并生成氯化镁、硝酸镁和水的碱式氯化镁[Mg(OH)Cl]。请你设计实验验证沉淀中含有氯元素。。
 、
、 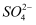 中的几种离子构成,取一定质量的该固体样品,进行如下实验:①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5g白色沉淀。
中的几种离子构成,取一定质量的该固体样品,进行如下实验:①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5g白色沉淀。 ②在沉淀中加入过量稀硝酸,仍有3g白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。则该固体中一定含有( )
 、
、 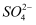 B . Cu2+、
B . Cu2+、  、
、 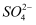 C . Cl-、
C . Cl-、  、
、 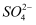 D . Na+、Ba2+、Cl-
D . Na+、Ba2+、Cl-

| 选项 |
实验目的 |
所用试剂或方法 |
| A |
稀释浓硫酸 |
把水倒入浓硫酸中,不断搅拌 |
| B |
鉴别NaCl溶液和稀盐酸 |
向盛有两种溶液的试管中分别滴入AgNO3溶液 |
| C |
除去NaOH溶液中的Na2CO3 |
加入适量的Ca(OH)2溶液、搅拌、过滤 |
| D |
验证Zn、Cu、Fe的金属活动性强弱 |
将铜片分别插入ZnSO4和FeSO4溶液中 |
- 中国领导全国各族人民进行社会主义现代化建设的历史被称之为 ( ) A.中国通史 B.中国经济
- 在人为干预下,地震损毁的某自然保护区恢复过程中的能量流动关系如下图[单位为1O3kj/(m2 .a)]。请据图分析,下列
- – Why did you _____ up these flowers ?– Because I want to gr
- pH与体积均相同的氢氧化钠溶液和氨水,分别与同浓度、同体积的AlCl3溶液反应,生成沉淀的质量也相同,则可能是(
- 冬天,我省有许多菜农利用温室栽培蔬菜。在温室中,蔬菜可直接在土壤中栽培,也可利用人工配制的营养液进行无土栽培。请回答下列
- 某市号召居民节约用水,为了解居民用水情况,随机抽查了20户家庭某月的用水量,结果如表,则这20户家庭这个月的平均用水量是
- Be careful not to _____ any word when you copy the important
- 下列是与微生物培养有关的问题,请回答: (1)某细菌固体培养基的组成成分是KH2PO4、Na2HPO4、MgSO4、葡萄
- 电动势为E=12 V的电源与电压表和电流表串联成闭合回路,如果将一电阻与电压表并联,则电压表读数减小为原来的,电流表的读
- 根据金属活动性顺序分析,下列描述或判断正确的是() A.金属钾能与硫酸锌溶液发生化学反应得到金属锌 B.金属铁与硫酸溶液
- 2013年1月29日,国务院总理邀请12位基层群众参加政府工作报告征求意见座谈会,他们中有教师、网络微博负责人、家政服务
- 下列离子方程式正确的是 ( ) A.向NaOH溶液中通入少量CO2
- 下列选项是无理数的为() A. B. C.3.1 D.
- 已知,,求证:.
- 如图在边长为1个单位长度的小正方形组成的网格中,给出了格点△ABC、直线l和格点O. (1)画出△ABC关于直线l成轴对
- 只用C、CO、CuO、CaCO3、稀盐酸五种物质,进行单一或两两反应,可写出生成物中有CO2的化学方程式有( )
- 依次填入下面横线处的词语,恰当的一组是( ) ①虽然人证物证俱在,但他还在为自己____________ 。 ②对于
- (2011•攀枝花)在同一平面内下列4个函数;①y=2(x+1)2﹣1;②y=2x2+3;③y=﹣2x2﹣1;④的图象不
- Only when he apologizes for his rudeness ____to him again.
- 在一个倾斜的长冰道上,一群孩子排成队,每隔1s有一个小孩坐在雪橇上从同一个位置无初速往下滑,每个孩子使用相同的雪橇。一位



