物质的鉴别、推断 知识点题库
A﹣I是初中化学中常见的物质.它们之间有如图所示的转化关系.已知A为铝土矿的主要成分,通常情况下F是一种液体,C、D、H、I为气体,H能参与绿色植物的光合作用,G为黑色固体.

请回答下列问题:
(1)G的化学式是 .
(2)H+单质碳→I,其反应条件是 .
(3)A B+C的化学方程式是 .
B+C的化学方程式是 .
(4)I+F(气体) H+D的化学方程式是.
H+D的化学方程式是.
据报道杭州有不法商贩用自来水冒充纯净水出售。自来水在消毒过程中通常会发生化学反应,其反应的微观过程可用甲乙两图表示( ![]() 表示氯原子,
表示氯原子, ![]() 表示氧原子,
表示氧原子, ![]() 表示氢原子)。对此有下列判断,其中错误的是( )
表示氢原子)。对此有下列判断,其中错误的是( )


-
(1) 写出下列物质的化学式:A;
-
(2) 反应②的基本反应类型是;
-
(3) 写出如图中反应①、③的化学方程式:
①;
③.
-
(1) 测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%。该样品a的水溶液中,含量最多的离子是(填离子符号)。
-
(2) 探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种)。请设计实验方案,完成下列表格。限选试剂:BaCl2溶液、NaOH溶液、AgNO3溶液、蒸馏水。
实验操作
预期现象及结论
步骤1:取少量样品b于烧杯中,
样品溶解,形成无色溶液
步骤2:取少量步骤1形成的溶液于试管中,再滴加少量NaOH溶液,振荡
,说明样品b中添加了镁盐
步骤3:
| 待鉴别的物质 | 鉴别试剂 | |
| A | 稀盐酸和稀硫酸 | 硝酸银溶液 |
| B | 氢氧化钡固体和氯化钡固体 | 水 |
| C | 氧气、二氧化碳气体 | 澄清的石灰水 |
| D | 氢氧化钠溶液和碳酸钠溶液 | 酚酞试液 |
【资料】氯化钙、氯化钡、氯化钾三种溶液均呈中性。

-
(1) 依据步骤①的实验现象得出固体物质中一定不含(填化学式)。
-
(2) 步骤②中发生反应的化学方程式为。
-
(3) 根据上述实验得出固体物质中一定含有(填化学式,下同),可能含有。为进一步确定可能含有的物质,采用的方法是(写出实验的操作、现象和结论)。
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别NaOH和NaCl固体 | 分别加少量水溶解 |
| B | 鉴别棉线和羊毛线 | 点燃后闻气味 |
| C | 除去H2中少量的水蒸气 | 将混合气体通过装有浓硫酸的洗气瓶 |
| D | 检验Na2CO3溶液中是否混有NaCl | 加入过量的稀盐酸后,再滴加硝酸银溶液 |

①图一用滴管滴入一定量的溶液后,烧杯中的溶液恰好由红色变成无色,滴管中的试剂是溶液,此时是图二中的(填“A”、“B”或“C”) 点,继续滴加该试剂,得到完整的图二、图三。根据图三的变化分析,判定此化学反应发生的依据是;
②图三 C 点溶液中含有的溶质是;
③在没有指示剂的情况下,反应结束后,为了确认酸.碱.反.应.确.实.发.生.,下列试剂不能实现的是。
A.铁粉 B、AgNO3 溶液 C、Na2CO3 溶液 D.氧化铜粉末

①将稀盐酸分别滴入试管甲和乙中,如图所示;
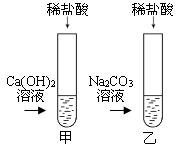
②将反应后甲、乙试管中的废液倒入一洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成,过滤 后得到白色沉淀和无色滤液;
③取少量滤液于试管中,滴加少量碳酸钠溶液,无明显现象;
④取少量滤液于试管中,滴加少量盐酸,有气泡产生。则②的无色滤液中( )
Ⅰ。现取样品16g于烧杯中并加84g水搅拌,全部溶解。再向烧杯中逐渐滴加26.1%硝酸钡溶液并不断搅拌,烧杯内固体的质量随加入硝酸钡溶液的质量的变化如图甲所示;
Ⅱ。在B点开始,向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图乙所示。则下列错误的是( )

第一步:通过观察发现 E 溶液呈蓝色,其它溶液均为无色;
第二步:取少量A、B、C、D溶液,分别滴加E溶液,现象为:A溶液中出现白色沉淀,B溶液中出现蓝色沉淀,C和D溶液均无明显现象;
第三步:取第二步中产生的蓝色沉淀,滴加C溶液后沉淀消失。则:
-
(1) A溶液中溶质的化学式是;
-
(2) 写出B和E反应的化学方程式:
-
(1) 下列铜制品中,利用金属导热性的是__________(填字母序号)。A . 铜质奖牌
 B . 铜导线
B . 铜导线 C . 铜火锅
C . 铜火锅
-
(2) “湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为。
-
(3) 利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):已知2Cu+2H2SO4+O2
 2CuSO4+2H2O
2CuSO4+2H2O

A~E中含铜、锌两种元素的物质有(填字母序号)。

【已知:Fe+Fe2(SO4)3=3FeSO4;SiO2不溶于水,也不与稀硫酸反应】
-
(1) 操作①的名称是。
-
(2) 溶液A中的溶质除H2SO4外,还存在。
-
(3) 上述流程中生成固体c的化学方程式。

-
(1) 溶液b中的溶质有。
-
(2) 小科不直接往固体B中加入稀硫酸制备BaSO4的原因是。

-
(1) 若 A 是紫红色金属,D 为难溶性碱.则D 的化学式为,C转化为 A 的化学方程式为。
-
(2) 若 A属于氧化物,其相对分子质量为56,A与水化合得B,C是白色难溶固体,则由D转化为C的化学方程式为。
- 近来,因为8月后钢市陷入暴跌行情,让多地钢厂开始裁员。这主要说明,价值规律能够( ) A.调节市场的供求关系
- 如图11甲所示,是“测定小灯泡额定功率”的实物连接图,其中电源是三节新干电池,灯泡额定电压是3.8V,其灯丝电阻约是10
- 甲~辛等元素在周期表中的相对位置如右表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,
- 甲图表示生物体内细胞呼吸的过程,图中a—i表示某物质,①—⑤表示相关生理过程,据图回答: (1)①—⑤过程
- 若圆与轴相切于点,与轴的正半轴交于两点,且,则圆的标准方程是( ) A. B. C.
- 下列说法中错误的是 A.凡是放热反应和熵增加的反应,就更易自发进行 B.对于同一物质在不同状态时的熵值是:气态>液
- 2008年北京奥运会期间,我国在奥运村设置专门的宗教服务中心,有专业神职人员为各国运动员和官员提供宗教服务。这表明………
- 借助楔形文字而得以传承下来的文学作品是 A.《摩诃婆罗多》 B.《吉尔伽美什》 C.《罗摩衍那》 D.《荷马史诗》
- 与最接近的两个整数是( )A.1和2 B.2和3 C.3和4 D.4和5
- 胡适曾经指出:“……变换了全国的空气,解除了一个不能为善而可以为恶的最上层高压势力,然后才能有各种革命的新种子在那个解放
- 有人认为,《史记》中的黎鼾就是埃及著名的亚历山大城,汉武帝遣使前往的西域诸国中也包括黎鼾。751年,杜环在与大食作战中被
- 下图是制作临时装片的四个步骤,这四个步骤的正确顺序应是( ) A ①②③④ B ②③④① C ④②①③
- 已知0<x<y<a<1,则有A.loga(xy)<0 B
- 在蛋白质的鉴定实验中,滴加的双缩脲试剂A和B的量依次是 A.都是1mL B.1 mL, 4滴 C. 4滴
- 下列有关空气各成分的说法正确的是( ) A.氧气的化学性质比较活泼,属于可燃物 B.二氧化碳属于空气污染物 C.
- 热水法制备Fe3O4纳米颗粒的反应为: 3Fe2++2S2O32—+O2+xOH-===Fe3O4+S4O62—+2H2
- 61. —How long doesit take you to cook these potatoes? —It___
- 完形填空Frank and Dale 1 students. They are good 2 . They
- —Is this your school ID card? —No, it's not . My ID car
- 玉米根尖细胞所含的核酸中,含有碱基种类数共有()A. 8 B. 7 C. 5 D. 4



