物质科学(二) 知识点题库
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为 16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量。
数据如下表:
|
锥形瓶 |
锥形瓶+稀盐酸 |
锥形瓶+反应后溶液 |
|
|
质量(克) |
35.5 |
55.5 |
80.5 |
-
(1) 本次实验中,实际消耗的氢氧化钠溶液质量为克。
-
(2) 该瓶稀盐酸的溶质质量分数为。
-
(3) 另有同学做了同样的实验,却得到了不同的结果。于是用精密 pH 试纸测得反应后锥形瓶内溶液的 pH 为 8.2,则他测出的盐酸溶质质量分数(选填“偏大”或“偏小”)。

-
(1) 过程②中,铁钉主要与空气中的氧气、发生反应。
-
(2) 过程③中除去铁锈的化学方程式为。
-
(3) 如果用a、b、c分别代表光亮铁钉、锈蚀铁钉、无锈铁钉,则它们的质量由大到小的顺序为(用字母表示)。

-
(1) 图中字母在水循环中所代表环节是:A.蒸发;B.;C.降水。
-
(2) 南水北调改变的是(填字母)这一环节。
-
(3) 使水循环连续进行的动力是:和地心引力。
-
(1) 烹饪前,在锅内加入适量水,再加入葱、姜、盐、料酒等调味品。这些调味品分别与水充分混合后,能形成溶液的有。
-
(2) 人们往往会把鸡放入高压锅内烹饪,以缩短加热时间。这是因为高压锅内气压增大,水的沸点会。
|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
|
|
溶解度(g) |
A |
35 |
35.5 |
36 |
36.5 |
37 |
|
B |
6 |
10 |
18 |
36.5 |
50 |
|
-
(1) 若将B物质从溶液中结晶析出,宜采用的方法是:。
-
(2) 我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天晒盐”。据此你认为表中(填“A”或“B”)物质的溶解度与氯化钠相似。

-
(1) 请写出图中带有标号仪器的名称:①。
-
(2) 实验中制取的氧气可以用上图中的(填字母)装置来收集。
-
(3) 用制得的氧气完成D装置所示实验,该实验的现象是。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】他以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
|
实验序号 |
KClO3质量 |
其他物质质量 |
待测数据 |
|
① |
1.2g |
/ |
|
|
② |
1.2g |
CuO 0.5g |
|
|
③ |
1.2g |
MnO2 0.5g |
-
(1) 上述实验应测量的“待测数据”是
-
(2) 若实验②比实验①的“待测数据”更 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
-
(3) 将实验②反应后的固体加水溶解、过滤、洗涤、干燥,称量仍得到0.5g氧化铜,若要验证氧化铜是该反应的催化剂,还需验证氧化铜的不变。
【预期结论】氧化铜也能作氯酸钾的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是。


【提出猜想】干燥剂中可能含有CaO、Ca(OH)2、CaCO3。
【实验探究】小组讨论后设计如图所示实验进行探究:
【实验结论】①在实验步骤B中有放热现象说明干燥剂含有。
②在实验步骤B中的白色沉淀物可能含有哪些物质?。
③在实验步骤D中形成红色溶液,说明干燥剂中含有Ca(OH)2 。
【分析与交流】小金经过分析认为实验结论③不准确,理由是。
| 物质 | R | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
| 反应前质量/g | m1 | m2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | m3 | m4 | m5 |
①m1=  m4时,R是H2
m4时,R是H2
②m1+m2=m3时,R是C或CO
③m3:m4=11:9时,R是CH4或CH4O
④ 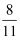 m3+
m3+ 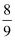 m4+
m4+  m5≥m2
m5≥m2
|
实验操作 |
0 |
1 |
2 |
3 |
4 |
5 |
|
加入稀盐酸的总质量(克) |
0 |
2.5 |
5 |
7.5 |
10 |
12.5 |
|
烧杯和相关物质的总质量(克) |
74.50 |
77.00 |
79.50 |
81.78 |
84.06 |
86.56 |
查阅资料发现:碳酸钠与盐酸发生的化学反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,实验过程中,若碳酸钠过量时发生的化学反应:Na2CO+HCl=NaHCO3+NaCl,碳酸钠完全反应后继续加入盐酸发生的化学反应:NaHCO3+HCl=NaCl+H2O+CO2↑。

-
(1) 该实验结束后,往烧杯中滴入紫色石蕊试液,溶液呈色。
-
(2) 根据实验数据计算稀盐酸的溶质质量分数。
-
(3) 已知随着加入的稀盐酸总质量的增加,溶液中Na+的数量变化如图乙所示。用图像表示出实验过程中溶液里HCO3-的数量变化。

| 温度(℃) | 20 | 50 |
| 溶解度/g | 30 | 110 |
-
(1) ①~④杯溶液中,是该温度下A物质的饱和溶液的是:。(填序号)
-
(2) ④中溶液的溶质质量分数是。
-
(3) 像A这种溶解度受温度影响较大的固体物质,一般用的方法获得晶体。


| 常见物质的溶解度(20 ℃) | ||||
| 物质名称 | 氯酸钾 | 硝酸钾 | 氯化钠 | 蔗糖 |
| 溶解度/g | 7.4 | 31.6 | 36.0 | 203.9 |
- 如图,点、、是上的三点,. (1)求证:平分. (2)过点作于点,交于点.若,,求的长.
- 下列各选项中加线字的解释错误的一项是 ①从此道至吾军,不过二十里耳《史记·项羽本纪》(名词,道路) ②师者,所以传道受业
- 在答题卷横线上填入相应的诗句。(每空1分,共13分,错字、漏字、添字,该空均不得分。) (1)何当共剪西窗烛,
- 某人欲估算飞机着陆时的速度,他假设飞机着陆过程在平直跑道上做匀减速运动,在跑道上滑行的距离为s,从着陆到停下来的时间为t
- 如图,在△ABC中,AB=10,AC=8,BC=6,经过点C且与边AB相切的动圆与CB,CA分别相交于点E,F,则线段E
- 当一个人的情绪不好时,应该采取一些方法进行调节。下列方法中错误的是( ) A.当某一件事没有成功时,找一个理由来安慰
- 19.仿照下面句子,另写两句富有意蕴的句子。(2分) 故乡的歌是一支清远的笛,总在有月亮的晚上响起。 故乡的歌是___
- “其目的不是同共产主义作斗争,而是同经济失调作斗争,因为经济失调很容易使一切极权主义运动在欧洲社会混水摸鱼,现在俄国共
- 函数的最大值为 ;
- 绘制等高线地形图时,选择等高距的主要依据是( )。 A.绘图纸张大小 B.地形海拔的高
- 下列各句中加线的熟语使用不恰当的一项是: A.生活对于任何人都非易事,我们必须有相机行事的精神,最要紧的还是我们要有
- 如图,是函数的导函数的图象,则下面判断正确的是( ) A. 在区间(-2,1)上是增函数 B. 在(1,3)上是
- 益阳市生产的松花皮蛋全国闻名。将水、生石灰、纯碱、食盐按100∶11.2∶5.3∶3.5的质量比混合而成料浆,将鲜鸭蛋粘
- 2010年举办上海世博会,是党中央、国务院站在新的历史起点上,根据中国经济社会发展的新形势新任务,从实践科学发展观、构建
- 分子式为C5H12O且可与金属钠反应放出氢气,且能发生消去反应的有机化合物有(不考虑立体异构) A.5种
- 为配制0.1mol/L的NaOH溶液,下列说法中正确的是( ) A.取4g NaOH固体溶于1L水中
- 右图是自制的平行光源的装置。实验时移动小水瓶的位置,当小灯泡位于水透镜的 处时,才会有平行光束从细缝中射出。
- 某温度时,将20 g KNO3溶解在100 g水中恰好饱和,关于该饱和溶液的叙述正确的是( ) A.m(溶质)∶m(溶剂
- 我们经常提到的像:①小孔成像 ②平面镜成像 ③放大镜成像 ④电影屏幕上的像 ⑤汽车倒后镜中的像。下列关于以上像的描述正确
- 温家宝总理说:“信心比货币和黄金还重要,一个民族、一个国家在困难的时候,如果失去信心,那就失去一切,有了信心,才有力量的



