第二章 开发海水中的卤素资源 知识点题库
等体积NaCl、MgCl2、AlCl3溶液分别与足量的AgNO3溶液反应。若生成的沉淀的物质的量之比为3︰2︰1,则三种盐酸盐溶液的物质的量浓度比为 ( )
A . 1︰2︰3
B . 9︰6︰1
C . 3︰2︰1
D . 9︰3︰1
实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气设计了如下实验装置。
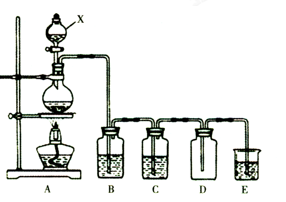
请按要求回答下列问题:
-
(1) 仪器X的名称为。
-
(2) 已知装置B中选用的试剂为饱和食盐水,其作用为 。
-
(3) 将氯气通入C中的紫色石蕊试液,可以观察到的现象是。
-
(4) 装置E中装有NaOH溶液,该装置中反应的化学方程式 。
可用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下,下列说法错误的是()
盐卤 ![]() Mg(OH)2
Mg(OH)2 ![]() MgCl2溶液
MgCl2溶液 ![]() MgCl2•6H2O
MgCl2•6H2O ![]() MgCl2
MgCl2 ![]() Mg
Mg
A . 若在实验室进行操作①只需要漏斗和烧杯两种玻璃仪器
B . 操作①发生的反应为非氧化还原反应
C . 操作②是蒸发浓缩结晶
D . 在整个制备过程中,未发生置换反应
宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”涉及的化学反应是:4Ag + 2H2S + O2 = 2X + 2H2O,下列说法错误的是( )
A . X的化学式为Ag2S
B . 还原性:H2S>H2O
C . 每消耗11.2L O2 , 反应中转移电子的数目为2NA
D . X是氧化产物
下列四个反应
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2
③Cl2+H2O=HCl+HClO ④C+H2O(g)  CO+H2
CO+H2
试从氧化还原的角度,回答下列问题:
-
(1) 水只作还原剂的是(填序号)
-
(2) 二氧化氯(ClO2)是一种在水处理方面有广泛应用的高效安全消毒剂,而且不会产生对人体有潜在危害的物质。工业上可以用如下方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。反应中氧化剂是,生成1.25mol氧化产物共转移电子mol。写出该反应的离子方程式。
下列反应中,硝酸只表现氧化性的是( )
A . 3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O
B . C+4HNO3(浓) 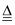 CO2↑+4NO2↑+2H2O
C . Al(OH)3+3HNO3=Al(NO3)3+3H2O
D . 3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O
CO2↑+4NO2↑+2H2O
C . Al(OH)3+3HNO3=Al(NO3)3+3H2O
D . 3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O
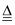 CO2↑+4NO2↑+2H2O
C . Al(OH)3+3HNO3=Al(NO3)3+3H2O
D . 3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O
CO2↑+4NO2↑+2H2O
C . Al(OH)3+3HNO3=Al(NO3)3+3H2O
D . 3Zn+8HNO3=3Zn(NO3)2+2NO↑+4H2O
对溶液中下列离子进行检验,正确的操作是( )
A . NH4+:取样,加入氢氧化钠溶液,即产生使湿润红色石蕊试纸变蓝的气体
B . SO42-:取样,加入足量的盐酸无现象,再滴入氯化钡溶液有白色沉淀产生
C . Fe2+:取样,滴入硫氰化钾溶液无现象,再加入过量的氯水,溶液呈血红色
D . Cl-:取样,滴入硝酸银溶液产生白色沉淀,再加入过量的硫酸沉淀不消失
在下列元素中,与氢气反应最剧烈的是( )
A . 氟
B . 氯
C . 溴
D . 碘
设  为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:
为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:  。下列说法正确的是( )
。下列说法正确的是( )
 为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:
为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:  。下列说法正确的是( )
。下列说法正确的是( )
A . 如果氯气管道漏气,则会看到有大量白雾生成
B . 反应中每形成 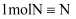 键,转移电子数为
键,转移电子数为 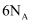 C .
C . 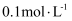 的
的  溶液中,
溶液中,  的数目小于
的数目小于  D . 该反应中,氧化剂与还原剂的物质的量之比为
D . 该反应中,氧化剂与还原剂的物质的量之比为 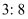
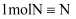 键,转移电子数为
键,转移电子数为 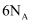 C .
C . 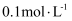 的
的  溶液中,
溶液中,  的数目小于
的数目小于  D . 该反应中,氧化剂与还原剂的物质的量之比为
D . 该反应中,氧化剂与还原剂的物质的量之比为 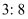
24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL浓度0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4 , 则元素Cr在还原产物中的化合价为( )
A . +2
B . +3
C . +4
D . +5
下列说法错误的是( )
A . 液氨可用作制冷剂
B . 硫酸铜能杀死某些细菌,常用作游泳场馆池水的消毒剂
C . 工业上通常采用高温冶炼黄铁矿(主要成分FeS2)的方法获得铁
D . 碘化银可用于人工降雨
下表中对应关系错误的是( )
| A | NaCl=Na++Cl-; NH3·H2O | 均属于电离方程式 |
| B | Ba2++SO HCO | 均可表示一类反应 |
| C | SO2使酸性高锰酸钾溶液褪色; SO2使碱性酚酞溶液褪色 | 均利用SO2的同一性质 |
| D | Cl2+2NaOH=NaCl+NaClO+H2O; 3S+6NaOH=2Na2S+Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
A . A
B . B
C . C
D . D
下列反应属于氧化还原反应又不属于四种基本反应类型的是( )
A . 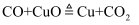 B .
B .  C .
C . 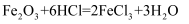 D .
D . 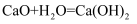
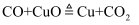 B .
B .  C .
C . 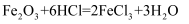 D .
D . 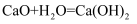
用高分子吸附树脂提取卤水中的碘(主要以I-形式存在)的工艺流程如图:下列说法错误的是( )
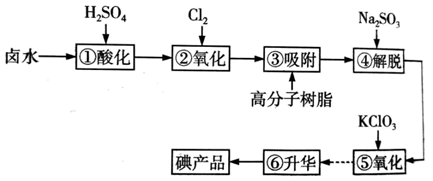
A . 高分子树脂在流程中起到富集I2的作用
B . ④中的Na2SO3起到氧化剂的作用
C . 若②和⑤中分别得到等量的I2 , 则消耗的n(Cl2):n(KClO3)=5:2
D . 由⑥得到碘产品的过程,主要发生的是物理变化
三氟化氮(  )是微电子工业中优良的等离子刻蚀气体。它在潮湿的环境中能发生反应:
)是微电子工业中优良的等离子刻蚀气体。它在潮湿的环境中能发生反应: 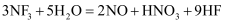 。下列有关该反应的说法正确的是( )
。下列有关该反应的说法正确的是( )
 )是微电子工业中优良的等离子刻蚀气体。它在潮湿的环境中能发生反应:
)是微电子工业中优良的等离子刻蚀气体。它在潮湿的环境中能发生反应: 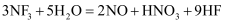 。下列有关该反应的说法正确的是( )
。下列有关该反应的说法正确的是( )
A .  是氧化剂,
是氧化剂,  是还原剂
B . 还原剂与氧化剂的分子数之比为
是还原剂
B . 还原剂与氧化剂的分子数之比为 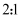 C . 若生成
C . 若生成 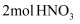 ,则转移
,则转移 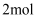 电子
D .
电子
D .  是还原产物,
是还原产物, 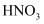 是氧化产物
是氧化产物
 是氧化剂,
是氧化剂,  是还原剂
B . 还原剂与氧化剂的分子数之比为
是还原剂
B . 还原剂与氧化剂的分子数之比为 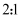 C . 若生成
C . 若生成 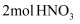 ,则转移
,则转移 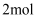 电子
D .
电子
D .  是还原产物,
是还原产物, 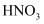 是氧化产物
是氧化产物
实验室常用MnO2与浓盐酸反应制备Cl2 , 并开展相关探究。
-
(1) 制备实验开始时,先检查装置气密性,接下来的操作依次是___ (填序号)。A . 往烧瓶中加入MnO2粉末 B . 加热 C . 往烧瓶中加入浓盐酸
-
(2) 利用制得的Cl2 , 可以制备多种含氧酸盐。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并探究两者的氧化性强弱。
已知:氯气与碱反应在常温下生成次氯酸盐,温度较高时生成氯酸盐。且反应放出热量。
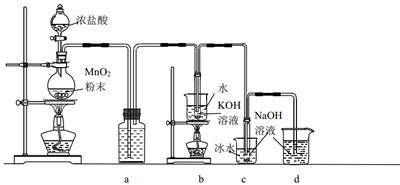
①c中采用冰水浴冷却的目的是。
②反应结束后,取出b中试管,经、、过滤、洗涤、干燥,得到KClO3晶体。
③取少量KClO3和NaClO溶液分别置于1号和2号试管中,再滴加KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显色。可知该条件下KClO3的氧化性 NaClO(填“强于”或“弱于”)。
实验室常用KMnO4与浓盐酸反应来制备氯气:2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,在此反应中:
-
(1) 氧化剂是,氧化产物是。(填化学式)
-
(2) 氧化剂与还原剂的物质的量之比为。
-
(3) 若生成71 g Cl2 , 则消耗的HCl是mol,被氧化的HCl是mol,转移的电子的物质的量是mol。
-
(4) 将此反应改写成离子方程式。
甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O2氧化CH4生成CH3OH的催化剂,反应过程如图所示。下列叙述错误的是( )
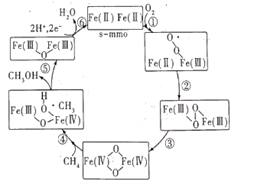
A . 基态Fe原子的核外电子排布式为[Ar]3d64s2
B . 步骤③有非极性键的断裂和极性键的形成
C . 每一步骤都存在铁和氧元素之间的电子转移
D . 图中的总过程可表示为:CH4+O2+2H++2e-  CH3OH+H2O
CH3OH+H2O
 CH3OH+H2O
CH3OH+H2O
钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,该过程表示为:Na+(x+y)NH3 Na+(NH3)x+e-(NH3)y , 下列说法错误的是( )
Na+(NH3)x+e-(NH3)y , 下列说法错误的是( )
 Na+(NH3)x+e-(NH3)y , 下列说法错误的是( )
Na+(NH3)x+e-(NH3)y , 下列说法错误的是( )
A . 钠加入液氨中溶液的导电性增强
B . e-(NH3)y的可能结构为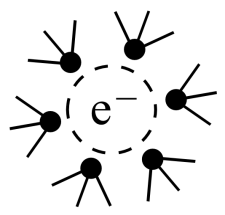 C . e-(NH3)y具有强还原性,钠/液氨体系可以还原炔烃、苯等有机物
D . e-(NH3)y在液氨体系中会产生H2
C . e-(NH3)y具有强还原性,钠/液氨体系可以还原炔烃、苯等有机物
D . e-(NH3)y在液氨体系中会产生H2
 C . e-(NH3)y具有强还原性,钠/液氨体系可以还原炔烃、苯等有机物
D . e-(NH3)y在液氨体系中会产生H2
C . e-(NH3)y具有强还原性,钠/液氨体系可以还原炔烃、苯等有机物
D . e-(NH3)y在液氨体系中会产生H2
在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是( )
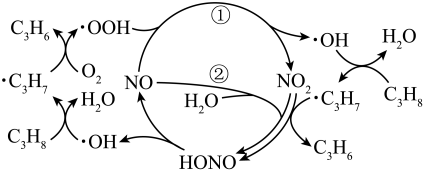
A . 含N分子参与的反应一定有电子转移
B . 由NO生成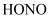 的反应历程有2种
C . 增大NO的量,
的反应历程有2种
C . 增大NO的量, 的平衡转化率不变
D . 当主要发生包含②的历程时,最终生成的水减少
的平衡转化率不变
D . 当主要发生包含②的历程时,最终生成的水减少
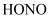 的反应历程有2种
C . 增大NO的量,
的反应历程有2种
C . 增大NO的量, 的平衡转化率不变
D . 当主要发生包含②的历程时,最终生成的水减少
的平衡转化率不变
D . 当主要发生包含②的历程时,最终生成的水减少
最近更新
- 如图,两个同心圆,大圆半径为5cm,小圆的半径为3cm,若大圆的弦AB与小圆相交,则弦AB的取值范围是.
- --- Judy, could you tell me_______the schoolbag? --- Oh, yes
- “Isn’t it about time you _____ to do morning exercises?” “Ye
- 鸦片战争后中国社会逐步沦为( ) A.封建社会 B.半殖民地半封建社会 C.殖民地
- 假如你身处偏远海岛,缺乏生存所需的淡水怎么办?小明为你提供一种简便的海水淡化方法。在地面上挖一水池,往池内灌海水,按图所
- “类推”是化学学习过程中常用的思维方法.现有以下类推结果,其中正确的是() A.因为碱溶液呈碱性,所以呈碱性的溶液一定
- 把红、蓝、黑、白4张纸牌分给甲、乙、丙、丁4个人,每人分得一张,事件“甲分得红牌”与事件“乙分得红牌”是( ) A.
- 下图是1956~1964年我国工业与农业的发展趋势示意图。根据该图,判断下列说法正确的是( ) A.1960年工
- 已知数列的前项和为,若,. (1)求数列的通项公式; (2)(II)若数列错误!未找到引用源。满足错误!未找到引用源。,
- 已知两点,则以为直径的圆的标准方程为___________________。
- 17、一种意思,可以形象表达,也可以抽象表达,不同的表达有不同的效果。请仿照示例,根据要求,在下列横线处填写出相应内容。
- 如图所示的电路中,电源电压为 3V,R 为定值电阻,灯 L 标有“6V 3W ”的字样,灯 L 的电阻不随温度变化。闭合
- 在△ABC中,,则△ABC的最大内角的度数是
- 图1表示植物生长素与其对植物生长的促进作用和关系,请据图回答下列问题: ⑴曲线OH段说明
- _____ your mother_____ a watch? A. Do haven’t B. Do has
- (本题10分) A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A元素的原子只有一个电子层,又知A与C、B与
- 二战前在欧、亚两个战争策源地形成的背景中,德国不同于日本的是( )A.受到世界经济危机的严重冲击 B.
- 士曾经是底层贵族,到了春秋战国时期逐渐由武士而蜕化成了文士,他们中不少人授徒讲学、著书立说、互相辩驳,并且成为当时推进社
- ---I must be off now, or it will be too late to see Tom.
- 作为社区养老保障的一项重要内容,“老年餐桌”已经覆盖到北京市2600多个社区。下面是对三位老人的一段采访记录,请你从中概
 NH
NH  +OH-
+OH- =BaSO4↓;
=BaSO4↓; +OH-=CO
+OH-=CO  +H2O
+H2O


