第二章 开发海水中的卤素资源 知识点题库
实验方法:将适量新制氯水加入到20mL富含溴离子的海水中(海水可以用01mol·L-1的溴化钠溶液代替),把溴置换出来
-
(1) 氯水中的氯气作 剂,涉及反应的离子方程式为.
-
(2) 得到的单质溴可以用有机溶剂在 (仪器)中实现萃取富集。
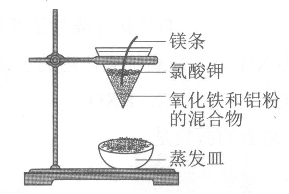
①KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;1∶6
②Fe2O3+2Al  Al2O3+2Fe;1∶2
Al2O3+2Fe;1∶2
③SiO2+3C  SiC(硅为+4价)+2CO↑;1∶2
SiC(硅为+4价)+2CO↑;1∶2
④3NO2+H2O=2HNO3+NO;2∶1
________Na2S+_________Na2SO3+________H2SO4→_______Na2SO4+_______S↓+______H2O
-
(1) 配平上述化学方程式,标出电子转移的方向和数目。
-
(2) 反应中被氧化的元素是。
-
(3) 反应中氧化产物和还原产物物质的量之比为。
-
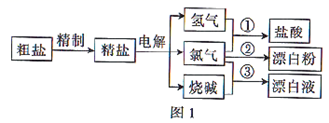
(1) 粗盐中含有
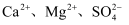 等杂质离子,欲用
等杂质离子,欲用 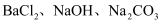 、盐酸进行精制,则这些试剂的加入顺序依次为
、盐酸进行精制,则这些试剂的加入顺序依次为  、、、。
、、、。
-
(2) 工业中制取漂白粉时是将氯气通入(填“澄清石灰水”或“石灰乳”)中,理由是。
-
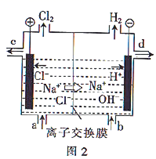
(3) 图2为离子交换膜法电解食盐水的示意图,离子交换膜的作用为、。
-
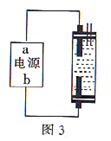
(4) 某化学课外小组用图3所示的简易装置制取“84”消毒液,则a为电源的极,阳极上的电极反应式为,生成次氯酸钠的离子方程式为。
 的绿色方法,原理如图所示。已知:
的绿色方法,原理如图所示。已知: 
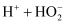 ,
, 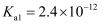 。下列说法错误的是( )
。下列说法错误的是( ) 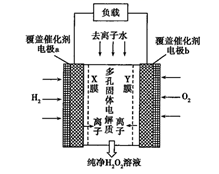
 ,理论上需消耗标准状况下
,理论上需消耗标准状况下 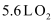 D . b极上的电极反应式为
D . b极上的电极反应式为 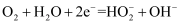
-
(1) 0.5molCH4的质量是 g ,在标准状况下的体积是L ,含 个氢原子,电子数是个。
-
(2) 71gNa2SO4 含有
 mol,完全溶于水,配成2 L溶液,则所得溶液中Na+的物质的量浓度为
mol,完全溶于水,配成2 L溶液,则所得溶液中Na+的物质的量浓度为
已知:
化学式 | Ag2Se | AgCl |
Ksp(常温) | 2.0×10-64 | 1.8×10-10 |
-
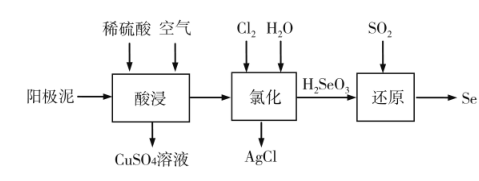
(1) 酸浸过程,通入稀硫酸和空气的目的是。
-
(2) “氯化”过程中发生如下转化:
①Se转化为H2SeO3 , 化学方程式为。
②Ag2Se转化为AgCl,从化学平衡的角度解释原因。
-
(3) ①“还原”过程中发生反应的化学方程式为。
②Cl2、SO2、H2SeO3氧化性由强到弱的顺序为。
-
(4) 滴定法测定CuSO4溶液的浓度,其基本原理为:
第一步:2Cu2++4I-=2CuI↓+I2。
第二步:2
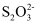 (无色)+I2=
(无色)+I2=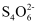 (无色)+2I-
(无色)+2I-①由此可知滴定所用的指示剂为。
②已知CuSO4溶液体积为25mL,滴定至终点时消耗cmol·L-1Na2S2O3溶液VmL,则CuSO4溶液的物质的量浓度为mol·L-1。
③若使用的KI溶液过量,对滴定结果的影响是(填“偏大”或“偏小”或“不影响”)。
-
(1) 物理吸附法
用活性炭负载纳米二氧化钛吸附水中的砷,纳米二氧化钛投加量对活性炭去除砷效果如图1所示:
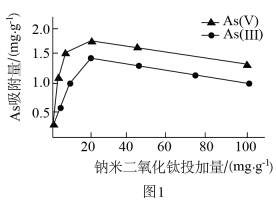
①纳米二氧化钛投加量为时,砷的吸附量可达最大。
②未加二氧化钛时就有一定的吸附砷的能力,可能的原因是。
③若要提高废水中As(III)的去除率,可采取的措施。
-
(2) 化学氧化法
该方法须将废水中的As(III)用空气或铁离子氧化为As(V),然后再去除,为了探究As(III)被哪种氧化剂氧化,设计如下实验:取含As(III)废水,在pH分别为1~10条件下反应1h后,过滤,测定滤液中三价铁和二价铁的含量,得出不同pH下三价铁和二价铁的浓度随pH变化如图2所示:
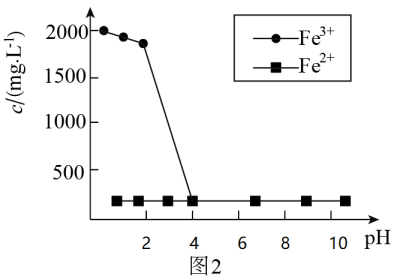
①pH在3~4时Fe3+浓度变化的主要原因为。
②由实验可知废水中的As(III)主要被氧化为As(V),理由为。
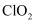 )是国际上公认的安全、无毒的绿色消毒剂,对酸性污水中的
)是国际上公认的安全、无毒的绿色消毒剂,对酸性污水中的 有明显的去除效果,其反应原理为:
有明显的去除效果,其反应原理为: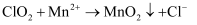 (部分反应物和产物省略、未配平),工业上可用
(部分反应物和产物省略、未配平),工业上可用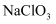 制取
制取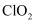 , 化学方程式如下:
, 化学方程式如下: 。有关反应:
。有关反应: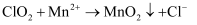 (部分反应物和产物省略、未配平)的说法正确的是( )
(部分反应物和产物省略、未配平)的说法正确的是( )
 的污水,需要8.96L
的污水,需要8.96L 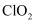 B . 该反应中氧化剂和还原剂的物质的量之比为2:5
C . 工业上用更为廉价的
B . 该反应中氧化剂和还原剂的物质的量之比为2:5
C . 工业上用更为廉价的 代替
代替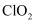 去除
去除 效率更高
D . 利用该原理处理含
效率更高
D . 利用该原理处理含 的污水后溶液的pH升高
的污水后溶液的pH升高
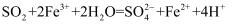 ;②
;② , 下列有关说法错误的是( )
, 下列有关说法错误的是( )
 B . K2Cr2O7能将Na2SO3还原成Na2SO4
C . 每有1mol K2Cr2O7参加反应,转移电子的数目为6NA
D . 若标况下有6.72LSO2参加反应,则最终消耗0.1mol K2Cr2O4
B . K2Cr2O7能将Na2SO3还原成Na2SO4
C . 每有1mol K2Cr2O7参加反应,转移电子的数目为6NA
D . 若标况下有6.72LSO2参加反应,则最终消耗0.1mol K2Cr2O4
- Gateway Academy Pre-Sessional Courses Our pre-sessionalcours
- 细胞分化与细胞增殖的主要不同是() A.细胞数量增多 B.细胞的形态、结构相同 C.细胞在生理功能上相似 D.相同细胞的
- 下列关于哲学的说法中,正确的是 A.哲学是自然科学和社会科学的总和 B.哲学是关于世界观的学说,是具体知识的概括和总结
- 钢铁工业是四川省攀枝花市的主导工业部门。甲图是“攀枝花市及其附近地区简图”,乙图是设想的“以攀枝花钢铁工业为基础的生产流
- We walked as fast as we could _____ to catch the train.A. ho
- 已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1kJ·mol-1; HCl(aq)与NaOH(aq)反应的Δ
- 如图6-7-6所示,原长为L的轻质弹簧,劲度系数为k,一端系在圆盘的中心O,另一端系一质量为m的金属球,不计摩擦,当盘和
- 以专题的形式统揽历史阶段是学习历史的一个好方法。下列历史阶段可包含在专题“封建国家的分裂和民族大融合”之中的是() A.
- I usually_______ books in the morning. A.look B.read
- 2009年是达尔文的《物种起源》发表150周年,也是达尔文诞辰200周年。达尔文的《物种起源》发表后,引起了宗教势力的强
- .求值:tan 20°+tan40°+tan 20°tan 40°=.
- 2007年元月,在湖北发生了一起危险化学品泄漏事故,造成上百人中毒,1人死亡。有机物a是一种重要的化工原料,在有机合成中
- 改革开放之后,我国人民的物质生活水平有了大幅度提高。人们要求富而乐、福而安、福而康,在富裕的同时获得快乐、安定、健康,体
- 等腰三角形的一内角等于50°,则其它两个内角各为_______________________.
- 若用化学抑制剂抑制肿瘤细胞的DNA的复制,这些细胞就停留在: A.分裂间期
- 右图是二战后某一国际组织召开的一次重要会议的场景,该组织产生的影响有分析材料,“大梦唤醒”是在1894年甲午战争中国战败
- 阅读下面的材料,按要求作文。 近年来,中国游客在国外旅游时的种种缺少公德的表现,引爆关于国人素质低的讨论。以90后为代表
- 跨入青春的门槛,追求远大的理想,走进美丽的家园,享受爱心的阳光,触摸科学与时尚……生活是多么精彩!请以\'生活因____
- 计算(ab2)3的结果是() A. ab5 B. ab6
- 小乐想利用两块电流表和阻值已知的电阻R0测量电阻RX的阻值。小乐选择了满足实验要求的电源、电流表A1和A2,并连接了部分



