第二章 开发海水中的卤素资源 知识点题库
用5.96 g NaClO固体配成100 mL溶液,向其中加入0.02 mol Na2Sx , 恰好完全反应生成NaCl和Na2SO4。
-
(1) NaClO溶液浓度为。
-
(2) 化学式Na2Sx中x的值为。
化学与生活、生产、社会、环境密切相关,下列说法不正确的是( )
A . 小型游泳池通常使用次氯酸钠而非氯气来消毒池水
B . 在食品袋中放入装有硅胶、铁粉的透气小袋,可防止食物受潮、氧化变质
C . 为使以面粉为原料的面包松软可口,通常用小苏打做发泡剂
D . 为提高农作物的产量和质量,应大量使用化肥和农药
下列实验得到的结论正确的是( )
A . FeCl2溶液中滴入KSCN溶液,再滴加大量H2O2 , 溶液出现血红色,后逐渐褪去,可以推断溶液中的Fe2+先转变成Fe3+ , 然后又转变成Fe2+
B . 金属钠与浓盐酸反应比金属钠与水反应速率更慢,可以推断浓盐酸中c(H+)较小
C . Na2SO3溶液中加入过量盐酸,没有气体生成,可以推断盐酸的酸性比H2SO3弱
D . 在100mL沸水中加入10gNaHCO3固体,产生大量的气泡,可以推断反应后溶液的碱性比10gNaHCO3固体溶于100mL冷水中形成的溶液的碱性强
高锰酸钾是中学常用化学试剂,工业上常以软锰矿(主要成分是MnO2)为原料进行制备,主要工艺流程如下图:

已知:3K2MnO4+2H3PO4═2KMnO4+MnO2↓+2K2HPO4+2H2O
| 物质 | KMnO4 | K2HPO4 | K2SO4 | CH3COOK | KCl | K2CO3 |
| 293K溶解度/g | 6.4 | 150 | 11.1 | 217 | 34 | 111 |
-
(1) 原料高温煅烧时选用铁坩埚和铁棒,理由是。
-
(2) ①中每生成1molK2MnO4时电子转移2mol,写出化学反应方程式。
-
(3) 从反应机理和产物分离角度考虑,③可用磷酸,也可用下列________试剂。A . 醋酸 B . 盐酸 C . 硫酸 D . CO2
-
(4) 下列描述错误的是_________。A . 操作⑤中蒸发至大量晶体析出再冷却晶体,趁热过滤 B . 抽滤时布氏漏斗中选用大小略小于漏斗内径且盖住全部小孔的滤纸 C . 可用无水乙醇洗涤产品提高纯度 D . KMnO4晶体的烘干温度过高会降低产率
-
(5) 粗产品的洗涤步骤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复2~3次。
请选出正确的操作并排序。(操作可重复使用)
-
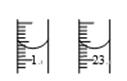
(6) 高锰酸钾产品的纯度测定:准确称取0.7900g产品,配成250mL溶液,量取25.00mL于锥形瓶中,用0.1000mol•L﹣1(NH4)2Fe(SO4)2标准溶液进行滴定,滴定终点的现象。滴定前和滴定后的液面见下图。计算出高锰酸钾的纯度为。
化学反应方程式是化学学习的基本工具,本学期在化学反应速率与化学平衡章节学过几个重要的方程式,请你按要求写出:
-
(1) 硫代硫酸钠与稀硫酸溶液反应的离子方程式:。
-
(2) 在重铬酸钾的硫酸溶液中的Cr2O72-与CrO42-之间转化的离子方程式:。
①Cu丝 ②Cl2 ③Al2(SO4)3溶液 ④蔗糖 ⑤浓硝酸⑥Ca(OH)2⑦NH4Cl⑧CO2 ⑨氨水
请用以上相应的数字编号和化学用语回答问题:
-
(1) 属于电解质的是;属于非电解质的是.
-
(2) 实验室制取氨气的化学反应方程式.
-
(3) 工业制漂白粉的化学反应方程式.
-
(4) 实验室制Al(OH)3的离子方程式
-
(5) ①和⑤的化学方程式并用双线桥标出电子转移.
在全国人民众志成城抗击新冠病毒期间,使用的“84消毒液”的主要有效成分是( )
A . NaOH
B . NaCl
C . NaClO
D . Na2CO3
葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通常以酒样中SO2的量计),某研究小组设计了如下实验(已知还原性:SO32->I->Cl-)。下列说法错误的是( )
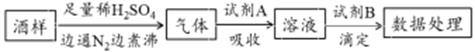
A . 葡萄酒中加亚硫酸盐的主要目的是防止氧化,利用了亚硫酸盐的还原性
B . 通入N2和煮沸的目的是为了将产生的气体从溶液中全部赶出
C . 若试剂A选择氯水,则试剂B可选择NaOH标准液
D . 若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I2标准液
已知下列几个反应的化学方程式:① 2KI+Cl2=2KCl+I2、② 2FeCl2+Cl2=2FeCl3、③ 2FeCl3+2HI=2FeCl2+I2+2HCl,下列有关物质的氧化性的强弱排列顺序中正确的是( )
A . Cl2>Fe3+>I2
B . Cl2>I2>Fe3+
C . Fe3+>Cl2>I2
D . Fe3+>I2>Cl2
氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
-
(1) 火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。
其中被氧化的元素是,还原产物是。
-
(2) 实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显价。
②以上反应中的氧化剂为,当有1 mol CuI参与反应时,转移电子mol。
③标明上述反应电子转移的方向和数目。
。
-
(3) 工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8Mn
 +5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O6Mn
 +5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。
反应后煮沸溶液,赶尽SO2 , 剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
Mn
 +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为 mol。
阿伏加德罗常数的值为NA , 下列说法正确的是( )
A . 标准状况下,2.24L苯含有的分子为0.1NA
B . 0.1molFe与足量氯气反应,转移的电子数目为0.2NA
C . 2.8gCO和C2H4混合物中含有的分子数为0.1NA
D . 1molMg2+含有核外电子数为2NA
黑火药在发生爆炸时,有可能发生如下的反应:16KNO3+8C+S8=8K2S+16NO2↑+8CO2↑。
-
(1) 上述反应所涉及元素中,某元素易形成简单阳离子,其离子结构示意图是;某元素原子核外电子中有三个未成对电子,请写出其原子最外层电子排布式;有两种元素最外层电子数相同,请写出其中原子序数较小的元素形成简单离子的电子式;发生氧化反应的元素,其原子核外电子的轨道表示式为。
-
(2) 上述反应中,被还原的元素是,氧化产物是。
-
(3) 请标出上述反应的电子转移方向和数目。
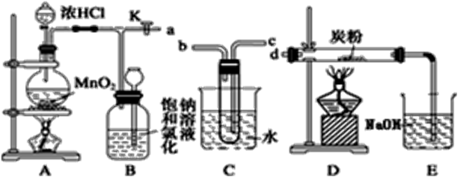
如图是某研究性学习小组设计制取氯气,并以氯气为反应物进行特定反应的装置。
-
(1) 写出A中反应的离子反应方程式:。要将C装置接入B和D之间,正确的接法是:a→→→d。
-
(2) 实验开始时先点燃A处酒精灯,打开旋塞K,让Cl2刚好充满整个装置,再点燃D处酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g)。
D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是,B的作用是。
-
(3) 在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由:。
-
(4) 实验结束后,测得D装置质量减轻1.92g,E中NaOH溶液(足量)增重36.08g,可算出D中反应的氯气转化率为。(转化率=D中参加反应的氯气的量/通入D中氯气总量)
下列反应中,属于氧化还原反应的是( )
①H2+Cl2  2HCl
2HCl
②Al2O3+2NaOH=2NaAlO2+H2O
③2HgO 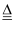 2Hg+O2↑
2Hg+O2↑
④CuO+2HNO3=Cu(NO3)2+H2O
A . ②③
B . ②④
C . ①④
D . ①③
氯气的水溶液称“氯水”,氯水中含有多种分子和离子,因此氯水有多重性质,下列有关新制氯水的说法中错误的是( )
A . 新制氯水呈黄绿色,且有刺激性气味,说明氯水中含有  B . 向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明
B . 向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明  的氧化性强于I2
C . 新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有
的氧化性强于I2
C . 新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有  D . 新制氯水滴到
D . 新制氯水滴到  溶液中,有气体产生,说明氯水中含有
溶液中,有气体产生,说明氯水中含有 
 B . 向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明
B . 向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明  的氧化性强于I2
C . 新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有
的氧化性强于I2
C . 新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有  D . 新制氯水滴到
D . 新制氯水滴到  溶液中,有气体产生,说明氯水中含有
溶液中,有气体产生,说明氯水中含有 
氯酸钾和浓盐酸之间有下列反应: 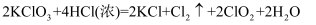 。
。
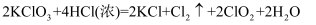 。
。
-
(1) 该反应中发生还原反应的物质是,氧化产物是。
-
(2) 用双线桥标出方程式中的电子得失:
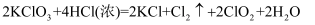
-
(3) 当有0.2mol电子发生转移时,生成的氯气的体积为L(标准状况),被氧化的HCl有mol。
下列实验中的颜色变化与氧化还原反应有关的是( )
A . NO2气体溶于水,气体由红棕色变为无色
B . SO2气体通入品红溶液,溶液由红色变为无色
C . KI溶液滴入AgCl浊液中,沉淀由白色逐渐变为黄色
D . KSCN溶液滴入FeCl3溶液中,溶液由棕黄色变为红色
下列各反应中,氧化反应与还原反应在同种元素中进行的是( )
A . 3Cl2+6NaOH  5NaCl+NaClO3+3H2O
B . 2KMnO4
5NaCl+NaClO3+3H2O
B . 2KMnO4  K2MnO4+MnO2+O2↑
C . 2Mg+CO2
K2MnO4+MnO2+O2↑
C . 2Mg+CO2  2MgO+C
D . 2FeCl2+Cl2=2FeCl3
2MgO+C
D . 2FeCl2+Cl2=2FeCl3
 5NaCl+NaClO3+3H2O
B . 2KMnO4
5NaCl+NaClO3+3H2O
B . 2KMnO4  K2MnO4+MnO2+O2↑
C . 2Mg+CO2
K2MnO4+MnO2+O2↑
C . 2Mg+CO2  2MgO+C
D . 2FeCl2+Cl2=2FeCl3
2MgO+C
D . 2FeCl2+Cl2=2FeCl3
下列变化中,一定要加入适当的还原剂才能实现的是( )
A . CO→CO2
B . HCl→Cl2
C . CaO→CaCO3
D . CuO→Cu
下列实验的颜色变化不涉及氧化还原反应的是( )
A .  遇空气变为红棕色气体
B . 向含
遇空气变为红棕色气体
B . 向含 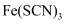 的溶液中加入铁粉,溶液颜色变浅
C . 用
的溶液中加入铁粉,溶液颜色变浅
C . 用 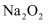 作潜水艇的供氧剂
D . 向
作潜水艇的供氧剂
D . 向 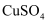 溶液中加入过量氨水,溶液变为深蓝色
溶液中加入过量氨水,溶液变为深蓝色
 遇空气变为红棕色气体
B . 向含
遇空气变为红棕色气体
B . 向含 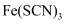 的溶液中加入铁粉,溶液颜色变浅
C . 用
的溶液中加入铁粉,溶液颜色变浅
C . 用 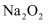 作潜水艇的供氧剂
D . 向
作潜水艇的供氧剂
D . 向 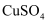 溶液中加入过量氨水,溶液变为深蓝色
溶液中加入过量氨水,溶液变为深蓝色
最近更新
- 如图所示,自动卸货车始终静止在水平地面上,车厢在液压机的作用下,θ角逐渐缓慢增大且货物相对车厢静止的过程中,下列说法不正
- 已知离散型随机变量的分布列如右表.若,,则 __, . 0 1 2
- 2014年3月,李克强总理在十二届全国人大二次会议上作的《政府工作报告》,经代表分组审议并提出修改意见后,在全体会议上获
- 解方程:+1=.
- 在竞赛进入最后阶段,有的运动员会出现血压下降、心率加快、四肢发冷等症状,这是由于随着人体大量出汗而向外排出大量的(
- 下列计算正确的是 ( )
- 气体的温度从27 ℃降低到0 ℃,用热力学温度表示,以下说法正确的是( ) A.气体的温度降低了27 K
- 将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g) +B(g) 2C(g)+2D(g)△H<0
- 化学兴趣小组的同学取10g铜锌合金样品于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7g时,恰好完全反应
- 1912年4月孙中山访察武汉后说:“以南皮(注:南皮即张之洞)造成楚材,颠覆满祚,可谓为不言革命之大革命家。”这表明当时
- She knew what she wanted to say, butwhen she started speaki
- 在图12-3-5所示的图象中,实线是一列简谐横波在某一时刻的图象,经过t=0.2 s后这列波的图象如图中虚线所示,求这列
- 在做凸透镜成像实验时,当蜡烛距凸透镜15cm,在光屏上成放大的像,则下列说法中不正确的是( )A.蜡烛距透镜40
- 乳酸()是人体生理活动的一种代谢产物。以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。 请
- 二氧化氯(ClO2)是一种环保型杀菌消毒剂。在生活中主要用于饮用水的消毒和食品保鲜。用二氧化氯消毒后的水可以直接饮用。
- 已知f(x)=试讨论x→0时,f(x)的极限.
- 在文中横线处填恰当的关联词语,使上下文连贯起来。(3分)我不敢妄图与我们当代最伟大的作家比高下, ① 我也不远追
- 下列说法正确的是( )A.运动电荷在磁感应强度不为零的地方,一定受到洛伦兹力的作用B.运动电荷在某处不受洛伦兹力的
- 某学生想制作一种家用环保型消毒液发生器,用石墨做电极电解饱 和NaCl溶液。通电时,为使Cl2被完全吸收,制得有较强杀菌
- 下面是“观察种子的结构”实验示意图,请据图回答问题:(1)在图一所示的玉米种子的剖面上滴一滴碘液,变成蓝色的部分是[



