第二单元 生产生活中的含氮化合物 知识点题库
-
(1) PbO2可由NaClO氧化Pb(NO3)2溶液得到.
①Pb(NO3)2被氧化为PbO2的离子方程式为.
②Pb(NO3)2溶液中通入H2S发生Pb2+(aq)+H2S(aq)⇌PbS(s)+2H+(aq),直至平衡,该反应的平衡常数为K=1已知:Ksp(PbS)=3.55×10﹣28;H2S电离常数Ka1=1.3×10﹣7 , Ka2=7.1×10﹣15].
-
(2) 制备碱式碳酸铅的实验步骤如图1:
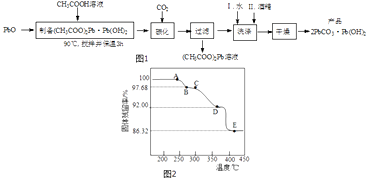
①“碳化”时,发生反应的化学方程式为.
②“洗涤”时,经水洗涤后再用酒精洗涤的目的是.
-
(3) 为确定2PbCO3•Pb(OH)2(相对式量:775)的热分解过程,进行如下实验:称取一定量(2)实验制得的样品放在热重分析仪中,在氩气流中热分解,测得样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如图2所示.
①A→B过程中,从体系中逸出的分解产物(化合物)为(填化学式);C→D过程中,从体系中逸出的分解产物(化合物)为(填化学式).
②根据图中实验数据,计算并确定E点残留固体的化学式(写出计算过程).
选项 | 实验操作 | 现象 | 结论 |
A | 某钾盐晶体中滴入浓盐酸,产生的气体通入品红溶液 | 品红溶液褪色 | 产生的气体一定是SO2 |
B | 用磁铁吸引氧化铁与铝粉发生铝热反应后的黑色产物 | 能被磁铁吸引 | 黑色熔化物中含铁、四氧化三铁中的1种或2种 |
C | 向某硫酸盐溶液中滴入酸性H2O2溶液,再滴入KSCN溶液 | 溶液变为红色 | 该硫酸盐一定为FeSO4 |
D | 某品牌加碘食盐的溶液中,加入淀粉,并通入NO2 | 溶液变为蓝色 | 该加碘食盐中碘的存在形式为IO3﹣ |
选项 | 实验事实 | 理论解释 |
A | 深蓝色的[Cu(NH3)4]SO4溶液中加入乙醇析出晶体 | 乙醇增强了溶剂的极性 |
B | 用KSCN检验溶液中的Fe3+ | Fe3+遇SCN﹣生成血红色沉淀 |
C | CH4熔点低于CO2 | 碳氢键比碳氧键的键长短、键能大 |
D | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
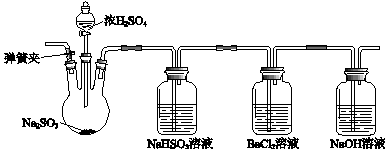
ⅠSO2不能与BaCl2反应;ⅡBaSO3是白色难溶于水的物质,但可溶解于盐酸.
-
(1) 该实验制备SO2的化学方程式是.
-
(2) BaCl2溶液中出现了不溶于稀盐酸的白色沉淀,该沉淀可能是.
-
(3) 甲同学认为出现白色沉淀是由于装置中存在O2 , 排除干扰的方法是.
-
(4) 按照(3)中改进后的方法重新进行实验,现象是,实验结论与文献一致.
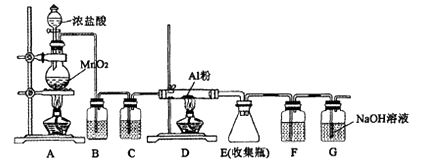
| 步骤 | | | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色 气泡后,迅速停止 | Fe、Cu接触后,其表面 均产生红棕色气泡 |
下列说法中,错误的是( )
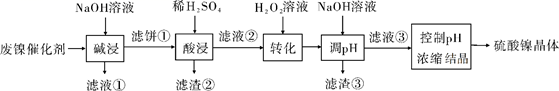
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
|
金属离子 |
Ni2+ |
Al3+ |
Fe3+ |
Fe2+ |
|
开始沉淀时(c=0.01 mol·L−1)的pH 沉淀完全时(c=1.0×10−5 mol·L−1)的pH |
7.2 8.7 |
3.7 4.7 |
2.2 3.2 |
7.5 9.0 |
回答下列问题:
-
(1) “碱浸”中NaOH的两个作用分别是。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式。
-
(2) “滤液②”中含有的金属离子是。
-
(3) “转化”中可替代H2O2的物质是。若工艺流程改为先“调pH”后“转化”,即
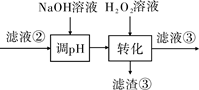
“滤液③”中可能含有的杂质离子为。
-
(4) 利用上述表格数据,计算Ni(OH)2的Ksp=(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L−1 , 则“调pH”应控制的pH范围是。
-
(5) 硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式。
-
(6) 将分离出硫酸镍晶体后的母液收集、循环使用,其意义是。
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 5.4 |
| 沉淀完全的pH | 5.0 | 3.7 | 9.7 | 8.0 |
-
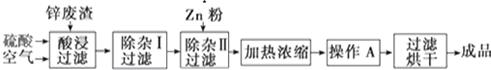
(1) 上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有
-
(2) 在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是;为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液pH范围是;为控制上述pH范围可选择加入的试剂或药品是。
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
-
(3) 在“除杂Ⅱ”步骤中,加入Zn粉的作用是。“操作A”的名称是。
-
(4) 常温下,已知Ksp〔Cu(OH)2〕=2.0×10-20 , 某CuSO4溶液里c(Cu2+)=2.0×10-4mol/L,如果要生成 Cu(OH)2沉淀,则应调整溶液pH大于 。

甲:向反应混合液中滴入稀硝酸中和NaOH 溶液,然后滴入AgNO3溶液,若有淡黄色沉淀生成,则可证明发生了消去反应。
乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。
丙:向反应混合液中滴入酸性FeCl3溶液,若溶液颜色变为紫色,则可证明发生了水解反应。
其中正确的是( )
请参照下表给出的数据填空:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 4 |
-
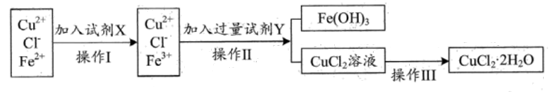
(1) 加入试剂X的目的是 。
-
(2) 适合本实验的X物质可以是(填字母)。
A KMnO4 B H2O2 C NaClO D Cl2
-
(3) 加入试剂Y的目的是调节溶液的pH,试剂Y的化学式为,根据题给信息,溶液的pH范围应为。
-
(4) 当c(Fe3+)=1.0×10-5mol•L-1时,可以认为沉淀完全,则Fe(OH)3的Ksp= 。
-
(5) 实验室在配制CuCl2溶液时需加入少许(填物质名称),理由是(用化学用语和必要的文字回答)。
-
(6) 操作III是。
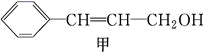
![]()
-
(1) 写出一种能与甲反应(不需要其他条件)但不能与乙反应的试剂的名称: ;1 mol乙最多可与 mol H2发生加成反应。
-
(2) 甲有多种同分异构体,其中满足下列条件的同分异构体有 种
a分子中有苯环:
b能发生银镜反应:
c.核磁共振氢谱显示有4组峰,且峰面积之比为1:1:2:6
-
(3) 由甲转化为乙的过程为(已略去部分产物):
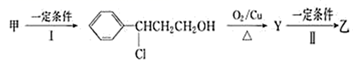
①反应I的反应类型为,设计步骤I的目的是 。
②写出反应II的化学方程式:。
③乙在碱性( NaOH)条件下与新制Cu(OH)2悬浊液反应的化学方程式为 。
 闪电
B .
闪电
B .  合成氨车间
C .
合成氨车间
C .  绿色植物光合作用
绿色植物光合作用
选项 | 操作或做法 | 目的 |
A | 溴乙烷和NaOH乙醇溶液共热,所产生气体直接通入酸性高锰酸钾溶液中,溶液褪色 | 检验反应生成乙烯 |
B | 将SO2通入溴水溶液中,溶液褪色 | 检验SO2的漂白性 |
C | 在待测液中先用稀硝酸酸化,再滴加AgNO3溶液,生成白色沉淀 | 检验溶液中是否含有Cl- |
D | 向丙烯醛溶液中滴加溴水,溶液褪色 | 检验丙烯醛中是否含有碳碳双键 |
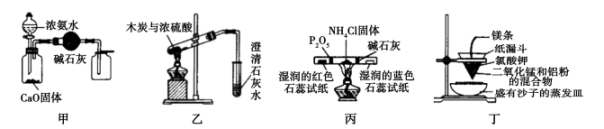
 的性质进行下列实验,其中能达到实验目的的是( )
的性质进行下列实验,其中能达到实验目的的是( )
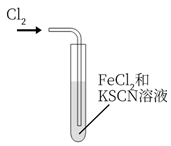 探究
探究 的氧化性
B .
的氧化性
B . 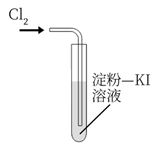 探究
探究 的漂白性
C .
的漂白性
C . 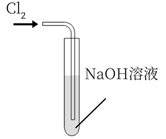 模拟工业制漂白粉
D .
模拟工业制漂白粉
D . 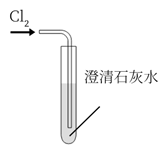
 尾气处理
尾气处理
- .下列事故的处理方法中,不正确的是() A.正在使用的电器着火,立即用水浇灭 B.燃着的酒精灯不慎碰倒,立即用湿布盖灭
- The missingchildren haven’t been found yet. Something terri
- .Fifty-two miners were killed in the accident. ______ , thir
- 下列叙述中,能说明某化合物一定是弱电解质的是( )A.该化合物水溶液和熔融状态下均不导电B.该化合物饱和溶液导电能
- .阅读下面一段话,按要求作答。(6分) “地下看西安,地上看泉州。”在泉州这片古老而神奇的土地上,名胜古迹星罗棋
- 下列说法正确的是( )A.话筒是一种常用的声传感器,其作用是将电信号转换为声信号B.电熨斗能够自动控制温度的原因
- 阅读下列关于苏格拉底之死的材料雅典人口总数雅典公民总数陪审、审判人员及产生方式表决形式程序罪名陪审员审判员产生方式约40
- 为纪念编制了第一个元素周期表的俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔。该元素最稳定的一种原子可
- 如图所示的四幅图中,能够增大压强的是:
- 下图是二战后苏联某画家创作的一幅漫画,该漫画( )A.反映冷战时期意识形态对立 B.揭示出欧洲援助计划
- 仿照“成熟”的句式,以“成功”为陈述对象写一句话。 成熟是一种明亮而不刺眼的光辉,一种圆润而不腻耳的声响,一种不
- 20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60 (足球烯,分子中含
- 已知函数f(x)=2x-2-x,数列{an}满足f(log2an)=-2n. (1)求数列{an}的通项公式; (2)求
- 图是一个环境温度监控电路,R1为定值电阻,R2为用半导体材料制成的热敏电阻(电阻随温度的升高而变小)。当环境温度升高时,
- .World Expo 2010 Shanghai China, a grand-scale global event,
- ()2. 如图所示,某同学用一个闭合线圈穿入蹄形磁铁由1位置经2位置到3位置,最后从下方S极拉出,则在这一过程中,线圈的
- 反比例函数图象的对称轴的条数是 ( )A.0
- 已知二次函数y=ax2+bx-3的图象经过点A(2,-3),B(-1,0). 求二次函数的解析式;
- 从2008年起,山西省政府开始推进煤矿企业的兼并重组整合,到2009年底,通过重组整合,山西矿井数量由以往的2600座减
- 减少空气污染的措施是①实验室使用排风电扇;②开发新能源;③冶金工厂产生的工业废气经净化处理后,才能排放到空气中;④向煤中





