专题4 硫、氮和可持续发展 知识点题库
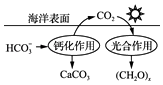
①目前我国空气质量检测体系包括:PM2.5、SO2、NO2、O3、CO等指标.其中被认为是引起雾霾天气的元凶;会引起硫酸型酸雨的气体为.
②NH3催化还原氮氧化合物转化为无污染物质是目前应用最广泛的烟气氮氧化合物脱除技术,写出NH3催化还原NO2反应的化学方程式.
③减少CO2的排放对于环境保护具有重要意义.在海洋碳循环中,可通 过图3所示的途径固碳.写出钙化作用的离子方程式:.
选项 | 实验操作 | 实验目的或结论 |
A | 向0.1mol·L-1 Na2SO4溶液中滴加BaCl2溶液至不再产生沉淀,再滴加0.1mol/L Na2CO3无现象 | 证明Ksp(BaSO4)<Ksp(BaCO3) |
B | 向盛有KI3溶液的两试管中分别滴加淀粉溶液、AgNO3溶液,前者变蓝色,后者有黄色沉淀 | 证明KI3溶液中存在:I3- |
C | 向NaAlO2溶液中持续通入气体,先产生白色沉淀,后沉淀完全溶解 | 该气体可能是CO2 |
D | 在Fe(NO3)2溶液中滴加硫酸酸化的双氧水溶液,溶液变黄色 | 证明氧化性:H2O2>Fe3+ |
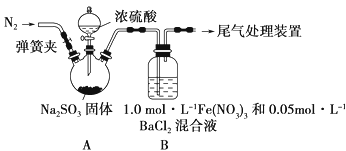
已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1,请回答下列问题:
-
(1) 装置A中反应的化学方程式是
-
(2) 为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是
-
(3) 装置B中产生了白色沉淀,其成分是 ,说明SO2具有 性。
-
(4) 分析B中产生白色沉淀的原因:
猜想1:;
猜想2:SO2与Fe3+反应;
猜想3:在酸性条件下SO2与NO3-反应;
①按猜想2,装置B中反应的离子方程式是
②按猜想3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是 (填字母)。
a.0.1 mol·L-1硝酸钠溶液
b.1.5 mol·L-1Fe(NO3)2溶液
c.6.0 mol·L-1 NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 充分吸收了Na2SiO3饱和溶液的小 木条,沥干后放在酒精灯外焰加热 | 小木条不燃烧 | Na2SiO3可作 防火剂 |
| B | 将H2在充满Cl2的集气瓶中燃烧 | 集气瓶口上方 有白烟生成 | H2、Cl2化合 生成HCl |
| C | 将FeCl2加入酸性高锰酸钾溶液中 | 溶液紫色褪去 | FeCl2具有漂 白性 |
| D | 除去表面氧化膜的铝箔,在酒精灯 上充分加热 | 铝不能滴落下 来 | 铝熔点高,没 能熔化 |
-
(1) 用如图装置制备纯净的CO2
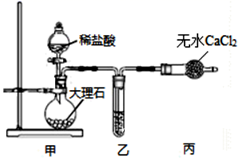
①甲装置中盛放稀盐酸的仪器名称是,乙装置中应加入的试剂是。
②装置甲中反应的离子方程式为。
-
(2) 按照下面的装置图进行实验(夹持装置略)。
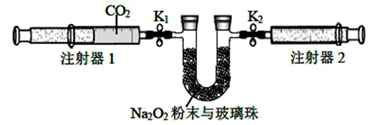
①先组装仪器,然后,再用注射器1抽取100 mL纯净的CO2 , 将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2 , 向右推动注射器1的活塞,可观察到的现象是。
③实验过程中,需缓慢推入CO2 , 其目的是,反应的化学方程式为。
-
(3) 实验结束后,当注射器1的活塞推到底时,测得注射器2中气体体积为65 mL,则反应消耗CO2的体积是。
 )是无公害型冷却水系统的金属级蚀剂,工业上利用钼精矿(主要成分是不溶于水的
)是无公害型冷却水系统的金属级蚀剂,工业上利用钼精矿(主要成分是不溶于水的  ,含少量
,含少量 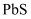 等)制备钼酸钠的工艺如图所示。
等)制备钼酸钠的工艺如图所示。 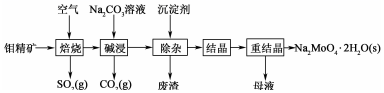
回答下列问题:
-
(1) ①
 中钼元素的化合价是;
中钼元素的化合价是; ②在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶进入,这样处理的目的是。
-
(2) “焙烧”时
 转化为
转化为 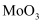 ,写出该反应的化学方程式:。
,写出该反应的化学方程式:。
-
(3) “碱浸”所得
 ,溶液中含
,溶液中含  杂质,其中
杂质,其中 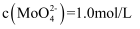 ,
, 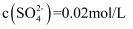 ,在结晶前需加入
,在结晶前需加入 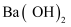 固体以除去溶液中的
固体以除去溶液中的  。当
。当 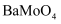 开始沉淀时,
开始沉淀时,  的去除率是。(
的去除率是。(  ,溶液体积变化可忽略)
,溶液体积变化可忽略)
-
(4) “除杂”过程中加入的除杂剂是
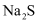 ,则废渣的化学式为。
,则废渣的化学式为。
-
(5) 钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在不同介质中的腐蚀速率实验结果如下图:
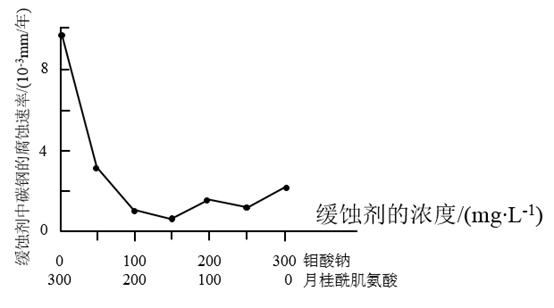
要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为。
-
(6) 另一种利用钼精矿制备钼酸钠的工艺流程中,直接向粉碎后的钼精矿中加入
 溶液和
溶液和 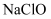 溶液来得到钼酸钠,则得到钼酸钠溶液的离子方程式为。
溶液来得到钼酸钠,则得到钼酸钠溶液的离子方程式为。
 甲基丙烷和异丁烷互为同系物,化学性质相似
C . 甲酸甲酯和乙酸互为同分异构体,化学性质不同
D . 富勒烯与金刚石互为同素异形体,物理性质相似
甲基丙烷和异丁烷互为同系物,化学性质相似
C . 甲酸甲酯和乙酸互为同分异构体,化学性质不同
D . 富勒烯与金刚石互为同素异形体,物理性质相似
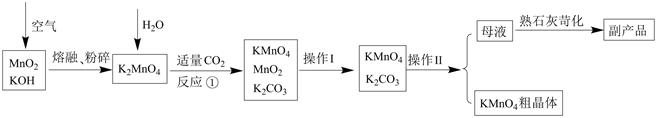
回答下列问题:
-
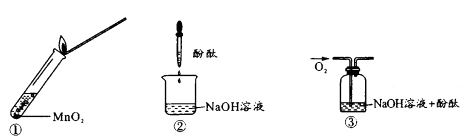
(1) 写出MnO2、KOH与空气共熔发生反应的化学方程式。
-
(2) 反应①中氧化产物与还原产物的物质的量之比为。假设无其他副反应发生,该步反应K2MnO4的最大理论转化率为%(保留一位小数)。
-
(3) 操作I为。
-
(4) 已知有关物质在不同温度(单位:℃)下的溶解度(单位:g/100g水中)如下图:
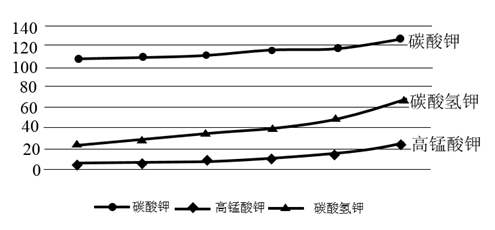
据图推断操作II最好采用。反应①中若CO2通入过量造成的影响是。
-
(5) 上述流程中可以循环利用的物质有。
-
(6) 由于直接歧化制备高锰酸钾的产率不高,且后续分离纯化步骤较多,目前工业上较多采用电解K2MnO4水溶液法制备,试写出该电解过程总反应的化学方程式。
| 选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 | 装置 |
| A | 氨水 | CaO | 无 | 制取并收集氨气 | |
| B | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 制备纯净的Cl2 | |
| C | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 比较酸性强弱: H2CO3>H2SiO3 | |
| D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | 验证SO2具有还原性 |
 )溶液来处理。工业上制备过硫酸钠的原理如下:
)溶液来处理。工业上制备过硫酸钠的原理如下: 主反应: 
副反应: 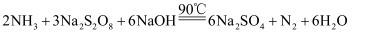
(制备  )
)
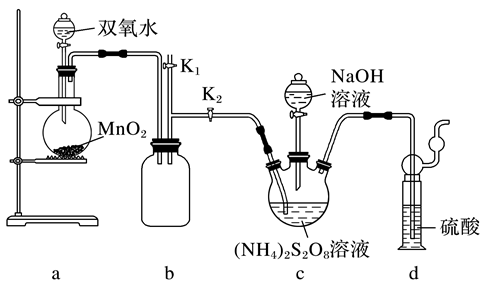
-
(1) 检查装置a气密性的方法:用止水夹夹住a、b之间的橡皮管,向分液漏斗中加水,,证明装置a气密性良好;装置a中产生的气体需要持续通入装置c中的原因是(答2点)、。
-
(2) 装置c中盛放(NH4)2S2O8溶液的仪器名称是;图中还需补充装置。
(测氰化钠的含量)
已知:①废水中氰化钠的最高排放标准为0.50 mg/L。
②
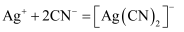 ,
, 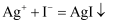 ,AgI呈黄色,
,AgI呈黄色, 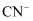 优先与
优先与 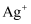 发生反应。
发生反应。实验如下:取1 L处理后的NaCN废水,浓缩为10.00 mL置于锥形瓶中,并滴加几滴KI溶液作指示剂,用0.0012 mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为3.75 mL。
-
(3) 滴定终点的现象是。
-
(4) 若用双氧水处理NaCN后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的化学方程式是。
 )是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是
)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是  ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。 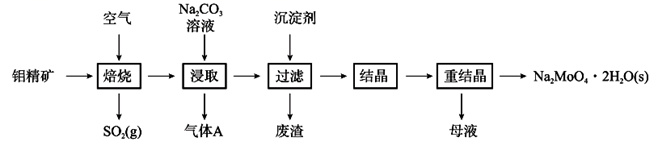
-
(1)
 中钼元素的化合价是。
中钼元素的化合价是。
-
(2) “浸取”时得到的气体A的电子式为;
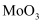 与
与  发生反应的离子方程式为。
发生反应的离子方程式为。
-
(3) 向滤液中加入沉淀剂
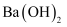 固体以除去
固体以除去  。若滤液中
。若滤液中 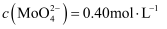 ,
, 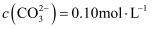 ,当
,当 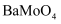 开始沉淀时
开始沉淀时  的去除率是%[已知:
的去除率是%[已知:  ,
,  ]。
]。
-
(4) 钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示:
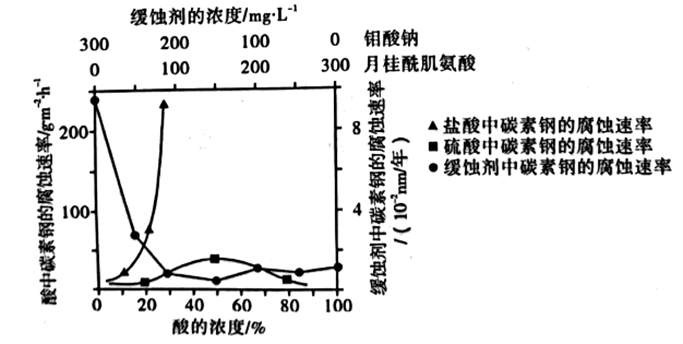
①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为。
②碳钢在盐酸中的腐蚀速率比硫酸快得多,其原因可能是;硫酸浓度大于50%,碳钢的腐蚀速率下降,原因可能是。
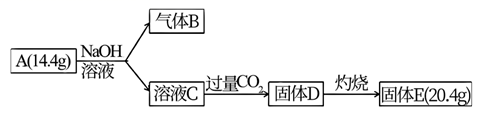
已知∶标准状况下,气体B的密度是氢气的8倍;固体E既溶于NaOH溶液又可溶于稀硫酸。
请回答∶
-
(1) B的化学式是
-
(2) 组成A的元素有
-
(3) 请写出 A 与 NaOH溶液反应的化学方程式
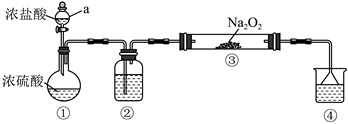
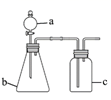
请回答:
-
(1) 装置①中仪器a的名称是。
-
(2) 装置②的作用是。
-
(3) 装置③中反应的化学方程式是。
-
(4) 该小组同学想进一步通过实验验证装置③中产生的黄绿色气体中含有氯气,下列方案可行的是_________。A . 将气体通入AgNO3溶液中,观察有无白色沉淀产生 B . 将气体通入放有湿润的淀粉-KI试纸的洗气瓶,观察试纸有无变蓝 C . 将气体通入NaHCO3溶液中,观察有无气泡产生 D . 将气体通入放有湿润的有色布条的洗气瓶,观察布条有无褪色
-
(5) 装置④的作用是尾气处理,下列试剂可以选用的是______。A . 饱和食盐水 B . 蒸馏水 C . NaOH溶液 D . 饱和Na2CO3溶液
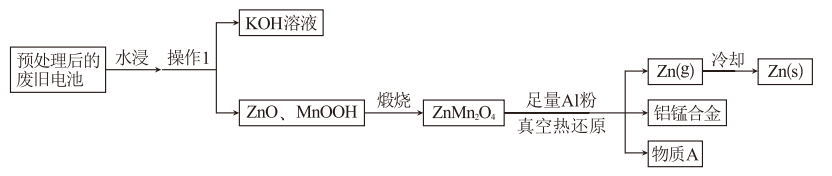
-
(1) “操作1”的名称为。
-
(2)
 中
中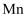 元素的化合价为。
元素的化合价为。
-
(3) “煅烧”得到
 的化学方程式为。
的化学方程式为。
-
(4) 物质
 的主要成分为(填化学式)。
的主要成分为(填化学式)。
-
(5) 预处理后的废旧电池质量为
 , 其中
, 其中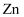 元素的质量分数为
元素的质量分数为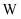 , 回收得到
, 回收得到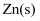 的质量为
的质量为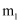 , 则
, 则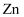 元素的回收率为(回收率
元素的回收率为(回收率 )。
)。
-
(6) 氢氧燃料电池选用
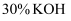 溶液作为电解质溶液,负极的电极反应式为。
溶液作为电解质溶液,负极的电极反应式为。
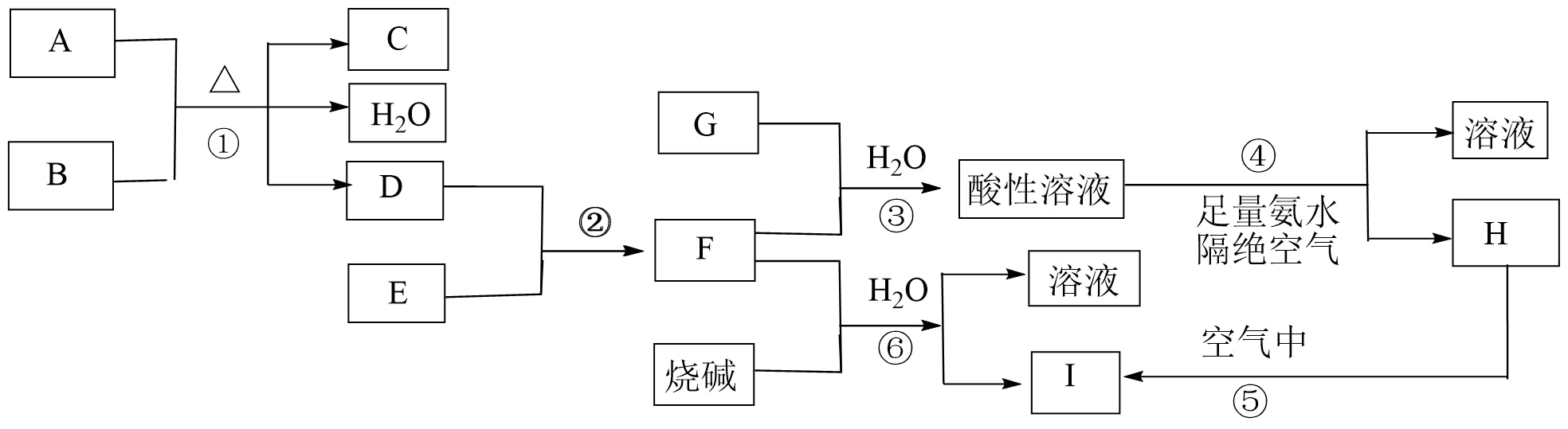
请回答下列问题:
-
(1) 推断出下列物质(用化学式作答):C,G。
-
(2) 请写出下列反应的方程式:反应①的离子方程式;反应③的离子方程式;反应⑤的化学方程式。
-
(3) 欲从反应⑥的体系中得到沉淀I的系列操作是、、恒温干燥(均填操作名称)。
-
(4) 实验室配制90 mL2 mol/L的烧碱溶液,需选用mL容量瓶。用托盘天平称取g烧碱。若定容时,俯视刻度线,配制的溶液的浓度(填“偏大”“偏小”或“无影响”)。
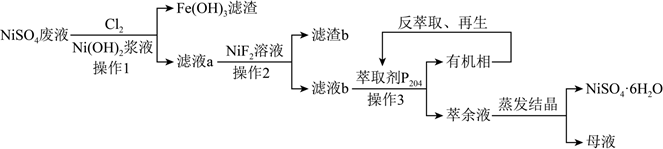
资料1:25℃时,生成氢氧化物沉淀的pH
| Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Mg(OH)2 | Ca(OH)2 | Ni(OH)2 | |
| 开始沉淀时 | 6.3 | 1.5 | 6.2 | 9.1 | 11.8 | 6.9 |
| 完全沉淀时 | 8.3 | 2.8 | 8.2 | 11.1 | 13.8 | 8.9 |
注:金属离子的起始浓度为0.1mol/L.
资料2:25℃时,Ksp(CaF2)=4×10-11 , Ksp(MgF2)=9×10-9 , ZnF2易溶于水。
资料3:P204(二乙基己基磷酸)萃取金属离子的反应为:x 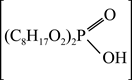 +Mx+
+Mx+ 
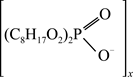 M+xH+
M+xH+
-
(1) 操作1、2的名称是,操作3的名称是。
-
(2) 操作1中加入Cl2的主要目的是。
-
(3) NiF2溶液参与反应的离子方程式是。杂质离子沉淀完全时,溶液中c(F-)=mol/L(c(杂质离子)≤10-5mol/L即可视为沉淀完全)。
-
(4) 滤液b中含有的微粒主要有。
-
(5) 在硫酸盐溶液中,P204对某些金属离子的萃取率与pH关系如图所示,在一定范围内,随着pH升高,萃取率升高的原因是。
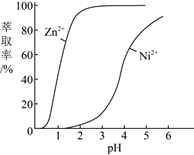
-
(6) 在母液中加入其它物质,可制备操作1中所需Ni(OH)2浆液,写出制备的离子方程式。

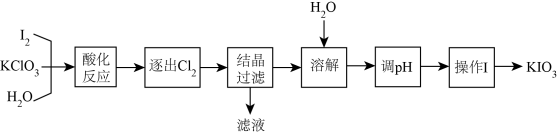
已知:“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。
-
(1) KIO3中碘元素的化合价为。
-
(2) 逐出的Cl2可用检验,“滤液”中的溶质主要是,“调pH”中所用的试剂是。
-
(3) 已知KIO3在水中的溶解度随温度升高而增大,则操作I包含的操作应该是、、过滤。
-
(4) 为测定“加碘食盐”中碘元素含量:①称取50.00g食盐,配成250mL溶液;②量取25.00mL溶液于锥形瓶中,加入足量KI,并用少量稀硫酸酸化,使KIO3与KI反应完全;③以淀粉为指示剂,用2.0×10-4mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液体积为30.00mL。已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
①判断滴定终点的依据是。
②该食盐中碘元素的含量是mg/kg。
- The idea puzzled me so much that I stopped for a few second
- 若向量a=(3,2),b=(0,-1),则向量2b-a的坐标是( )A.(3,-4) B.(
- into use in April,2000,the hotline was meant for
- (2009年1月徐州市高三质检24题)【历史上重大改革回眸】阅读下列材料: 材料一 “百日维新”虽然失败了,但它毕竟触
- 使匈奴无力再与西汉对抗的事件是A.长平之战B.昭君出塞C.匈奴分为南北两部D.漠北战役
- 已知∠α,∠β互为补角,且∠α=∠β,则∠α= _______
- (2009年浙江文综12)隶书是我国书法的五种主要字体之一,它 A.源于殷商时期的甲古文和金文 B.始
- 如图所示,半径为R的半球形陶罐,固定在可以绕竖直轴旋转的水平转台上,转台转轴与过陶罐球心O的对称轴重合,转台以一定角速度
- 已知二次函数y=mx2+nx+p图象的顶点横坐标是2,与x轴交于A(x1,0),B(x2,0),x1<0<x
- 陈独秀说:“孔子之道,施于今日之社会为不适于生存。任诸自然之淘汰,其势力迟早必归于消灭。”陈独秀批判孔子所运用的思想武器
- 1893年,中国消费品原料进口占进口总额的13%,到1903年,这一比例上升到22.3%,导致中国近代消费品原料进口额增
- 若方程的解为,则满足的最大整数 .
- (本小题满分9分) 已知,是同一平面内的两个向量,其中,且与垂直,(1)求; (2)求|- |.
- 下列反应中氯元素只被氧化的是( )。A.5Cl2+I2+6H2O=10HCl+2HIO3B.2Cl2+2Ca(O
- 襄邑道中 (宋)陈与义飞花两岸照船红,百里榆堤半日风。卧看满天云不动,不知云与我俱东。【小题1】诗人观察途中景物的立足
- 2011年1月14日,2010年度国家科学技术奖励大会在北京人民大会堂隆重举行。中国科学院院士、中国工程院院士
- 下列说法正确的是 ( ) A.CO2能与血液中血红蛋白结合导致中毒 B.CO能溶于水
- 鳕鱼在春季向北方游,深秋各南方游,这种季节性洄游主要与什么有关( ) A.阳光 B.温
- 给出下列六个命题: ① 两个向量相等,则它们的起点相同,终点相同; ② 若|a|=|b|,则a=b; ③ 若,则A、B、
- 关于豌豆自由组合定律的实验,下列哪些是正确的解释( ) ①黄色Y对绿色y是显性,圆粒R对皱粒r是显性。
 I2+I-平衡
I2+I-平衡