专题4 硫、氮和可持续发展 知识点题库
编号 | 实验内容 | 实验目的 |
A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有氧化性 |
B | 将Cl2通入NaBr溶液中 | 比较氯与溴的氧化性强弱 |
C | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 | 研究铜离子的氧化性 |
D | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
选项 | 实验 | 现象 | 结论 |
A | NaOH溶液中逐滴滴入0.1mol·L-1MgSO4溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 | 先有白色沉淀生成,后白色沉淀变为浅蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
B | CO2通入CaCl2溶液中 | 无明显现象 | 非金属性:Cl>C |
C | Cl2通入品红溶液中 | 品红褪色 | Cl2具有漂白性 |
D | 把铁片插入浓硝酸中 | 有大量红棕色气体产生 | 浓硝酸具有强氧化性 |
| 实验目的 | 实验操作及现象 | |
| A | 检验Na2SO3溶液是否变质 | 向Na2SO3溶液中加入Ba(NO3)2溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解 |
| B | 证明酸性条件下H2O2氧化性强于I2 | 向淀粉KI溶液中滴入3滴稀硫酸,未见溶液变蓝;再加入10%的H2O2溶液,溶液立即变蓝色 |
| C | 证明碳的非金属性强于硅 | 将浓盐酸滴入碳酸钠固体中,生成的气体通入盛有水玻璃的试管中,出现浑浊 |
| D | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4 溶液中,溶液紫色褪去 |
| 实验操作 | 现象 | 结论 | |
| A | 食醋浸泡水垢 | 产生无色气体 | 乙酸的酸性比碳酸强 |
| B | 乙醇与橙色酸性重铬酸钾溶液混合 | 橙色溶液变为绿色 | 乙醇具有氧化性 |
| C | 将石蜡油加强热产生的气体通入溴的四氯化碳溶液中 | 溴的四氯化碳溶液褪色 | 石蜡油分解的产物不都是烷烃 |
| D | 硫酸铜固体上滴乙醇 | 白色固体变蓝 | 乙醇中含有水 |
-
(1) Ⅰ.制备TiCl4
实验室利用反应TiO2 (s)+CCl4(g)
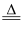 TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4 , 装置图和有关信息如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4 , 装置图和有关信息如下: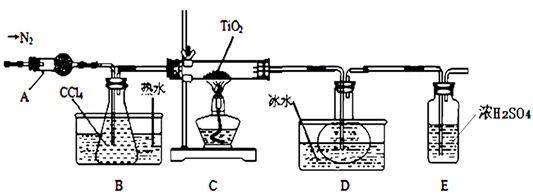
物质
熔点/℃
沸点/℃
其他
CCl4
-23
76
与TiCl4互溶
TiCl4
-25
136
遇潮湿空气产生白雾
请回答下列问题:
仪器A的名称是。
-
(2) 实验开始前后的操作包括:①检查装置气密性,②组装仪器,③通N2一段时间,④加装药品,⑤点燃酒精灯,⑥停止通N2 , ⑦停止加热。正确的操作顺序是。实验结束后欲分离D中的液态混合物,所采用操作的名称是。
-
(3) Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2。
写出生成TiO2·xH2O的化学方程式。
-
(4) 一定条件下,将TiO2溶解并还原为Ti3+ , 用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取上述TiO2试样0.2g,消耗0.1 mol·L-1 NH4Fe(SO4)2标准溶液20mL。
①则TiO2质量分数为。(相对原子量Ti-48)
②配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是抑制NH4Fe(SO4)2水解。
现在实验室中有一瓶98%的H2SO4 (ρ=1.84g/cm3) ,要配制2.0mol/L的稀H2SO4 250mL,请回答如下问题:需要量筒量取浓硫酸的体积为。在该实验使用的玻璃仪器中除烧杯、玻璃棒、量筒外,还有。
③在用浓硫酸配制稀硫酸过程中,下列操作中会造成稀硫酸溶液质量分数偏小的是(填字母)。
A.在稀释时,未恢复至室温就转移入容量瓶
B.在稀释过程中,有少量液体溅出
C.在转移过程中,烧杯和玻璃棒没有进行洗涤
D.在定容时,滴加蒸馏水超过刻度线,用滴管从容量瓶中小心取出多余液体至液体凹液面与刻度线相平
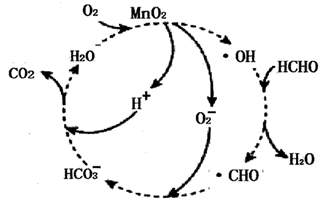
 CO2+H2O
C .
CO2+H2O
C .  为中间产物之一,该微粒与KO2中所含阴离子种类相同
D . CO2的结构式为O=C=O
为中间产物之一,该微粒与KO2中所含阴离子种类相同
D . CO2的结构式为O=C=O
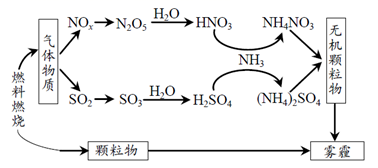
下列关于雾霾及其形成的叙述中,错误的是( )
-
(1) 用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出kJ热量。
-
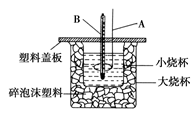
(2) 如图装置中仪器A的名称,作用是,碎泡沫塑料的作用是。
-
(3) 若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ/mol,其原因可能是。
-
(4) 用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会(填“偏大”、“偏小”或“无影响”)。
 闪电
B .
闪电
B .  合成氨车间
C .
合成氨车间
C .  绿色植物光合作用
绿色植物光合作用
实验操作 | 实验现象 | 解释或结论 | |
A | 用坩埚钳夹住已被砂纸打磨过的铝箔在酒精灯火焰上加热 | 铝不能滴落下来 | 铝熔点高,没能熔化 |
B | 将饱和FeCl3溶液滴入煮沸的NaOH溶液中,用光束照射所得液体 | 生成红褐色透明液体,用光束照射时可见一条光亮的通路 | 生成Fe(OH)3胶体有丁达尔效应 |
C | 用铂丝蘸取某溶液在火焰上灼烧,透过蓝色钴玻璃观察 | 火焰的颜色为紫色 | 该溶液中含K+ , 不含Na+ |
D | 取少量某溶液加入2滴KSCN溶液,再加入几滴氯水 | 滴加KSCN溶液时溶液不变红,滴加氯水后溶液变为红色 | 该溶液中不含Fe3+ , 含有Fe2+ |
 、
、 ⇌H++
⇌H++ D . 取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO2挥发
D . 取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO2挥发
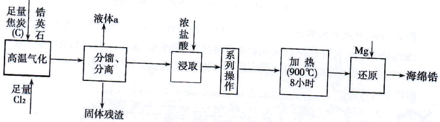
已知:常温下,ZrCl4是白色固体, 604K升华,遇水强烈水解:ZrCl4+9H2O=ZrOCl2·8H2O+2HCl,在浓盐酸中会析出ZrOCl2·8H2O沉淀。请回答下列问题:
-
(1) “高温气化”中可发生多个反应,写出发生的主要反应的化学方程式是。
-
(2) 分馏过程中,为防止产品变质,过程中一定需要注意的是。液体a的电子式是。
-
(3) 实验室中洗涤ZrOCl2·8H2O沉淀操作是。
-
(4) “还原”中氧化剂是(填化学式)。
-
(5) 由于锆铪(Hf)矿石共生,这样制得的锆中常含有少量的铪,需要进一步分离提纯。
第一步:溶解分离
将样品溶于氢氟酸后再加入一定量KOH溶液,锆和铪均以[MF6]2-存在。
①已知在水中K2HfF6比K2ZrF6的溶解度大,且K2ZrF6的溶解度随温度的升高而增大,可以利用
方法进行分离。
②离子交换法:利用强碱型酚醛树脂R-N(CH3)
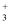 Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是。
Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是。③将所得溶液与有机相磷酸三丁酯(TBP)充分混合、振荡,可以达到Zr与Hf分离。这种分离方法是。
第二步:高温还原
在高温条件下,加入铝将制得的K2ZrF6还原可得锆,反应的化学方程式是。
-
(1) 实验室中可以在50℃左右,用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如下图。
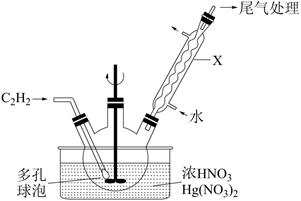
C2H2的电子式为;仪器X的名称为;装置中浓硝酸的还原产物为NO2 , 生成草酸的化学方程式为,若反应温度高于50℃,生成草酸的速率会减慢,主要原因是。
-
(2) 三草酸合铁酸钾{K3[Fe(C2O4)3]·3H2O}为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用(NH4)2Fe(SO4)2·6H2O为原料制备三草酸合铁酸钾的步骤如下:
①称取5g(NH4)2Fe(SO4)2·6H2O固体,溶解,加硫酸酸化,搅拌下加入25mL1mol·L-1H2C2O4溶液,静置,析出黄色的FeC2O4·2H2O沉淀,过滤并洗涤沉淀2~3次。
②将上述FeC2O4·2H2O沉淀溶解在10mL饱和草酸钾溶液中,再加入20mL饱和H2C2O4溶液,保持溶液温度40℃左右,缓慢滴加3%H2O2溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾30min,再加入8~9mL草酸溶液,控制pH在3~4,变为绿色透明的三草酸合铁酸钾溶液。
③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体2~3次,干燥、称量。
其中,生成FeC2O4·2H2O的化学方程式为;保持溶液温度40℃所采用的加热方法是,加热至沸腾30min的目的是;洗涤晶体所用试剂为。
-
(3) 制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定K3[Fe(C2O4)3]·3H2O(M=491g/mol)的纯度,进行如下实验:
称取样品10.72g,加稀硫酸溶解后配成100mL溶液。取20.00mL配制的溶液,用浓度为0.2000mol·L-1的KMnO4溶液滴定至终点时消耗KMnO4溶液28.00mL。已知:5H2C2O4+2
 +6H+=2Mn2++10CO2↑+8H2O,样品中K3[Fe(C2O4)3]·3H2O的质量分数为(保留两位小数)。
+6H+=2Mn2++10CO2↑+8H2O,样品中K3[Fe(C2O4)3]·3H2O的质量分数为(保留两位小数)。
-
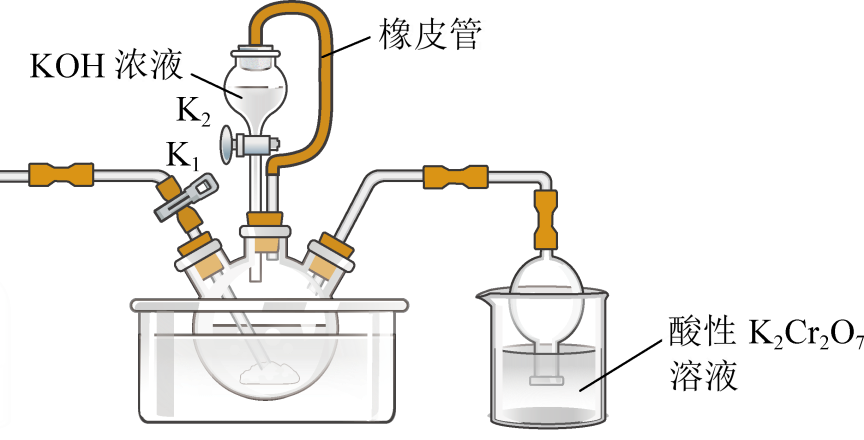
(1) NH4SCN的制备:关闭k2 , 打开k1 , 向三颈烧瓶中CS2层通入NH3并水浴加热制取NH4SCN,同时生成一种酸式盐,写出该反应的化学方程式,该反应(填“是”或“不是”)氧化还原反应。
-
(2) KSCN溶液的制备:关闭k1 , 保持三颈烧瓶内液体温度105℃一段时间以使酸式盐杂质分解除去,打开k2 , 缓缓滴入适量的KOH溶液制备KSCN溶液,该过程的加热方式为。
-
(3) 尾气处理:烧杯中酸性K2Cr2O7溶液用于除去尾气中两种污染性气体,其中一种气体A能使酚酞试液变红,另一种气体B能使酸性K2Cr2O7溶液颜色变浅(含Cr3+),且产生浅黄色沉淀,写出除去杂质气体B的离子方程式。
-
(4) KSCN晶体的制备:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,冷却结晶、、、干燥,得到KSCN晶体。
-
(5) 测定晶体中KSCN的含量:称取7.0g样品配成500mL溶液,量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000mol·L-1AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液24.00mL。
①滴定时发生的反应:SCN-+Ag+=AgSCN↓(白色),则滴定终点的现象是。
②晶体中KSCN的质量分数为(保留三位有效数字)
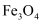 可用作油漆、红色涂料
B . 碳酸氢钠可用作食品膨松剂
C .
可用作油漆、红色涂料
B . 碳酸氢钠可用作食品膨松剂
C .  有毒,严禁将其添加到任何食品中
D . 焰火中黄色来源于钾盐灼烧
有毒,严禁将其添加到任何食品中
D . 焰火中黄色来源于钾盐灼烧
- 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd
- 名著阅读:他们站起身,手拉着手向前走去,可心里不抱任何希望。他俩想合计出呆在洞里有多久了,可是他们只知道好像是过了许多天
- 有人说“当我们全面建设小康社会的时候;当我们提倡解放思想、实事求是、与时俱进的时候,思想已经失去了它的时代意义”那么,对
- 阅读下面的文章,完成小题。 回想春天的气味 唐 敏 我常常喜欢看童话书,在夜深人静的时候,看着孩子们的故
- 如图,把一个长方形纸片沿折叠后,点分别落在的位置.若,则等于_______度.
- 如图所示,水平固定倾角为30°的光滑斜面上有两个质量均为m的小球A、B,它们用劲度系数为k的轻质弹簧连接,现对B施加一水
- 探月飞船进入地月转移轨道后关闭推进器,会依靠惯性沿地球与月球的连心线飞往月球。在飞行途中飞船中会经过一个特殊的点P,在这
- 已知F双曲线﹣=1的左焦点,E是该双曲线的右顶点,过F垂直于x轴的直线与双曲线交于A,B两点,若E在以AB为直径的圆外,
- 南南同学学完了溶质质量分数后与小组同学到实验室练习配制一定溶质质量分数的溶液。先用托盘天平称取纯净的氢氧化钠于洁净烧杯中
- 书面表达(满分25分) 从学校毕业,或上大学,或步入社会,毕业意味着前进、意味着选择。请以Graduation and
- 在高倍显微镜下观察处于有丝分裂中期的植物细胞,都能看到的结构是 A.细胞壁、染色体、细胞膜
- 下列词语中没有错别字的一组是 A.蕴藉 水蒸气 一筹莫展 集腋成裘 B.痉挛 破天荒 坐无
- 垂直,则=___________。
- I was too excited ______ . A. speak B. to
- 已知函数在x=1处的导数为3,则的解析式可能为() A. =(x-1)2+3(x-1) B. =2(
- 番茄的果肉属于A.细胞B.组织C.器官D.系统
- 短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原
- 阅读下面的材料,根据要求作文。 “挤”是一种状态,无数人挤在纷扰的城市,挤在狭窄的路上,挤在人口日渐膨胀的世界:“挤”也
- 中国古籍中有些人名,如刘敬先,殷孝祖(《宋书》),杨延宗(《新庸:括》),汤显袒(《明史》)等。你推测材料中这一现象主要
- 阅读下文,完成文后各题。 刘超,字世瑜,琅邪临沂人,汉城阳景王章之后也。(1) 章七世孙封临沂县慈乡侯,子孙因家焉。父和



