专题4 硫、氮和可持续发展 知识点题库
-
(1) 实验一:探究酸的强弱对酸与镁条反应速率的影响。
①设计实验方案如下表,表中c = mol·L-1。
编号
酸的种类
酸的浓度/mol·L-1
酸的体积/mL
镁条质量/g
①
醋酸
1.0
10
2.0
②
盐酸
c
10
2.0
②实验步骤:
a)检查装置(下图)的气密性后,添加药品;
b)反应开始后,(填写操作) ;
c)将所记录的数据转化为曲线图(右图)。
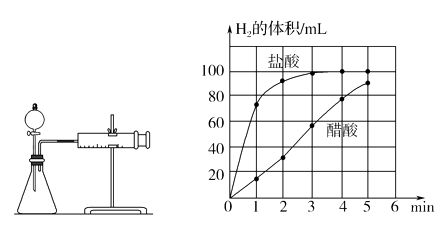
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:。
-
(2) 实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比)。
设计实验方案,将待测物理量和对应的测定方法填写在下表中。
待测物理量
测定方法
①
量取25.00mL醋酸溶液于锥形瓶中,滴加指示剂,将0.1000 mol·L-1 NaOH标准溶液装入中,滴定至终点,记录数据.重复滴定2次.
②
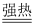 3Na2SO4 + Na2S
C . 固体产物中加入稀盐酸可能有淡黄色沉淀产生
D . 加入BaCl2溶液,出现白色沉淀,则能确定产物中有Na2SO4
3Na2SO4 + Na2S
C . 固体产物中加入稀盐酸可能有淡黄色沉淀产生
D . 加入BaCl2溶液,出现白色沉淀,则能确定产物中有Na2SO4
-
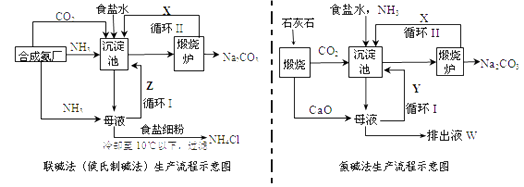
(1) 两种方法的沉淀池中均发生的反应化学方程式为。
-
(2) X是,Y是(填化学式)。
-
(3) Z中除了溶解的氨气、食盐外,其它溶质还有;排出液中的溶质除了氢氧化钙外,还有。
-
(4) 根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气能增大NH4+的浓度,使氯化铵更多析出
c.加入食盐细粉能提高Na+的浓度, 使NaHCO3结晶析出
-
(5) 为检验产品碳酸钠中是否含有氯化钠,请设计实验方案。
-
(6) 联碱法中,每当通入NH3 22.4L(已折合成标准状况下)时可以得到纯碱50.0g,则NH3的利用率为。(结果精确到0.01)
-
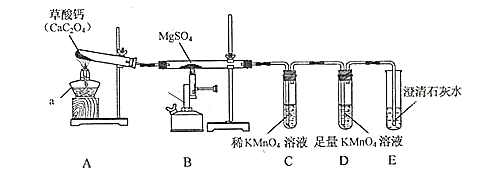
(1) 仪器 b 的名称是;CaC2O4 中 C 的化合价是。
-
(2) 连接好装置,开始实验前需要对上述装置进行的操作是。
-
(3) 装置 A 中充分反应后残留的固体是一种常见补钙剂的有效成分,则该化学方程式是。
-
(4) 实验时观察到装置 C 中紫红色褪去,装置 E 中溶液变浑浊,则装置 B 中反应的化学方程 式是;装置 D 的作用是。
-
(5) 该装置的不足之处是。
实验 | 现象 | 结论 | |
A | 某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 原溶液中有Fe2+ , 没有Fe3+ |
B | 将红热的木炭投入浓硫酸中产生的气体通入澄清的石灰水 | 石灰水变浑浊 | 木炭化成CO2 |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
D | 将0.1mol/L的NaCl溶液滴入硝酸银溶液至不现有沉淀产生,再滴加0.1mol/L KI溶液 | 先有白色沉淀生成,后变黄色沉淀 | Ksp(AgCl) >Ksp(AgI) |
 B . 证明二氧化氮生成四氧化二氮为放热反应
B . 证明二氧化氮生成四氧化二氮为放热反应 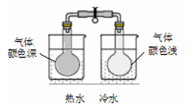 C . 测定溶液pH
C . 测定溶液pH 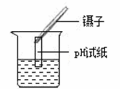 D . 测定盐酸浓度
D . 测定盐酸浓度 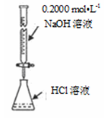
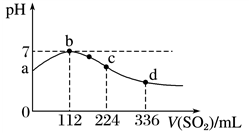
下列分析正确的是( )
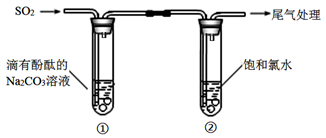
下列有关反应的方程式,错误的是( )
 HCO3-+ OH-
B . ①中溶液红色褪去的原因:2SO2 + CO32-+ H2O = CO2+ 2HSO3-
C . ②中溶液显黄绿色的原因:Cl2+ H2O = HCl + HClO
D . ②中溶液黄绿色褪去的原因:SO2+ Cl2 + 2H2O = H2SO4 + 2HCl
HCO3-+ OH-
B . ①中溶液红色褪去的原因:2SO2 + CO32-+ H2O = CO2+ 2HSO3-
C . ②中溶液显黄绿色的原因:Cl2+ H2O = HCl + HClO
D . ②中溶液黄绿色褪去的原因:SO2+ Cl2 + 2H2O = H2SO4 + 2HCl
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将氯化铁溶液加热灼烧 | 有固体析出 | 该固体是氯化铁 |
| B | 氯化铜溶液中有氯化铁杂质,加入氧化铜除杂 | 有红褐色物质析出 | 调节pH使铁离子水解平衡右移 |
| C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 |
| D | 向1 mL 0.1 mol/L的AgNO3溶液中加入4滴0.1 mol/L的NaCl溶液,再加10滴0.1 mol/L的NaI溶液,再振荡 | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
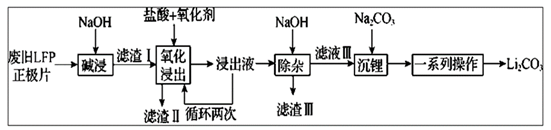
已知:Li2CO3在水中的溶解度随温度升高而降低,但煮沸时发生水解。回答下列问题:
-
(1) 在“碱浸”时,为加快浸出速率,下列措施不可行的是(填标号)。
a.适当提高浸出温度
b.使用电动搅拌器
c.适当提高氢氧化钠的浓度
d.增大废料的颗粒
-
(2) “氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如表,实际生产中氧化剂选用H2O2 , 不选用 NaClO3的原因是。在“氧化浸出”时,温度不宜超过50℃,其目的是。“氧化浸出”时生成了难溶的FePO4 , 该反应的离子方程式为。
序号
锂含量/%
氧化剂
pH
浸出液体Li浓度/(g·L-1)
浸出渣中Li含量/%
1
3.7
H2O2
3.5
9.02
0.10
2
3.7
NaClO3
3.5
9.05
0.08
3
3.7
O2
3.5
7.05
0.93
4
3.7
NaClO
3.5
8.24
0.43
-
(3) “浸出液”循环两次的目的是。
-
(4) “沉锂”的温度保持在95℃,最适宜的加热方式为。“一系列操作”具体包括、洗涤、干燥。
-
(5) “滤渣Ⅱ”经纯化可得FePO4 , 流程中生成的Li2CO3、FePO4在高温条件下与H2C2O4煅烧可得 LiFePO4 , 实现再生利用,其化学方程式为。
-
(1) I.化合物A由三种元素组成,气体B是含氢量最高的烃。固体E既能溶于盐酸,又能溶于氢氧化钠溶液。按如下流程进行实验:
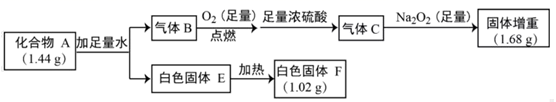
E的化学式为:,气体C与Na2O2反应的化学方程式为:
-
(2) A的化学式为:,A与足量盐酸反应的化学方程式为:
-
(3) Ⅱ.将ClO2通入NaOH和H2O2的混合溶液中,可制得一种高效漂白剂亚氯酸钠(NaClO2),实验装置如图所示:
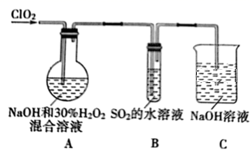
请回答:
写出A装置中发生反应的离子方程式
-
(4) 请设计实验方案探究通入足量的ClO2后,B装置溶液中存在的含有硫元素的微粒
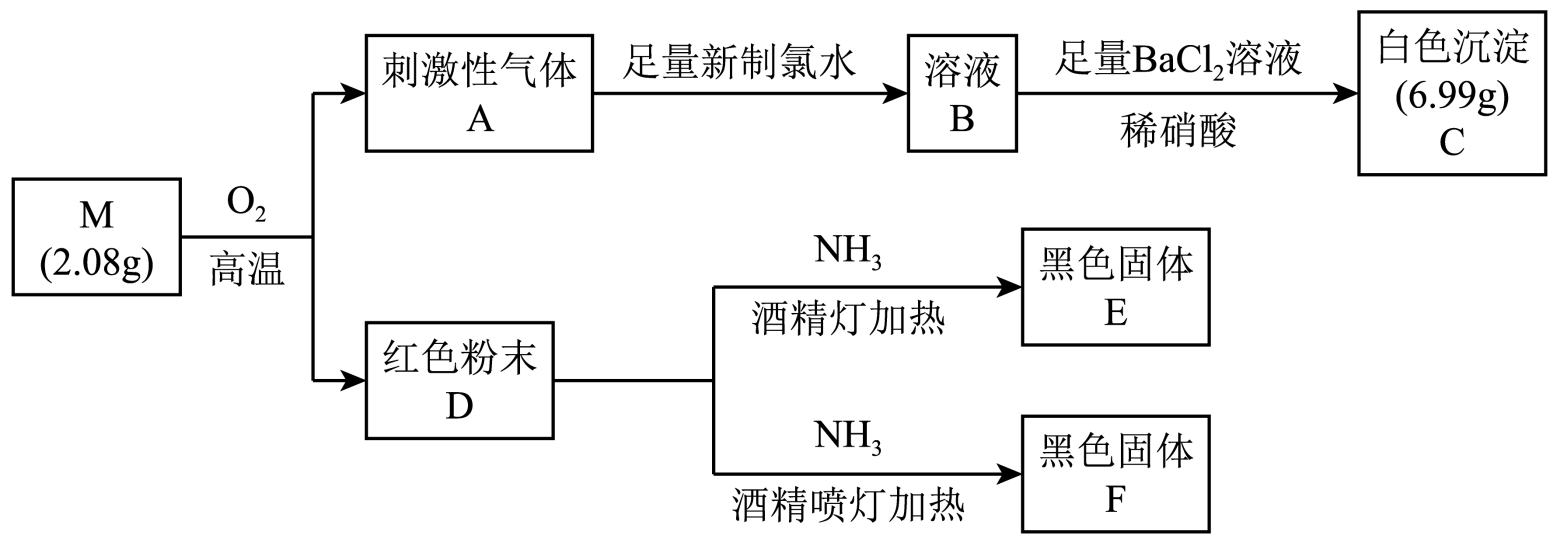
回答下列问题:
-
(1) D是(填化学式)。
-
(2) 根据上述信息推知,M是(填化学式)。
-
(3) 将A通入新制氯水中发生主要反应的离子方程式为。
-
(4) 为了探究温度对D和氨气反应的产物的影响,设计如下实验:
步骤
操作
E(甲组)
F(乙组)
I
取少量产物,加入稀盐酸
溶解、无气泡
溶解,有气泡
II
取步骤I中溶液,滴加KSCN溶液
溶液变红
无明显变化
III
向步骤II溶液中滴加双氧水
红色变深
溶液变红
①根据上述现象,得出实验结论:E为X3O4(X表示形成化合物M的一种元素),F为(填化学式)。
②乙组实验中,步骤III中溶液由无色变红的原因是(用离子方程式表示)。
③通过交流、讨论,有人认为E中除X3O4外还可能含单质X,判断的理由是。

 )俗称保险粉,易溶于氢氧化钠溶液,难溶于乙醇,干粉末易吸水,受热易分解,是一种强还原剂,用于纺织工业的漂白。实验室用如图所示装置(夹持装置已略去)制备保险粉,其相关制备原理为
)俗称保险粉,易溶于氢氧化钠溶液,难溶于乙醇,干粉末易吸水,受热易分解,是一种强还原剂,用于纺织工业的漂白。实验室用如图所示装置(夹持装置已略去)制备保险粉,其相关制备原理为 。
。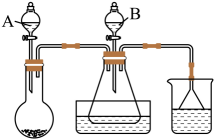
回答下列问题:
-
(1) 烧瓶中
 固体与仪器A中硫酸反应制取
固体与仪器A中硫酸反应制取 , 仪器A的名称为。
, 仪器A的名称为。
-
(2) 打开仪器A的活塞,滴入硫酸。一段时间后,打开仪器B的活塞往锥形瓶中加入甲酸钠和氢氧化钠的甲醇溶液,继续通入
 并控制反应温度不超过83℃,待锥形瓶中出现晶体,再通过仪器B加入乙醇,之后过滤,洗涤,干燥。
并控制反应温度不超过83℃,待锥形瓶中出现晶体,再通过仪器B加入乙醇,之后过滤,洗涤,干燥。①烧杯中盛放的试剂是。
②打开仪器A的活塞一段时间之后,再打开仪器B的活塞加入反应液的原因为。
③温度控制不超过83℃的原因为。
④加入乙醇的目的为。
-
(3) 某小组设计实验测定某保险粉样品中连二亚硫酸钠的质量分数,相关测定原理如下(杂质不参与反应):
①
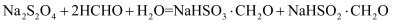
②

请完成表格内容:
操作
现象
目的/结论
Ⅰ
取mg样品于烧杯中,加入20mL中性甲醛溶液,搅拌至完全溶解,缓慢转移至250mL容量瓶中,用水稀释至刻度,摇匀。
目的:样品处理,将
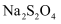 转化为
转化为
Ⅱ
移取25.00mL该溶液至250mL锥形瓶中,加入盐酸溶液和少量溶液,然后用浓度为c mol/L的标准碘溶液滴定至终点,重复三次实验,消耗标准碘溶液的体积的平均值为V mL。
当滴入最后一滴标准碘溶液时,溶液变为蓝色,且半分钟内不褪色
结论:
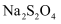 的质量分数为(用含m、V、c的代数式表示)
的质量分数为(用含m、V、c的代数式表示)
选项 | 实验操作 | 现象 | 结论 |
A | 将干燥纯净的氯气依次通过干燥的有色布条和湿润的有色布条 | 只有湿润的有色布条褪色 | 干燥的氯气没有漂白性 |
B | 用坩埚钳夹住一束铁丝,放入充满氯气的集气瓶中 | 剧烈燃烧,产生红棕色烟 | 氯气与铁反应生成氯化铁 |
C | 向 | 产生白色沉淀,溶液红色逐渐变浅 | 产物硫酸钡和水都是非电解质,不导电 |
D | 向培养皿中加入适量水,滴入1~2滴酚酞溶液,取一块绿豆粒大小的金属钠放入水中 | 剧烈反应,有气体产生,溶液颜色由无色变为红色 | 钠与水反应产生碱性物质 |
 与金属钠在高温下反应生成纳米石墨,设计如下装置:
与金属钠在高温下反应生成纳米石墨,设计如下装置: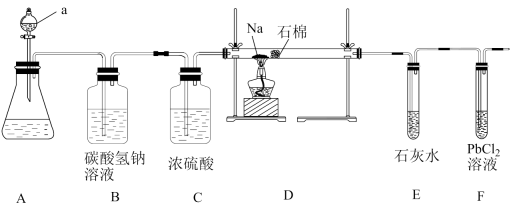
回答下列问题
-
(1) 装置A中的a的仪器名称为。
-
(2) 实验时,在点燃酒精灯前必须进行的操作是。
-
(3) 装置E中出现现象时,再点燃酒精灯,以上操作的目的是。
-
(4) 待装置D加热一段时间后观察到钠块表面变黑,继续加热后,钠燃烧,有白烟生成。取残留固体溶于水,发现有黑色的不溶颗粒存在;取上层液体与过量的
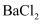 溶液反应发现有白色沉淀生成,根据以上信息,写出装置D中的反应方程式。
溶液反应发现有白色沉淀生成,根据以上信息,写出装置D中的反应方程式。
-
(5) 装置F中的
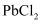 溶液吸收CO变黑色,可以处理产生的尾气,试用反应方程式分析CO产生的原因。
溶液吸收CO变黑色,可以处理产生的尾气,试用反应方程式分析CO产生的原因。
- Max is __________ at playing volleyball than me. A.goodB.wel
- 上海中智库玛在线调查公司调查结果显示:有83%的中国人希望有机会在现场观看奥运会,人们最关心“奥运会的门票价格”。200
- 学校组织到农村参加社会实践活动,小强第一次学习挑担子,他做了以下三次实验,请你根据各小题后的要求作答。 (1)他先在扁担
- 阅读下面的文字,完成19~22题。(18分)吃 饭王琼华“我是陈宝山,老部长,您还记得我吗?”快下班时,一个电话让我呆
- 阅读下面的材料,按要求作文。(60分) 在汽车已经走进千家万户的今天,越来越多的人学会了开车。开车的人都知道,在某个位置
- 如图所示,半径为L=1m的金属圆环,其半径Oa是铜棒,两者电阻均不计且接触良好。今让Oa以圆心O为轴,以角速度=10ra
- 党的十七大报告中指出:“建设生态文明,基本形成节约能源和保护生态环境的产业结构、增长方式、消费模式”。之所以要重视生态文
- 在表中四种实验条件下,测定了不同光照强度对光合作用速率的影响,结果如图所示。则①曲线1和曲线3比、②曲线4和曲线3比、③
- --- Shall I take a message for you? --- _____. A. You are we
- 已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:元素A
- 在一定容积的密闭容器中发生可逆反应A(g)+2B(g)2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是: A
- 要了解近代广东民族资本主义企业的历史,可以提供较详尽资料的是( ) A.继昌隆缫丝厂 B.贻来牟机器磨坊
- 马克思、恩格斯说:“由于阶级对立的发展是同工业的发展步调一致的,所以这些发明家也不可能看到无产阶级解放的物质条件,于是他
- Be tough-minded, but tender-hearted, ? A.isn’t
- 将1mol N2和3 mol H2通入4L的密闭容器中反应,半分钟后测得H2的物质的量为2.1 mol,现用如下三种物质
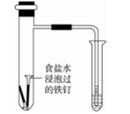
- 把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图4-24所示平面图),经过一段时间后,首先观察到溶液变红的
- 温家宝指出:“就业不仅关系一个人的生计,而且关系一个人的尊严。”这就要求政府 A.通过推动经济发展为劳动者直接安
- 2009年6月26日,广东省韶关市一家玩具厂部分新疆籍员工与该厂其他员工发生冲突。事件发生后,境外“三股势力”大肆炒作,
- 猪笼草是一种食虫植物,为了验证猪笼草分泌液中有蛋白酶,某学生设计了两组实验,如下图所示。经35℃水浴保温一段时间后,1、
- 已知曲线y=f(x)=2x2上一点A(2,8),则点A处的切线斜率为() A.4 B.16 C.8 D.2
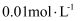
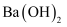 溶液中滴入几滴酚酞溶液,插入电导率传感器,然后匀速逐滴加入
溶液中滴入几滴酚酞溶液,插入电导率传感器,然后匀速逐滴加入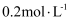
 溶液
溶液


