实验1-3 污水处理--电浮选凝聚法 知识点题库
MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600¾﹣700¾,所用燃料为H2 , 电解质为熔融的K2CO3 . 已知该电池的总反应为2H2+O2═2H2O,则下列有关该电池的说法正确的是( )
A . 该电池的正极的反应式为:4OH﹣+4e﹣═O2+2H2O
B . 该电池负极的反应为:H2+CO32﹣﹣2e﹣═H2O+CO2
C . 放电时CO32﹣向正极移动
D . 该燃料电池能量转化率很低
常温下铝在空气中不易生锈而铁易生锈原因是( )
A . 铝比铁化学性质活泼
B . 铝表面有一层致密氧化膜起保护作用
C . 铝性质太活泼已经全部被氧化成了氧化铝
D . 铁有可能只失去二个电子而铝失三个电子,从而比铝更容易被氧化
化学能帮助我们更好地认识生活、改善生活.
①家用铁锅未洗净晾干,放置一段时间后出现红褐色锈斑,其主要的原因是铁发生了腐蚀.
②乘车禁止携带物品的部分标识如图所示.在浓硝酸、食盐、汽油、石膏四种物品中,不能携带上车的是.
③过氧乙酸( ![]() )易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式.某胃药的主要成分是AlbMgc(OH)mCO3 , 常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式.
)易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式.某胃药的主要成分是AlbMgc(OH)mCO3 , 常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式.

关于金属的腐蚀和防护说法不正确的是( )
A . 纯的金属在有水的溶液中比不纯的金属(或合金)在其中更容易发生腐蚀
B . 金属根据接触的介质的不同,发生腐蚀的化学原理分为:化学腐蚀和电化学腐蚀
C . 铝不需要特别的处理就具有抗腐蚀能力
D . 在轮船在装上一块锌可以起到保护船身的作用
我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖.
①合金是生活中常见的材料.某合金具有密度小、强度高的优良性能,常用于制造门窗框架.该合金中含量最高的金属元素的原子结构示意图为.
②铁锈的主要成分是(填化学式),它是钢铁在潮湿的空气中发生腐蚀的结果.
③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有Na2CO3、和(填化学式).
下列有关物质性质或应用的说法正确的是( )
A . 医疗上,常用碳酸钠治疗胃酸过多
B . 在海轮外壳上安装锌块以减缓船体腐蚀
C . 液氨汽化放出大量的热,可用作制冷剂
D . 明矾具有强氧化性,常用于自来水的杀菌消毒
下列方法不能用于金属防腐处理的是( )
A . 电镀
B . 船底焊上锌块
C . 喷油漆、涂油脂
D . 把金属制品埋入潮湿、疏松的土壤中
锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH- , 下列说法错误的是( )
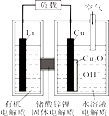
A . 整个反应过程中,氧化剂为O2
B . 放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
C . 放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应
D . 通空气时,铜被腐蚀,表面产生Cu2O
下列有关说法正确的是( )
A . 一定条件下反应2SO2+O2  2SO3达到平衡时,v(O2)正=2v(SO3)逆
B . 用右图所示方法可保护钢闸门不被腐蚀
2SO3达到平衡时,v(O2)正=2v(SO3)逆
B . 用右图所示方法可保护钢闸门不被腐蚀 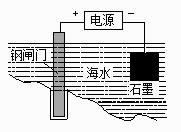 C . 常温下,向NH4Cl溶液中加入少量NaOH固体,溶液中
C . 常温下,向NH4Cl溶液中加入少量NaOH固体,溶液中  的值增大
D . 常温下, pH=2的HCl溶液与pH=12的Ba(OH)2溶液等体积混合,两者恰好完全反应
的值增大
D . 常温下, pH=2的HCl溶液与pH=12的Ba(OH)2溶液等体积混合,两者恰好完全反应
 2SO3达到平衡时,v(O2)正=2v(SO3)逆
B . 用右图所示方法可保护钢闸门不被腐蚀
2SO3达到平衡时,v(O2)正=2v(SO3)逆
B . 用右图所示方法可保护钢闸门不被腐蚀  C . 常温下,向NH4Cl溶液中加入少量NaOH固体,溶液中
C . 常温下,向NH4Cl溶液中加入少量NaOH固体,溶液中  的值增大
D . 常温下, pH=2的HCl溶液与pH=12的Ba(OH)2溶液等体积混合,两者恰好完全反应
的值增大
D . 常温下, pH=2的HCl溶液与pH=12的Ba(OH)2溶液等体积混合,两者恰好完全反应
下列说法或表达正确的是( )
①次氯酸的电子式为 ![]()
②含有离子键的化合物都是离子化合物
③等质量的O2与O3中,氧原子的个数比为3:2
④丁达尔效应可用于区分溶液和胶体,云、雾均能产生丁达尔效应
⑤将金属Zn与电源的负极相连,可防止金属Zn被腐蚀
⑥稀硫酸、氨水均为电解质
A . ②④⑤
B . ②④
C . ①③⑤
D . ①②③
下列有关金属腐蚀与防护的说法错误的是( )
A . 纯银器表面在空气中因化学腐蚀渐渐变暗
B . 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C . 海轮外壳连接锌块以保护外壳不受腐蚀
D . 可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其对环境无污染,能量密度高,电池总反应为: 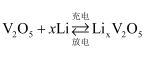 。下列说法中错误的是()
。下列说法中错误的是()
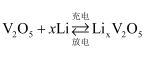 。下列说法中错误的是()
。下列说法中错误的是()
A . 放电时负极反应为: 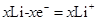 B . 若放电时转移
B . 若放电时转移 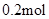 电子,则用去的锂为
电子,则用去的锂为 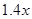 g
C . 锂在放电时做负极材料,充电时为阴极材料
D . 该电池充电时阳极的反应为:
g
C . 锂在放电时做负极材料,充电时为阴极材料
D . 该电池充电时阳极的反应为: 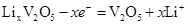
下列有关金属腐蚀与防护的说法正确的是( )
A . 钢铁析氢腐蚀和吸氧腐蚀的速率一样快
B . 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C . 海轮外壳焊接锌块是采用了牺牲阳极的阴极保护法
D . 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
被称为“软电池”的纸质电池,其总反应为:Zn+2MnO2+H2O=ZnO+2MnOOH。下列说法正确的是( )

A . 该电池中 Zn 作正极
B . MnO2 电极上发生氧化反应
C . 该电池工作时电流由 Zn 经导线流向 MnO2
D . 当 6.5gZn 完全溶解时,流经电路的电子数目为 0.2NA
下列叙述中错误的是( )
A . 电热水器用镁棒防止内胆腐蚀,采用的是牺牲阳极的阴极保护法
B . 葡萄酒中含维生素C等多种维生素,通常添加微量  防止营养成分被氧化
C . 复方氢氧化铝、碳酸氢钠片、雷尼替丁等抗酸药均能抑制胃壁细胞分泌盐酸
D . 2020年1月我国爆发了新冠肺炎疫情,可采用“84”消毒液来杀灭新型冠状病毒
防止营养成分被氧化
C . 复方氢氧化铝、碳酸氢钠片、雷尼替丁等抗酸药均能抑制胃壁细胞分泌盐酸
D . 2020年1月我国爆发了新冠肺炎疫情,可采用“84”消毒液来杀灭新型冠状病毒
 防止营养成分被氧化
C . 复方氢氧化铝、碳酸氢钠片、雷尼替丁等抗酸药均能抑制胃壁细胞分泌盐酸
D . 2020年1月我国爆发了新冠肺炎疫情,可采用“84”消毒液来杀灭新型冠状病毒
防止营养成分被氧化
C . 复方氢氧化铝、碳酸氢钠片、雷尼替丁等抗酸药均能抑制胃壁细胞分泌盐酸
D . 2020年1月我国爆发了新冠肺炎疫情,可采用“84”消毒液来杀灭新型冠状病毒
下列说法错误的是( )
A .  会破坏铝表面氧化膜的结构
B . 钢铁在潮湿空气中生锈主要是发生了化学腐蚀
C . 不可以向人体注射消毒水来杀灭2019-nCoV
D .
会破坏铝表面氧化膜的结构
B . 钢铁在潮湿空气中生锈主要是发生了化学腐蚀
C . 不可以向人体注射消毒水来杀灭2019-nCoV
D .  的热稳定性比
的热稳定性比  强
强
 会破坏铝表面氧化膜的结构
B . 钢铁在潮湿空气中生锈主要是发生了化学腐蚀
C . 不可以向人体注射消毒水来杀灭2019-nCoV
D .
会破坏铝表面氧化膜的结构
B . 钢铁在潮湿空气中生锈主要是发生了化学腐蚀
C . 不可以向人体注射消毒水来杀灭2019-nCoV
D .  的热稳定性比
的热稳定性比  强
强
埋在地下的钢管常用如图所示方法加以保护,使其免受腐蚀,下列说法不正确的是( )
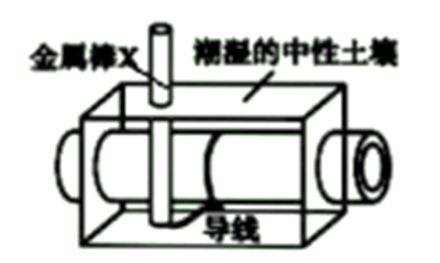
A . 金属棒的材料可能为镁
B . 钢管附近土壤的pH增大
C . 这种方法称为外加电流的阴极保护法
D . 镀锌铁片的镀层破坏后铁皮仍耐腐蚀的原理与此相同
铁及其化合物是生活中常见的物质。
-
(1) 铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,铜作(填 “阳”或“阴”)极,铜离子向极移动,阴极的电极反应式为。
-
(2) 下图中,为了减缓海水对铁闸门A的腐蚀,材料B可以选择(填字母序号)。
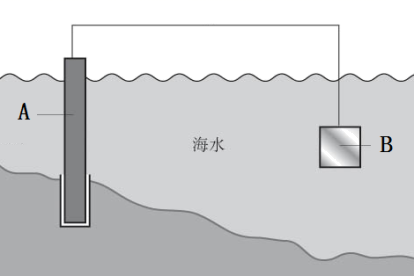
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:。
-
(3) 将FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该变化的离子方程式为。
含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是( )
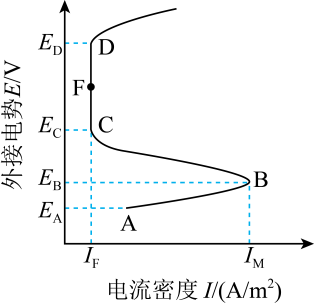
A . 阳极保护法中受保护的金属外接电源的负极
B . 电流密度越大,金属受保护程度越好
C . CFD区,金属受到保护
D . 外接电势越高,对金属保护性越有效
下列叙述中正确的是( )
A . 由铜、锌作电极与硫酸溶液组成的原电池中,溶液中的H+向正极移动
B . 钢铁发生腐蚀时,正极上发生的反应为Fe-2e-=Fe2+
C . 铜锌原电池工作时,若有13 g锌被溶解,溶液中就有0.4 mol电子通过
D . 原电池必须有两个活泼性不同的金属作电极
最近更新
- 如图,将“笑脸”图标向右平移4个单位,再向下平移2个单位,点P的对应点P'的坐标是()A.(﹣1,6) B.(﹣9,
- 如图,有一艘渔船在捕鱼作业时出现故障,急需抢修,调度中心通知附近两个小岛A、B上的观测点进行观测,从A岛测得渔船在南偏东
- 对于相同状况下的12C18O和14N2两种气体,下列说法正确的是A.若质量相等,则质子数相等 B.若分
- 在没有被破坏的地层中,有关化石分布情况,下列不正确的是( ) A、古老地层中的生物化石简单低等 B、在极古老的地层
- 【2012年·浙江省台州市】 4.阅读下列材料,回答问题。(4分) 材料一:中国烟民已超过3亿,占全球吸烟者总数
- 下列关于复制、转录和翻译的说法正确的是()A. 三个过程在所有生活细胞都能进行 B. 三个过程发生的场所都是细胞质 C.
- 下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
- 当一只蚜虫受到攻击时,就会放出一种起警告作用的化学物质,以便使邻近的蚜虫迅速逃避敌害,这种现象所属的特征及信息传递类型分
- 曲线上切线平行于轴的点的坐标是 A.(-1,2) B.(1,-2
- 在炎炎盛夏,常常看到一些工地上工人们挥汗如雨的施工景象。暑期劳动安全卫生问题,已经成为维护各地农民工权益的突出问题。某地
- 下列实验操作正确的是( )
- 若α、β∈(0,)、cos(-β)=,sin(-β)=-,则cos(α+β)的值为( )A.- B.
- 某地,水平运动的物体向左偏,一年中只有一天太阳直射,该地位于 ( ) A、北回归线 B、南回归线 C
- 两个氨基酸分子缩合形成二肽,脱去一分子水。这个水分子中的氢来自( ) A.羧基(—COOH)
- 求与直线y=x相切,圆心在直线y=3x上且被y轴截得的弦长为2的圆的方程.
- 种子萌发时,不必需具备的外界条件是A.适宜的温度B.充足的空气C.适量的水分D.较强的光照
- 国石化销售有限公司与25家境内外投资者签署要的相关协议,中国石化销售有限公司的注册资本将由人民币200亿元增至人民币28
- A: I prefer western food .It’s a kind of healthy food. B: __
- 图3-1中是正方体的展开图的是() 图3-1
- 读写任务(共1小题,满分25分) 阅读下面的短文,然后按照要求写一篇150词左右的英语短文。 A teacher onc



