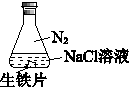
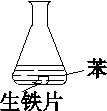
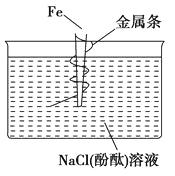
实验1-3 污水处理--电浮选凝聚法 知识点题库
 2PbSO4(s)+2H2O(l),下列说法正确的是( )
2PbSO4(s)+2H2O(l),下列说法正确的是( )
2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(g)
-
(1) 在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图1所示.
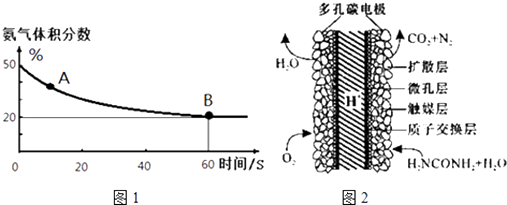
A点的正反应速率v正(CO2) B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”);氨气的平衡转化率为.
-
(2) 氨基甲酸铵是合成尿素的一种中间产物.将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:2NH3(g)+CO2(g)═NH2COONH4(s)将实验测得的不同温度下的平衡数据列于表:
温度(℃)
15.0
20.0
25.0
30.0
35.0
平衡气体总浓度 (10﹣3mol/L)
2.4
3.4
4.8
6.8
9.4
①关于上述反应的焓变、熵变说法正确的是.
A.△H<0,△S<0B.△H>0,△S<0 C.△H>0,△S>0D.△H<0,△S>0
②关于上述反应的平衡状态下列说法正确的是
A.分离出少量的氨基甲酸铵,反应物的转化率将增大
B.平衡时降低体系温度,CO2的体积分数下降
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高氨基甲酸铵的产率
③氨基甲酸铵极易水解成碳酸铵,酸性条件水解更彻底.将氨基甲酸铵粉末逐渐加入1L0.1mol/L的盐酸溶液中直到pH=7(室温下,忽略溶液体积变化),共用去0.052mol氨基甲酸铵,此时溶液中几乎不含碳元素.
此时溶液中c(NH4+)=;(填具体数值)NH4+水解平衡常数值为.
-
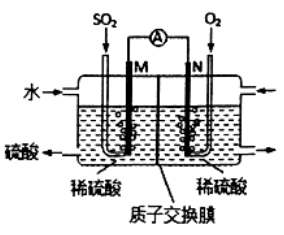
(3) 化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电.尿素燃料电池结构如图2所示,写出该电池的负极反应式:.
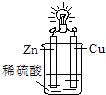 电池中锌是正极
B .
电池中锌是正极
B . 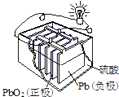 电池是一次电池
C .
电池是一次电池
C . 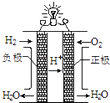 电池工作时,氢气发生还原反应
D .
电池工作时,氢气发生还原反应
D . 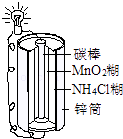 电池工作时,电子由锌通过导线流向碳棒
电池工作时,电子由锌通过导线流向碳棒
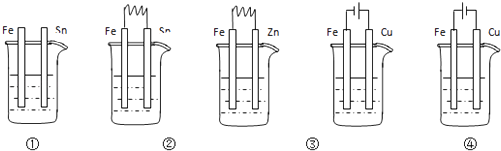
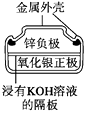
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
-
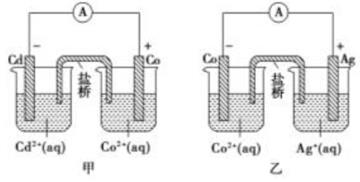
(1) 甲中Co电极发生的反应方程式为。
-
(2) 两烧杯中盐桥(填充物为浸有饱和KNO3溶液的琼脂)的作用是并使两烧杯中溶液保持电中性。
-
(3) 判断反应2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq)能否自发进行并解释理由。
-
(4) 开始时,乙电池左右烧杯各含100溶液,且Co2+、Ag+浓度均为4mol/L,当有1.204×1022个电子通过外电路时,两烧杯溶液中Co2+、Ag+浓度差为(忽略溶液的体积变化)。
-
(1) PSCl3(结构式为:
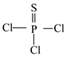 )中磷的化合价为。
)中磷的化合价为。
-
(2) S2Cl2分子中各原子均满足8电子结构,画出S2Cl2的结构式:。
-
(3) 能说明同周期的相邻元素S的非金属性比Cl弱的事实是_____(填标号)。A . H2SO3的酸性比HClO3的弱 B . 气态H2S的热稳定性比HCl的弱 C . Cl2通入Na2S溶液可发生反应:Cl2+S2-=2Cl-+S↓ D . SO2是常见的还原剂,ClO2是常见的氧化剂
-
(4) SOCl2(沸点78.8℃)可用作锂电池的非水电解质及有机合成的氯化剂等。
①SOCl2可由S2Cl2、SO2及Cl2在催化剂和180~200℃时,通过发生化合反应制得,该反应的化学方程式为。
②Li/SOCl2电池的电池反应为:4Li+2SOCl2→4LiCl↓+S+SO2。电池工作时,下列说法正确的是(填标号)。
A.Li电极的质量不变 B.电能转变为化学能
C.负极发生氧化反应 D.正极上SOCl2被还原
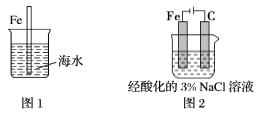
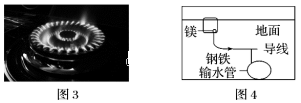
| 序号 | ① | ② | ③ |
| 实验 | | | |
| 现象 | 8小时未观察 到明显锈蚀 | 8小时未观察 到明显锈蚀 | 1小时观察 到明显锈蚀 |
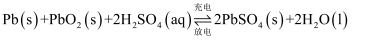 ②电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列关于电池的叙述正确的是( )
②电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列关于电池的叙述正确的是( )
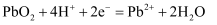
下列说法错误的是( )
- 自1957年10月4日,前苏联发射了世界上第一颗人造卫星以来,人类的活动范围逐步扩展,现在已成功地把人造天体送到火星上漫
- 下列叙述正确的是( ) A.钠在氧气中燃烧,火焰呈黄色,产生白色固体 B.屠呦呦利用乙醇萃取青蒿汁中的青蒿素,
- 洗衣机的脱水筒在工作时,有一衣物附着在竖直的筒壁上,则此时( )A.衣物受重力、筒壁弹力和摩擦力作用B.衣物随筒壁
- 常温下,A、B组成的混合气体()经分析发现无论怎样混合,气体中仅含的C、O两种元素的质量比总小于3∶8,若混合气体中C、
- 隋唐书法和绘画艺术灿烂夺目。下列各项,属隋唐时期书法家的是( ) ①阎立本 ②颜真卿 ③吴道
- (2013•长沙)用图甲所示的滑轮组运送货物上楼,每件货物重100N,每次运送的量不定,图乙记录了在整个过程中滑轮组的机
- 下列关于植物类群的叙述,正确的是() A.海带是藻类植物,依靠它的根固着在浅海岩石上 B.墙藓的茎、叶内没有输导组织,所
- 下列原子中的未成对电子数为1的是(单独占据1个原子轨道的电子称为未成对电子) ( ) A.N
- —Sorry, Sir. I didn’t quite follow you. — ______. I’ll ex
- 18世纪,亚当·斯密发现在一家扣针厂里,生产一枚扣针需要经过18道工序,这家工厂共10个工人,每人分别承担1—2道工序,
- Dear Editor. I’m a middle schoolstudent named Li Hua. I’m wr
- 原核细胞和真核细胞最明显的区别在于( ) A.有无核物质 B.有无细胞壁 C.有无核膜 D.有无细胞
- 已知一个几何体的三视图和有关的尺寸如图所示,描述该几何体的形状,并根据图中数据计算它的表面积。
- 如图所示,一质量m1=0.45kg的平顶小车静止在光滑的水平轨道上。车顶右端放一质量m2=0.2kg的小物体,小物体可视
- 下列实验操作中错误的是( ) A.称量食盐时,称量物放在称量纸上置于托盘天平左盘,砝码放在称量纸上置于托盘天平右
- 道路密度指的是在一定区域内,道路网的总里程与该区域面积的比值,平均车行速度是指某地区各种汽车的平均行车速度。下图是“某特
- 下列各项属于克里特文明与迈锡尼文明相同点的是( ) A.都产生于公元前16世纪B.都有泥版文书的出现C.都被古希腊人摧毁
- 假设你是李华,你的英国朋友Jack准备暑假一个人来中国游览三峡。请根据以下要点用英语给Jack写一封信为他提
- 十九世纪英国首相帕麦斯顿曾说“没有永远的朋友,也没有永远的敌人,只有永远的利益”。一战时,最能说明这句话的“望风使舵”的
- China news, Beijing, Feb. 9 – Housing price in China has alw