实验1-3 污水处理--电浮选凝聚法 知识点题库
(1)写出工业上用赤铁矿炼铁的主要化学反应方程式: 。
(2)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.试回答:
①铁锅的腐蚀主要是由(填化学或电化学)腐蚀造成的.形成的铁锈的主要成分是 。
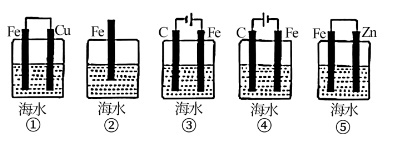
②为防止轮船的船体在海水中腐蚀,一般在船身连接 (填“锌块”或“铜块”)。
(1)已知H2、CO和CH3OCH3的燃烧热(△H)分别为﹣285.5kJ/mol、﹣283kJ/mol和﹣1460.0kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2 , 将悬浮物带到水面,利于除去.实验室以二甲醚燃料电池模拟该方法设计的装置如图所示:
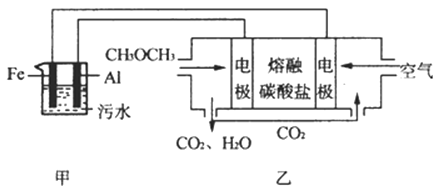
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极.写出该燃料电池的正极电极反应式 下列物质可用做电池熔融碳酸盐的是
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式:
③已知常温下Kap[Fe(OH)3]=4.0×10﹣38 , 电解一段时间后,甲装置中c(Fe3+)=
④已知:H2S的电离平衡常数:K1=9.1×10﹣8、K2=1.1×10﹣12;H2CO3的电离平衡常数:K1=4.31×10﹣7、K2=5.61×10﹣11 . 测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列各项正确的是
A.发生反应的离子方程式为:CO2+S2﹣+H2O═CO32﹣+H2S
B.发生反应的离子方程式为:CO2+S2﹣+H2O═HCO3﹣+HS﹣
C.c(Na+)=2[c(H2S)+c(HS﹣)+c(S2﹣)]
D.c(Na+)+c(H+)=2c(CO32﹣)+2c(S2﹣)+c(OH﹣)
E.c(Na+)>c(HCO3﹣)>c(HS﹣)>c(OH﹣)

-
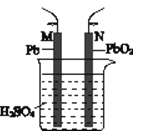
(1) 铅蓄电池是一种典型的可充电电池,电池总反应式为:
Pb+PbO2+4H++2SO42﹣
 2PbSO4+2H2O.写出放电时负极的电极反应式.
2PbSO4+2H2O.写出放电时负极的电极反应式. -
(2) 早在古代,硫酸铅就被用作白色颜料,但用这种颜料作出的画天长日久会变为黑色,经检测其成分为PbS.古画修复师在变黑处涂抹H2O2后即可将颜色修复,用化学方程式表示古画修复颜色的原理.
-
(3) PbO与次氯酸钠溶液反应可以制得PbO2 , 写出该反应的离子方程式.
-
(4) PbO2在加热过程中发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%(
 ×100%)的残留固体,若a点固体表示为PbOx或mPbO2•nPbO,列式计算x=,m:n=.
×100%)的残留固体,若a点固体表示为PbOx或mPbO2•nPbO,列式计算x=,m:n=. 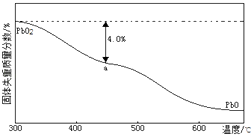
 Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
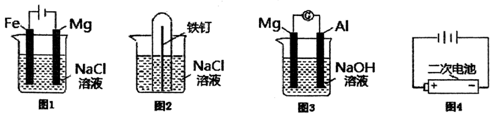
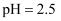 和
和 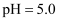 的醋酸溶液分别与生铁反应,进行腐蚀实验,测量密闭容器内压强变化情况如图。下列结论错误的是( )
的醋酸溶液分别与生铁反应,进行腐蚀实验,测量密闭容器内压强变化情况如图。下列结论错误的是( ) 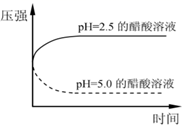
 的醋酸溶液中一定存在吸氧腐蚀
B . 酸度不同,腐蚀的主要类型可能不同
C . 两组溶液的pH一定逐渐变大
D . 若改用盐酸进行实验,腐蚀速率一定变大
的醋酸溶液中一定存在吸氧腐蚀
B . 酸度不同,腐蚀的主要类型可能不同
C . 两组溶液的pH一定逐渐变大
D . 若改用盐酸进行实验,腐蚀速率一定变大
 与H2反应生成S2- , 加速钢管的腐蚀,其反应原理如下图所示。
与H2反应生成S2- , 加速钢管的腐蚀,其反应原理如下图所示。 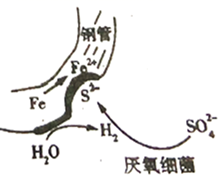
下列说法正确的是( )
 与H2的反应可表示为:4H2+
与H2的反应可表示为:4H2+  -8e-
-8e-  S2-+4H2O
S2-+4H2O
 D . 科考船只采用电化学保护法提高船体抗腐蚀能力
D . 科考船只采用电化学保护法提高船体抗腐蚀能力
- 印度最大的港湾和棉纺织品工业中心是( ) A.科伦坡 B.孟买 C
- 下列结构属于细胞水平的是( ) A.神经纤维 B一弹性纤维 C.胶原纤维 D.肌纤维
- 某中学高三(1)班举行了关于公民政治参与的主题交流活动。王敏说:我对政府工作提出过批评建议;张宇说:我参加过居民委员会的
- 已知关于x的不等式组有解,求实数a的取值范围,并写出该不等式组的解集.
- 前594年,梭伦当选为执政官,开始民主改革。政治上,他将雅典公民分为四个等级,分享不同的权利与义务。由此在雅典确立了A
- 下列叙述正确的是A.用稀NaOH清洗沾到皮肤上的苯酚B.Na2CO3溶液保存在带玻璃塞的试剂瓶中C.配制FeCl3溶液时
- ---Are Mr. and Mrs. Wang living alone in the house? ---Yes,
- 下列仪器名称正确的是 A
- 计算:a(a+1)=
- 2010年7月,四川省广安市广安区发生了160年以来特大洪水,广安区城北新南门、厚街、政府大道、北门口、体育场等沿江一带
- .如图,∠A=∠B,AE=BE,点D在AC边上,∠1=∠2,AE和BD相交于点O.(1)求证:△AEC≌△BED;(2)
- 为弘扬“大众创业万众创新”精神,激发群众创业创新热情,某县工商局积极发挥职能作用,部署启动了“大众创业万众创新”先进典型
- To our surprise the stranger _____ to be an old friend of my
- 发电站通过升压变压器、输电导线和降压变压器把电能输送到用户(升压变压器和降压变压器可视为理想变压器). (1)画出上述输
- 阅读下面文言文,完成后面题目。 【甲】出师表(节选) 先帝创业未半而中道崩殂,今天下三分,益州疲弊,此诚危急存亡之秋也。
- 在图所示的电路中,电流表的量程为0~0.6A,电压表的量程为0~15V,R0=36Ω,滑动变阻器的最大阻值为100Ω,电
- 为了制取氧气,实验室提供了以下药品和仪器装置. 【药品】①二氧化锰 ②氯酸钾 ③高锰酸钾 ④过氧化氢溶液(1)
- 有40g 5%的CaCl2溶液,若将其质量分数增大到10%,应采用的方法是A.把溶剂蒸发掉一半 B.加入40
- 在氢气和碘蒸气反应生成碘化氢的反应中,碘化氢的生成速率与碘的减少速率之比是( )。 A.1 :1 B.1 :
- 右图示甲状腺激素分泌调节示意图,图中TRH为促甲状腺激素释放激素。下列有关叙述错误的是 A.血液中TH过量时会抑制TRH



