实验1-3 污水处理--电浮选凝聚法 知识点题库
化学与生活密切相关,下列说法不正确的是( )
A . 为了防止食品受潮变质,常在食品包装袋中放入生石灰
B . 不可用铝制餐具长时间存放酸性或碱性食物
C . 明矾可用于净水
D . 为防止铁制品生锈,可以在铁制品的外层涂油漆或局部镀铜
2010年上海世博会,上海将有千辆氢燃料电池车上路,关于氢燃料电池下列说法不正确的是( )
A . 氢燃料电池是一种具有应用前景的绿色电源
B . 氢燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
C . 氢燃料电池能量转换率比氢气直接燃烧高
D . 氢燃料 电池工作时,发出淡蓝色火焰
如图的烧杯中盛的都是海水,铁在其中被腐蚀的速率由快到慢的顺序为( )
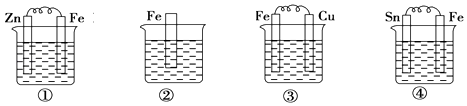
A . ③④②①
B . ③④①②
C . ④②①③
D . ②①③④
埋在地下的输油铸铁管道,在下列各种情况下被腐蚀速度最慢的是( )
A . 在含铁元素较多的酸性土壤中
B . 在潮湿疏松透气的土壤中
C . 在干燥致密不透气的土壤中
D . 在含碳粒较多、潮湿透气的土壤中
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O  3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A . 放电时负极反应为:Zn﹣2e+2OH=Zn(OH)2
B . 充电时阳极反应为:Fe(OH)3﹣3e+5OH﹣=FeO42﹣+4H2O
C . 放电时每转移3mol电子,正极有1molK2FeO4被氧化
D . 放电时正极附近溶液的碱性增强
下列叙述不正确的是( )
A . 金属腐蚀的本质是金属原子失去电子而被氧化
B . 钢铁吸氧腐蚀的正极反应是:O2+4e﹣+2H2O═4OH﹣
C . 将地下钢管与直流电源的正极相连,用来保护钢管
D . 氢氧燃料电池中,氢气在负极发生氧化反应
蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42﹣ 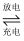 2PbSO4+2H2O请回答下列问题:已知硫酸铅不溶于水,放电时,该电池的负极反应为 Pb﹣2e﹣+SO42﹣═PbSO4 ,
2PbSO4+2H2O请回答下列问题:已知硫酸铅不溶于水,放电时,该电池的负极反应为 Pb﹣2e﹣+SO42﹣═PbSO4 ,
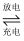 2PbSO4+2H2O请回答下列问题:已知硫酸铅不溶于水,放电时,该电池的负极反应为 Pb﹣2e﹣+SO42﹣═PbSO4 ,
2PbSO4+2H2O请回答下列问题:已知硫酸铅不溶于水,放电时,该电池的负极反应为 Pb﹣2e﹣+SO42﹣═PbSO4 ,
-
(1) 则正极的电极反应式是;
-
(2) 当外电路通过1mol电子时,理论上负极板的质量增加g.电解质溶液中溶质减少的物质的量为.
研究电化学腐蚀及防护的装置如图所示.下列有关说法正确的是( )
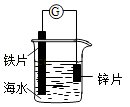
A . 锌片发生氧化反应作阴极
B . 电子从铁片经过导线流向锌片
C . 铁片上电极反应为:O2+2H2O+4e→4OH﹣
D . 该装置可用于研究外加电流阴极保护法
将两根铁钉分别缠绕铜丝和铝条,放人滴有混合溶液的容器中,如图所示,下列叙述错误的是( )
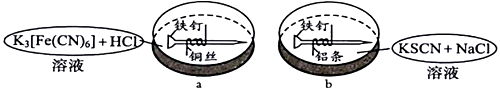
A . a中铁钉附近呈现蓝色沉淀
B . b中铁钉附近呈现红色
C . b中发生吸氧腐蚀
D . a中铜丝附近有气泡产生
全钒液流电池充电时间短,续航能力强,其充放电原理为VO2++V3++H2O 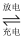 VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是( )
VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是( )
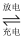 VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是( )
VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是( )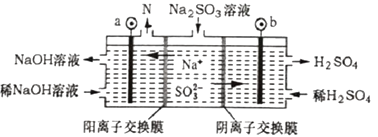
A . 全钒液流电池放电时,正极的电极反应式为VO2++2H++e-=VO2++H2O
B . 图中a电极为阴极,N物质是H2
C . 全钒液流电池充电时,V3+被氧化为VO2+
D . 电解时,b电极的反应式为SO32-+H2O-2e-=SO42-+2H+
如图所示是几种常见的化学电源示意图,有关说法正确的是( )
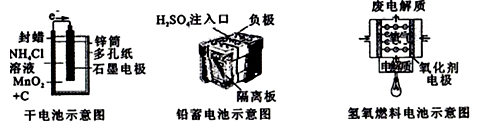
A . 上述电池分别属于一次电池、二次电池和燃料电池
B . 干电池工作时,H+向锌筒移动
C . 铅蓄电池工作过程中,每通过2 mol电子,负极质量减轻207g
D . 氢氧燃料电池的正极反应一定是O2+4e-+2H2O=4OH-
如下图所示装置中都盛有0.1 mol·L-1的NaCl溶液,放置一定时间后,装置中的四块相同的锌片腐蚀速率由快到慢的正确顺序是( )
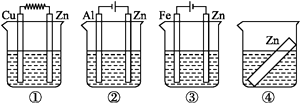
A . ③①④②
B . ①②④③
C . ①②③④
D . ②①④③
铅蓄电池是常见的二次电池,目前汽车上使用的电瓶大多数是铅蓄电池。已知铅蓄电池的电解质溶液为硫酸溶液,其充、放电按下式进行:Pb(s)+PbO2(s)+2H2SO4(aq) 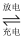 2PbSO4(s)+2H2O(l),下列有关该电池的说法正确的是( )
2PbSO4(s)+2H2O(l),下列有关该电池的说法正确的是( )
 2PbSO4(s)+2H2O(l),下列有关该电池的说法正确的是( )
2PbSO4(s)+2H2O(l),下列有关该电池的说法正确的是( )
A . 放电时,溶液中H+向PbO2电极迁移
B . 放电时,电路中转移0.2mol电子时Pb电极质量减小20.7g
C . 充电时,电解质溶液的pH增大
D . 充电时,阴极的电极反应式为:PbSO4+2H2O-2e-=PbO2+4H++SO42-
如何防止铁的锈蚀是工业上研究的重点内容。为研究铁的锈蚀,某同学做了探究实验,如下图所示,铁处于①②③三种不同的环境中
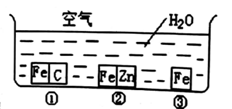
请回答:
-
(1) 金属腐蚀主要分为腐蚀和腐蚀两种。
-
(2) 铁被腐蚀的速率由快到慢的顺序是(填序号)。
-
(3) ①中正极的电极反应式为,②中负极的电极反应式为。
-
(4) 据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀可采取的措施有(填序号)。
①健身器材刷油漆 ②自行车钢圈镀铬
③将钢管用导线与铜条连接 ④将钢管用导线与碳棒连接
下图所示各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为( )
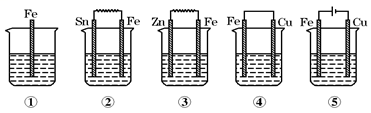
A . ⑤②①③④
B . ⑤④②①③
C . ④③②①⑤
D . ③②④①⑤
2018年10月24日港珠澳大桥正式通车。深埋在海水中的钢管桩易发生腐蚀,但中科院金属研究所研发的技术能保障大桥120年耐久性。下列保护钢管桩的措施不合理的是( )
A . 使用抗腐蚀性强的合金钢
B . 钢管桩附着铜以增强抗腐蚀性
C . 使用防止钢筋锈蚀的海工混凝土
D . 在钢筋表面覆盖一层高性能防腐涂料
化学与生产、生活密切相关,以下有关说法正确的是( )
A . 用CO2合成聚碳酸酯不可降解塑料,实现“碳”的循环利用
B . 绘制《山水画》所用的纸和墨的主要成分都是有机物
C . 纯银器表面在空气中逐渐变暗,是发生了电化学腐蚀
D . 海水是巨大的资源宝库,可以利用化学方法从海水中提取Br2、Mg等物质
2019年诺贝尔化学奖授予在锂离子电池研发领域作出贡献的三位科学家。下列对于锂离子电池所用材料分类错误的是( )
| | A | B | C | D |
| 正极(LiCoO2) | 负极(C) | 电解液(碳酸丙烯酯) | 隔膜(聚烯烃) | |
| 无机物 | 有机物 | 酯类 | 合成高分子 |
A . A
B . B
C . C
D . D
炒过菜的铁锅未及时洗净(残液中含  ),不久便会因被腐蚀而出现红褐色锈斑,腐蚀原理如图所示,下列说法正确的是( )
),不久便会因被腐蚀而出现红褐色锈斑,腐蚀原理如图所示,下列说法正确的是( )
 ),不久便会因被腐蚀而出现红褐色锈斑,腐蚀原理如图所示,下列说法正确的是( )
),不久便会因被腐蚀而出现红褐色锈斑,腐蚀原理如图所示,下列说法正确的是( ) 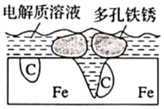
A . 腐蚀过程中,负极是  ,发生电极反应:
,发生电极反应: 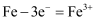 B .
B .  失去电子经电解质溶液转移给C
C . 正极的电极反应式为
失去电子经电解质溶液转移给C
C . 正极的电极反应式为 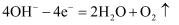 D . C是正极,
D . C是正极,  在C表面上发生还原反应
在C表面上发生还原反应
 ,发生电极反应:
,发生电极反应: 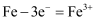 B .
B .  失去电子经电解质溶液转移给C
C . 正极的电极反应式为
失去电子经电解质溶液转移给C
C . 正极的电极反应式为 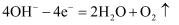 D . C是正极,
D . C是正极,  在C表面上发生还原反应
在C表面上发生还原反应
-
(1) I.种新型催化剂能使NO和CO发生反应:2NO+2CO
 2CO2+2N2。为研究化学反应速率的影响因素,在恒容条件下,某同学设计了三组实验,如表所示。
2CO2+2N2。为研究化学反应速率的影响因素,在恒容条件下,某同学设计了三组实验,如表所示。
2min末,c(NO)为6.0×10-4mol/L,则v(NO)=mol/(L·min) , v(N2)=mol/(L·min)。实验编号 t/℃ NO初始浓度/mol·L-1 CO初始浓度/mol·L-1 催化剂的比表面积/m2·g-1 I 280 1.20×10-3 5.80×10-3 82 II 280 1.20×10-3 5.80×10-3 124 III 350 1.20×10-3 5.80×10-3 82 -
(2) 下列选项中,能说明反应达到平衡的标志是____。A . 单位时间消耗
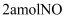 时,同时生成
时,同时生成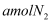 B .
B . 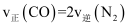 C . 容器内压强不再发生改变
D . 容器内气体的密度不再发生改变
C . 容器内压强不再发生改变
D . 容器内气体的密度不再发生改变
-
(3) 对比实验编号I和III,能验证对化学反应速率影响。下图是实验和(填实验编号)的对比。
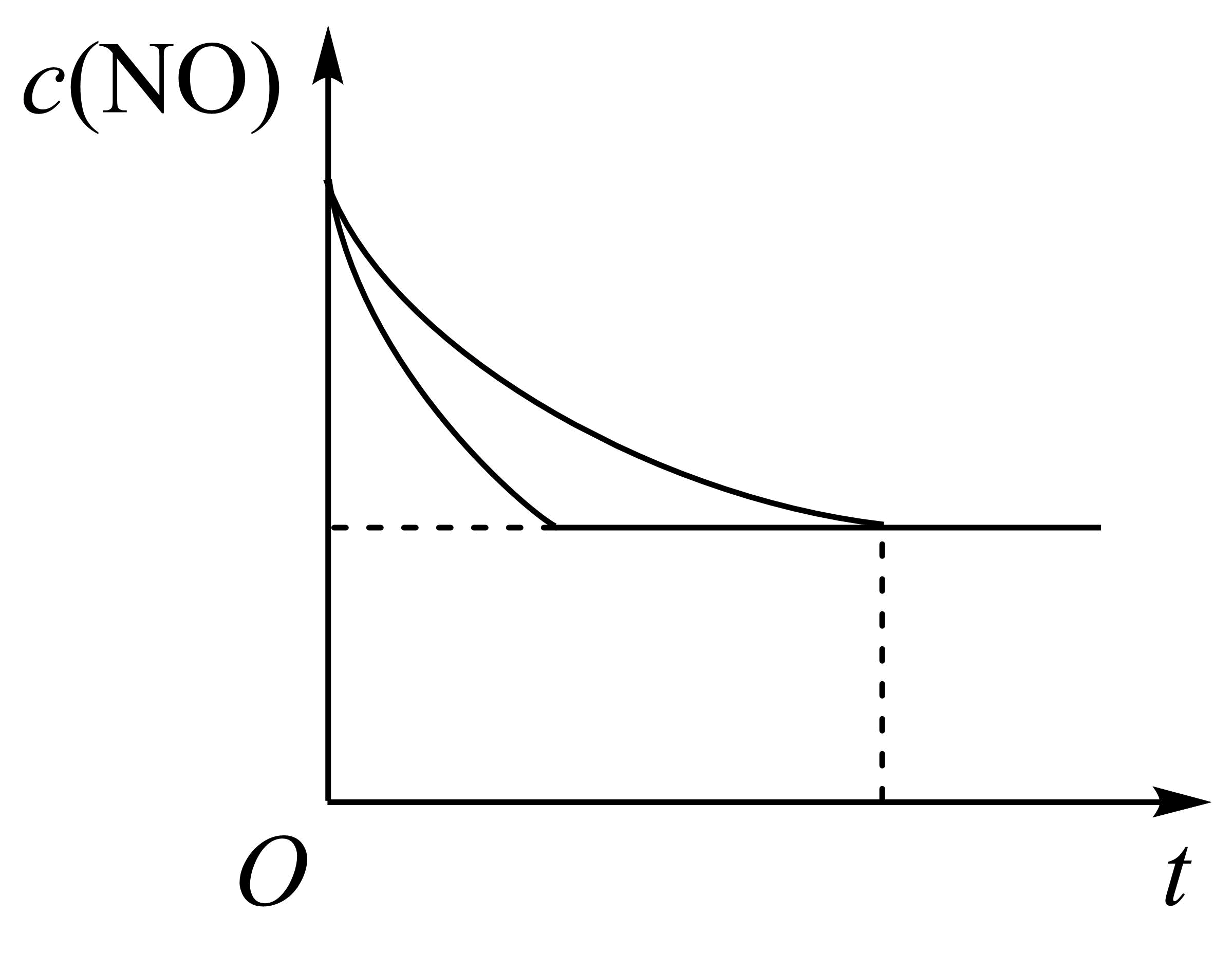
-
(4) II.知
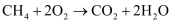 , 为了提高甲烷的能量利用率,可以把
, 为了提高甲烷的能量利用率,可以把 设计成燃料电池使用,如图所示,
设计成燃料电池使用,如图所示, 为质子交换膜,只允许
为质子交换膜,只允许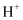 通过,回答下列问题。
通过,回答下列问题。
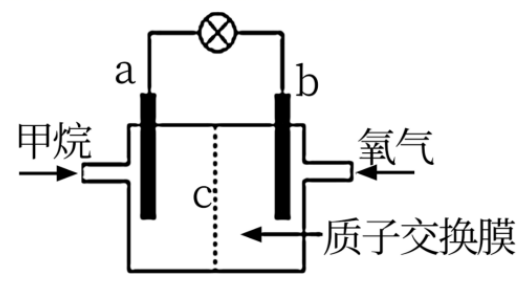
该燃料电池外电路的电流方向由到(填“a“b)。
-
(5)
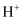 在电池内部电解质溶液中向(填“左”或“右”)移动。
在电池内部电解质溶液中向(填“左”或“右”)移动。
-
(6) a极反应方程式:。
-
(7) 在标准状况下,若每分钟通过质子交换膜的
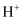 为
为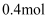 , 消耗甲烷的体积为L
, 消耗甲烷的体积为L
最近更新
- 下列说法正确的是 A.同温同压下,相同数目的分子必具有相同的体积 B.同温同压下,等体积的N2和CO的电子数相等 C.不
- 下列说法正确的是( ) A.化合反应一定是氧化反应 B.有氧气参加的反应一定是化合反应 C.糖和水混合制成糖水是化
- 图7是部分短周期元素化合价与原子序数的关系图,下列正确的是( ) A.原子半径:Z>Y>X B.气态氢化物的稳定性
- 我国最近从国外引进一套设备,它可以有效地消除“白色污染”。它把回收的废旧塑料经处理加工成汽油、煤油等。该加工过程的名称是
- 下图中,表示北半球高压的是: A.① B.② C.③ D.④
- 下列物质属于天体的是( ) ①卫星 ②吉林1号陨石③返回地面的神舟号宇宙飞船 ④按航线飞行的飞机 A、① B、①②
- 阅读下面材料,接要求答题。(共8分)材料一 据日本《朝日新闻》5月12日报道,根据日本文部科学省和美国能源部公布的最新核
- (—2.2)+3.8;
- 下列各种生理现象中,没有涉及到细胞间信息交流的是() A.精子与卵细胞的结合 B.肝细胞表面的糖蛋白结合胰岛素 C.吞噬
- 《子夜》中( )买办资本家,美国垄断资产阶级的走狗,并与蒋介石政权有很深的关系,他操纵着上海金融市场,故
- 一种新型熔融燃料电池因具有高发电效率而备受重视。现有Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通入CO气体,
- 下列词语中没有错别字的一组是:( ) A、精炼 如愿以偿 震慑 风靡一时 B、缉私 张灯结采 蔚蓝 前车之鉴 C、抵消
- 设函数。 (Ⅰ)求函数的最大值和最小正周期;w.w.w.k.s.5.u.c.o.m (Ⅱ)设A,B
- —Do you feel like __________out? —No. I’d rather we ___
- 如图所示是反映某种物质三种状态的微观模型。图乙中的物质为_态。某物质由图甲的状态直接变为图丙的状态时,发生的物态变化为
- 与酵母菌相比,硝化细菌具有的特点是w_w*w.k*s 5*u.c_o*m A.无线粒体,只能通过无氧呼吸获得能量 B.
- 岳阳山清水秀,文化底蕴丰厚,以下描绘能说明分子在作无规则运动的是A.洞庭湖,湖面波光闪烁B.君山竹,竹中泪痕斑斑C.毛尖
- 在建立血糖调节的模型活动中,甲同学持有2张“糖卡”(正面朝上),乙同学保管“胰高血糖素卡”和“胰岛素卡”,丙同学持有4张
- 盛夏天气炎热,小佳将奶茶喝掉一半后盖上盖子放入冰箱,一段时间后,她拿出奶茶瓶,发现奶茶全结成冰,请问奶茶结冰后不变的物理
- 下图是动物细胞有丝分裂和减数分裂过程,一个细胞中染色体数目变化规律的曲线和分裂过程中各分裂期之间的对应关系图,其中错误有