第一节 化学反应与能量变化 知识点题库
S(s)+O2(g)═SO2(g)△H2
Mn(s)+S(s)+2O2(g)═MnSO4(s)△H3
则下列表述正确的是( )
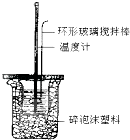
①量取反应物时,取50mL0.50mol•L﹣1的盐酸,还应加入的试剂是(填序号).
A.50mL0.50mol•L﹣1NaOH溶液
B.50mL0.55mol•L﹣1NaOH溶液
C.1.0gNaOH固体
②在该实验过程中,该同学需要测定的实验数据有(填序号).
A.盐酸的浓度 B.盐酸的温度
C.氢氧化钠溶液的浓度 D.氢氧化钠溶液的温度
E.水的比热容 F.反应后混合溶液的终止温度
③若用50mL0.5mol•L﹣1醋酸溶液代替上述盐酸测定中和热,所得数据.(填“偏大”或“偏小”或“不变”)
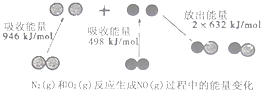

请回答下面问题:
-
(1) 用蒸馏水稀释0.1mol/L的醋酸溶液,下列选项中一定变小的是_____A . c(H+) B . c(H+)·c(OH-) C .
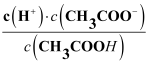
-
(2) CH3COONH4的水溶液呈 (选填 酸性”、“中性"或“碱性”)。
-
(3) 浓度为0.10 mol/L柠檬酸氢二钠(Na2HC6H5O7)溶液显酸性,通过计算说明其原因。
-
(4) 工业中常用碳酸镍制备氧化镍。已知:Ksp(NiCO3)=1.4×10-7 , 当 Ni , 2+恰好完全转化为NiCO3沉淀[即溶液中c(Ni2+)=1×10-5 mol·L-1]时,溶液中c(CO32-)=mol/L。
-
(5) II.乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。
2CO2(g)+6H2(g)
 CH3CH2OH (g)+3H2O(g) △H=a kJ/mol
CH3CH2OH (g)+3H2O(g) △H=a kJ/mol在一定压强下,测得.上述反应的实验数据如下表。
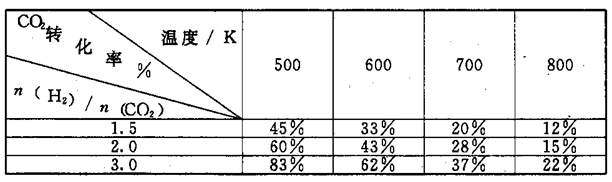
根据表中数据分析:
①上述反应的a0(填"大于”或“小于”)。
②在一定温度下.提高氢碳[即
 ]比,平衡常数K值(填“增大”、“减小”、或"不变”)。
]比,平衡常数K值(填“增大”、“减小”、或"不变”)。 -
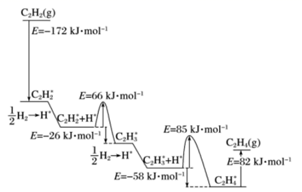
(6) 催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2 , 同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示;
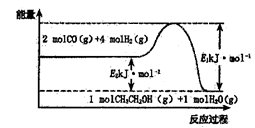
根据上图,写出反应的热化学方程式为。
 B . 化学反应中有物质变化也有能量变化
C . 需要加热的化学反应不一定是吸热反应
D . 化学键断裂吸收能量,化学键形成放出能量
B . 化学反应中有物质变化也有能量变化
C . 需要加热的化学反应不一定是吸热反应
D . 化学键断裂吸收能量,化学键形成放出能量
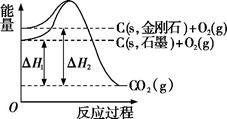
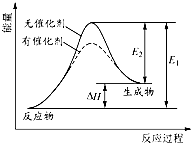
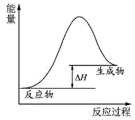 表示燃料燃烧反应的能量变化
B .
表示燃料燃烧反应的能量变化
B . 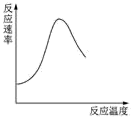 表示酶催化反应的反应速率随反应温度的变化
C .
表示酶催化反应的反应速率随反应温度的变化
C . 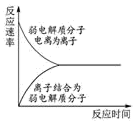 表示弱电解质在水中建立电离平衡的过程
D .
表示弱电解质在水中建立电离平衡的过程
D . 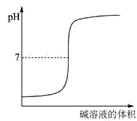 表示强碱滴定强酸的滴定曲线
表示强碱滴定强酸的滴定曲线
-
(1) 肼(N2H4 , N为-2价)和NO2是一种双组分火箭推进剂。两种物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,请写出上述反应的热化学方程式 。
-
(2) 已知下列热化学方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H1=-27.6kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=-58.8kJ/mol
Fe3O4(s)+CO(g)=3FeO(s) +CO2(g) △H3=+38.4kJ/mol
求以下热化学方程式的焓变
FeO(s)+CO(g)=Fe(s)+CO2(g) △H=。
-
(3) Ⅰ.已知:P4(s)+6Cl2(g) =4PCl3(g) △H=a kJ·mol-1 ,
P4(s)+10Cl2(g) =4PCl5(g) △H=bkJ·mol-1;
破坏PCl5中1molP-Cl键所需能量为ckJ,破坏PCl3中1molP-Cl键所需能量为1.2ckJ则破坏Cl2中1molCl-Cl键所需的能量为。
Ⅱ.已知拆开晶体硅中1molSi-Si键,二氧化硅固体中1molSi-O键,氧气中的1molO=O键分别需要提供a kJ、b kJ、c kJ能量,请写出晶体硅与氧气反应生成二氧化硅固体的热化学方程式: 。
-
(1) Ⅰ.化学上采用
 处理
处理  不仅可以消除污染,还可作为工业生产的能量来源。
不仅可以消除污染,还可作为工业生产的能量来源。 工业上可采用
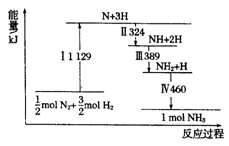
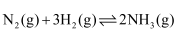 的方法合成氨。我国学者采用量子力学方法,通过计算机模拟,研究了在催化剂表面上合成氨的反应历程。图1为各步反应的能量变化示意图,其中“吸”表示各气态物质在催化剂表面吸附。
的方法合成氨。我国学者采用量子力学方法,通过计算机模拟,研究了在催化剂表面上合成氨的反应历程。图1为各步反应的能量变化示意图,其中“吸”表示各气态物质在催化剂表面吸附。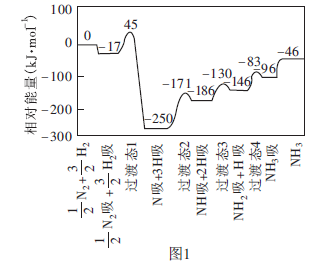
①该反应历程中正反应的最大活化能为
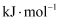 。
。②合成氨反应的热化学方程式为。
-
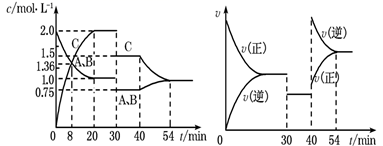
(2) 不同温度下,向三个容器中分别投入相同量的反应物进行反应,测得不同压强下平衡混合物中
 的物质的量分数如图2所示。
的物质的量分数如图2所示。 ①M点的
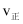 N点的
N点的 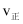 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。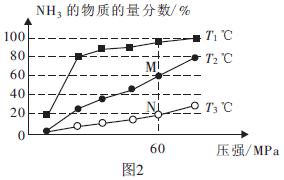
②
 ℃时,将
℃时,将 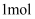
 和
和 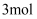
 充入2L的密闭容器中,维持压强为60MPa不变,达到N点的平衡状态,化学平衡常数K=
充入2L的密闭容器中,维持压强为60MPa不变,达到N点的平衡状态,化学平衡常数K= 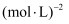 (用最简分数表示)。
(用最简分数表示)。 -
(3) Ⅱ.废水中的氮常以含氮有机物、氨、硝酸盐及亚硝酸盐等形式存在。
①用次氯酸钠除去氨氮(以
 示)的原理如图3所示。写出总反应的化学方程式:。
示)的原理如图3所示。写出总反应的化学方程式:。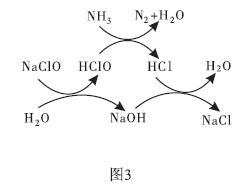
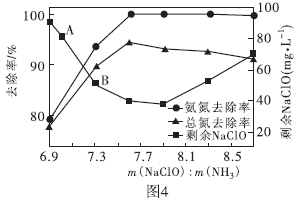
②取一定量的含氨氮废水,改变加入次氯酸钠的用量,反应相同时间后,溶液中氨氮去除率、总氮(溶液中所有可溶性的含氮化合物中氮元素的总量)去除率以及剩余次氯酸钠的含量随
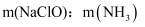 的变化情况如图4所示。当
的变化情况如图4所示。当 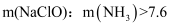 时,水体中总氮去除率反而下降,可能的原因是。
时,水体中总氮去除率反而下降,可能的原因是。 -
(4) 近年来,水体中的硝酸盐含量不断增加。工业上去除废水中硝酸盐的方法是采用电解法将
 转化为
转化为  ,部分装置如图5所示。
,部分装置如图5所示。 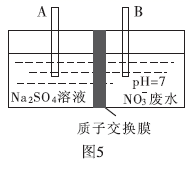
①B电极的电极反应式是.
②常温下,除去10L废水中的
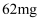
 后,最终废水的
后,最终废水的 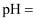 (电解前后废水的体积变化忽略不计)。
(电解前后废水的体积变化忽略不计)。
 NH3 (g) △H>0
NH3 (g) △H>0
下列说法中正确的是( )
-
(1) 铬元素可表现出多种颜色,如
 (黄),
(黄), (橙),Cr2+(蓝)等。室温下,Na2Cr2O7溶于水时发生的离子方程式为,若增强溶液酸性,溶液的颜色会(填“不变”“变黄”或“变橙”)
(橙),Cr2+(蓝)等。室温下,Na2Cr2O7溶于水时发生的离子方程式为,若增强溶液酸性,溶液的颜色会(填“不变”“变黄”或“变橙”)
-
(2) 微波炉将电能转变成一定频率的微波穿透食物,食物内的极性分子(如水、脂肪、蛋白质、糖等)被吸引振荡而加热食物。将盛有牛奶的陶瓷杯放入微波炉加热,牛奶和杯子相比更易热的是。
-
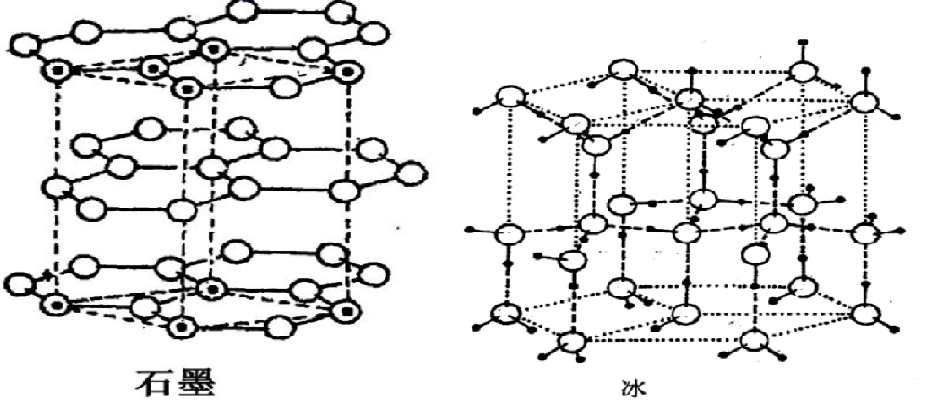
(3) 雪冰和石墨一般是六方晶系(如图)。1mol石墨碳原子含有的σ键数目是个,冰中平均每个水分子含有氢键的数目是,冰中的水分子排列方向是否相同(填“是”或“否”)。
-
(4) 钒催化剂参与SO2(g)+
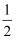 O2(g)
O2(g)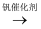 SO3(g) ΔH=−98kJ·mol−1反应的能量变化如图所示。SO3的VSEPR模型名称为,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:。
SO3(g) ΔH=−98kJ·mol−1反应的能量变化如图所示。SO3的VSEPR模型名称为,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:。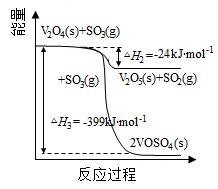
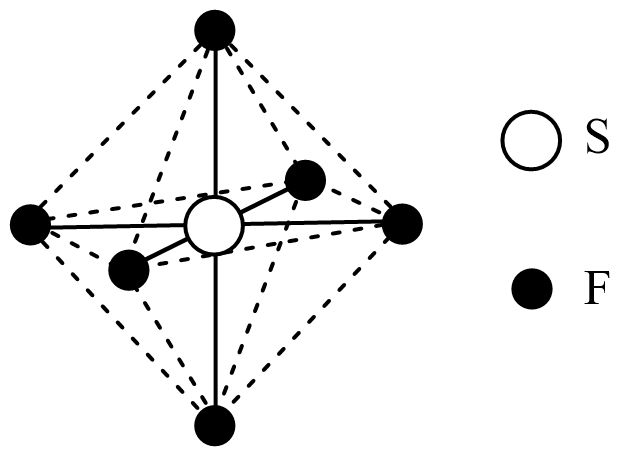
 的结构中只含有
的结构中只含有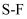 键,
键, 的结构如图所示,
的结构如图所示,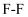 键、
键、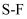 键的键能分别为
键的键能分别为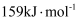 、
、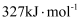 。
。
下列说法正确的是( )
 分子中每个原子的最外层都是8电子结构
B .
分子中每个原子的最外层都是8电子结构
B .  在氧气中燃烧生成
在氧气中燃烧生成 和
和 C .
C . 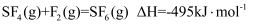 D .
D .  (g)中
(g)中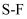 键的共用电子对偏向硫
键的共用电子对偏向硫
-
(1) (一)制备苯乙烯(原理如反应I所示):
Ⅰ.
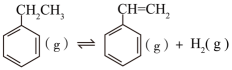 △H=+124kJ·mol-1
△H=+124kJ·mol-1部分化学键的键能如下表所示:
化学键
C-H
C-C
C=C
H-H
键能/ KJ/mol
412
348
X
436
根据反应I的能量变化,计算X=。
-
(2) 工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气。请用化学平衡理论解释通入水蒸气的原因:。
-
(3) 已知吉布斯自由能△G=△H-T△S ,当△G < 0时反应可自发进行。由此判断反应I在(填“高温”或“低温”)更易自发进行。
-
(4) (二)制备α-氯乙基苯(原理如反应Ⅱ所示):
Ⅱ.
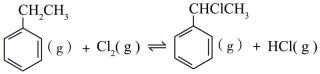 △H2>0
△H2>0T℃时,向10 L恒容密闭容器中充入2mol乙苯(g)和2 mol Cl2(g)发生反应Ⅱ,乙苯(或Cl2)、 α-氯乙基苯(或HCl)的物质的量浓度(c)随时间(t)变化的曲线如图所示:
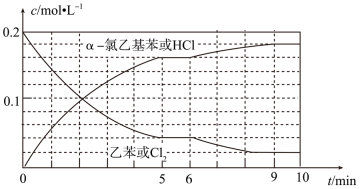
①0—2 min内,以HCl表示的该反应速率v(HCl)=。
②6 min时,改变的外界条件为,该条件下的平衡常数K的数值=。
③10 min时,保持其他条件不变,再向容器中充入1 mol乙苯、1 mol Cl2、1 molα-氯乙基苯和1mol HCl,则此时该反应v正v逆(填“>”、“<”或“=” );若12 min时反应再次达到平衡,则在0-12 min内,Cl2的转化率α=。(计算结果保留三位有效数字)
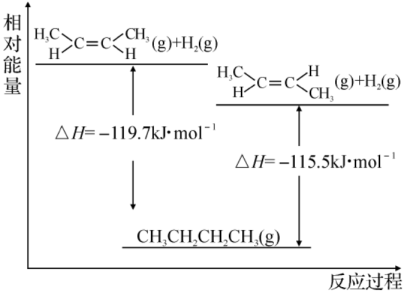
 C . 顺-2-丁烯转化为反-2-丁烯的过程属于物理变化
D . 完全燃烧等质量
C . 顺-2-丁烯转化为反-2-丁烯的过程属于物理变化
D . 完全燃烧等质量- 下列有关电池的说法不正确的是( )A.手机上用的锂离子电池属于二次电池B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电
- Don’tgive up halfway, Sandy. You’ll succeed ________ if you
- 2009年1月29日,温家宝总理在世界经济论坛发表讲话时指出,我国在面临外部需求明显收缩、部分行业产能过剩、经济增长下行
- 21.用水清洗一堆蔬菜上残留的农药.对用一定量的水清洗一次的效果作如下假定:用1个单位量的水可洗掉蔬菜上残留农药量的,用
- 下列各组混合物中,能用分液漏斗进行分离的是 A.醋酸和水 B.水和四氯化碳 C.碘和四氯化碳 D.汽油和
- 下列有关果酒制作的说法不正确的是 A. 酒精度数提高,红葡萄皮的色素进入发酵液,使葡萄酒呈现深红色 B. 用带盖的瓶子制
- 如图所示为简谐波在某时刻的波形图,图上a点和b点表示两个质点在此时刻的位移,它们的y坐标绝对值相同.对于两质点,下列判断
- 现有四个实验装置,若要验征绿色开花植物产生O需要光,为正确控制变量,则应选用的实验组合是: ( )A.①③
- 小行星带位于 A.木星和土星轨道之间 B.水星和金星轨道之间 C.金星和地球轨道之间
- 下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是A. a电极是负极B. b电极的电极反应为:4OH--4
- 如图所示,下列电路连接正确的是( )
- 下列物质的电子式书写正确的是①Ca(OH)2 ②H2S ③ OH﹣④Al3+ Al3+ ⑤N2 ⑥CO2 A. ①②③
- 甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图G3-5所示。下列说法正确的是()图G3-5 A.t1 ℃时,甲的溶解
- “”是“”的 ( )A.充分而不必要条件
- 19世纪中叶以后,中国逐渐被卷入资本主义世界体系。从人类文明演进的角度看,它对中国最主要的影响是() A.清政府统治土崩
- 下图曲线表示某生态系统中三个不同种群的生长繁衍情况。已知种群C是自养生物,下列说法不正确的是()A.该生态系统简单食物链
- 给下列加点字注音。 (1)壬戌( ) (2)举酒属客( ) (3)斗牛之间( ) (
- 从下列四张学习卡片上,你可以提炼的学习主题是 A.民族的交流与融合 B.国家的统一与发展C.对
- 如图33-6所示,光滑金属导轨AC、AD固定在水平面内,并处在方向竖直向下、大小为B的匀强磁场中,有一质量为m的导体棒以
- 仔细观察下面一幅漫画,根据要求回答问题。 高科技



