第一节 化学反应与能量变化 知识点题库
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ/mol,
C(s)+0.5O2(g)=CO(g)△H3=akJ/mol,则a=.
-
(1) 已知反应:H2(g)+
 O2(g)═H2O(g)△H1
O2(g)═H2O(g)△H1N2(g)+2O2═2NO2(g)△H2
 N2(g)+
N2(g)+ 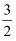 H2(g)═NH3(g)△H3
H2(g)═NH3(g)△H3利用上述三个反应,计算4NH3(g)+7O2(g)═4NO2(g)+6H2O(g)的反应焓变为 (用含△H1、△H2、△H3的式子表示).
-
(2) 已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ•mol﹣1
则以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:.
物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答下列问题:
-
(1) 下列物质本身具有的能量最低的是 (填字母代号).A . H2 B . Cl2 C . Br2 D . I2
-
(2) 下列氢化物中最稳定的是 (填字母代号).A . HCl B . HBr C . HI
-
(3) 1molCl2与足量的H2完全反应时(填“吸收”或“放出”)热量 kJ.
-
(1) I.研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)
 2NO(g) △H=+180.50kJ·mol-1
2NO(g) △H=+180.50kJ·mol-12CO(g)+O2(g)
 2CO2(g) △H=-566.00 kJ·mol-1
2CO2(g) △H=-566.00 kJ·mol-1为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式 。
-
(2) II.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)
 CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2 , 在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2 , 在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。 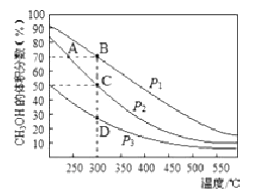
①该反应的反应热△H 0(填“>”或“<”),压强的相对大小与P1P2(填“>”或“<”)。
②该反应化学平衡常数表达式为。
③下列各项中,不能说明该反应已经达到平衡的是。
A.容器内气体压强不再变化
B.v(CO):v(H2):v(CH3OH)=1:2:1
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
④某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
-
(3) III.依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。
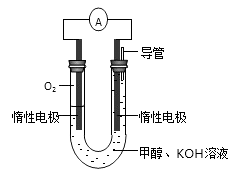
负极电极反应式为。
-
(1) I.在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2混合气体,2 min后,反应达到平衡,生成SO3气体0.5 mol,同时放出热量Q kJ。回答下列问题
写出该反应的热化学方程式为。
-
(2) 在该条件下,反应前后容器的体积之比为。
-
(3) ①若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)0.5mol(填 “大于”、“小于”或“等于”);
②若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量Q kJ(填 “大于”、“小于”或“等于”)。
-
(4) II. 用焦炭还原NO2的反应为:2NO2(g)+2C(s )
 N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示: 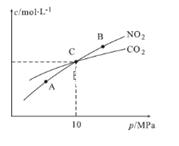
A、B两点的浓度平衡常数关系:Kc(A)Kc(B) (填 “﹥”、“<”或“﹦”)。
-
(5) A,B,C三点中NO2的转化率最高的是(填“A”或“B”或“C”)点。
-
(6) 计算C点时该反应的压强平衡常数Kp(C)=(Kp是用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
-
(1) 0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧的热化学方程式。
-
(2) 通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。下表是一些化学键的键能。
化学键
C-H
C-F
H-F
F-F
键能kJ/mol
414
489
565
155
根据键能数据估算下列反应:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反应热△H为。
-
(3) 1840年瑞士的化学家盖斯(Hess)在总结大量实验事实(热化学实验数据)的基础上提出:“定压或定容条件下的任意化学反应,在不做其它功时,不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
请写出CO还原FeO的热化学方程式:。
-
(4) 在恒温(500K)、体积为1.0L 的密闭容器中通入1.0 mol N2和1.0 mol H2发生合成氨反应N2 + 3H2
 2NH3 , 20 min 后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,该反应的热化学方程式为。
2NH3 , 20 min 后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,该反应的热化学方程式为。
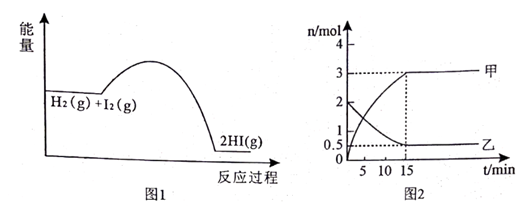
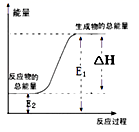
在容积为2L的恒温恒容密闭容器中通入2molH2和b molI2蒸气,反应过程的能量变化如图1所示,部分物质的物质的量随反应时间的变化关系如图2所示。
-
(1) 由图1中曲线变化可知,该反应为(填“放热”或“吸热”)反应;
-
(2) 图2中甲为;
-
(3) 试写出该反应的化学方程式:;
-
(4) 从反应开始到平衡,反应速率v(H2)=;
-
(5) 反应达到平衡时,H2的转化率为;
-
(6) 当b= 时,H2与I2的转化率相等;
-
(7) 5min时,v正(H2) v逆(H2)(填“>”、“<”或“=”);
-
(8) 下列叙述能说明该反应已达到平衡状态的是 。A . v正(HI)=2v逆(I2) B . 反应速率:v(H2)=v(I2)=0.5v(HI) C . 一个H-H键断裂的同时有两个H-I键断裂 D . 温度和体积一定时,某一生成物浓度不再变化 E . 温度和体积一定时,混合气体的颜色不再发生变化 F . 温度和体积一定时,混合气体的平均相对分子质量不再变化 G . 温度和压强一定时,混合气体的密度不再发生变化
-
(1) A、B两种元素的元素符号:A、B。
-
(2) 由A、Z所形成的化合物A2Z的电子式是,化合物类型是 (填“离子化合物”或“共价化合物”)。
-
(3) 由A、Y两元素形成的四核18电子的化合物的电子式为,结构式为 ,由A、Y、B所形成的化合物AYB的电子式是, 存在的化学键。
-
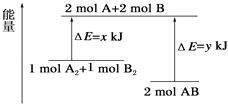
(4) 化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是___________。
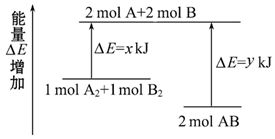 A . 该反应是放热反应 B . 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 C . 断裂2 mol A-B键需要吸收y kJ的能量 D . 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
A . 该反应是放热反应 B . 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 C . 断裂2 mol A-B键需要吸收y kJ的能量 D . 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
-
(1) 诺贝尔奖获得者埃特尔提出了合成氨反应吸附解离的机理,通过实验测得合成氨势能如图所示:
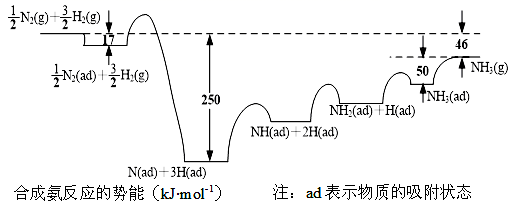
在合成氨吸附解离的过程中,下列状态最稳定的是 (填选项)。
A.
 B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)
B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)其中,NH3(ad)
 NH3(g) ∆H= kJ·mol-1 , 若要使该平衡正向移动,可采取的措施是(填选项)。
NH3(g) ∆H= kJ·mol-1 , 若要使该平衡正向移动,可采取的措施是(填选项)。A.升高温度 B.降低温度 C.增大压强 D.减小压强
-
(2) 在上述实验条件下,向一密闭容器中通入 1molN2和 3molH2充分反应,达到平衡时放出 46kJ 热量,计算该条件下 H2的转化率 。
-
(3) 在 t ℃、压强为 3.6 MPa 条件下,向一恒压密闭容器中通入氢氮比[c(H2):c(N2)] 为 3 的混合气体,体系中气体的含量与时间变化关系如图所示:
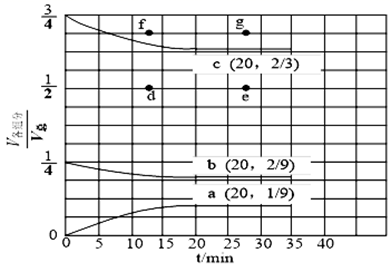
反应 20 min 达到平衡,试求 0~20 min 内氨气的平均反应速率 v(NH3)= MPa·min-1。若起始条件一样,在恒容容器中发生反应,则达到平衡时 H2的含量符合上图中 点(填“d”、“e”、“f”或“g”)。
-
(4) 在合成氨工艺中,未反应的气体(含不参与反应的惰性气体)可多次循环使用。当氢氮比[c(H2):c(N2)]为 3 时,平衡时氨气的含量关系式为:ω (NH3)=0.325·KP·P·(1-i ) 2 , (KP:平衡常数;P:平衡体系压强;i:惰性气体体积分数)。当温度为 500℃,不含惰性气体时,平衡体系压强为 2.4MPa,氨气的含量为 ω ,若此时增大压强,Kp 将(填“变大”、“变小”或“不变”)。若温度不变,体系中有 20%的惰性气体,欲使平衡时氨气的含量仍为 ω ,应将压强调整至 MPa。
-
(1) 目前海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,有关海洋中部分资源的利用如图所示,回答下列问题:
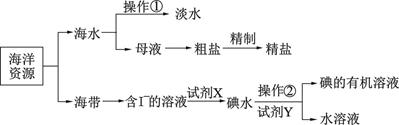
①实验室制取淡水常用的操作①是,操作②使用的玻璃仪器除了烧杯和玻璃棒之外必不可少的是。
②向含I-的溶液中加入试剂X的目的是使I-被氧化成I2 , 若X为硫酸酸化的H2O2溶液,写出该反应的离子方程式。
③下述物质中不可做试剂Y的是(填序号)
A 苯 B 乙醇 C 乙酸 D 四氯化碳
④我国从海水中直接获得的精盐还常常要添加(填序号)来预防地方甲状腺肿。
A 碘酸钾 B 碘单质 C 氯化钾
-
(2) 氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O
 2H2↑+O2↑。制得的氢气可用于燃料电池。
2H2↑+O2↑。制得的氢气可用于燃料电池。 ①分解海水的反应属于(填“放热”或“吸热”)反应,该化学反应中的氧气、氢气的总能量(填“>”、“=”或“<”)水的总能量。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-=2H2O B极:O2+4e-=2O2-
B极是电池的极,电子从该极(填“流入”或“流出”)。当消耗标况下氢气33.6L时,则导线中转移电子的物质的量为mol。
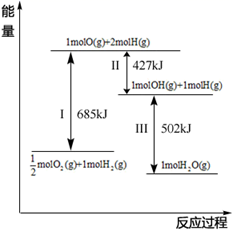
 B .
B . 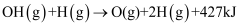 C .
C . 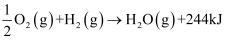 D .
D . 
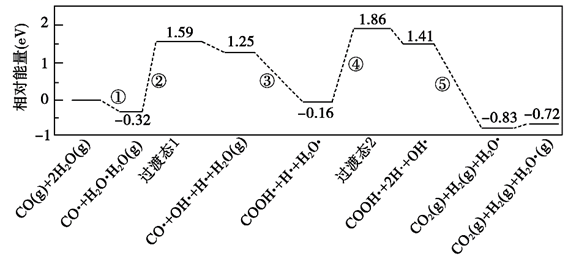
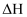 >0
B . 反应过程中发生非极性键的断裂与生成
C . 其他条件不变,使用另一高效催化剂可使CO的平衡转化率增大
D . 该历程中最大能垒(活化能)步骤的反应式为
>0
B . 反应过程中发生非极性键的断裂与生成
C . 其他条件不变,使用另一高效催化剂可使CO的平衡转化率增大
D . 该历程中最大能垒(活化能)步骤的反应式为 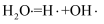
-
(1) 已知:2I2(s)+5O2(g)=2I2O5(s) △H1=-75.6 kJ/mol Ⅰ
I2O5(s)+5CO(g)
 5CO2(g)+I2(s) △H2=-1377.2 kJ/mol Ⅱ
5CO2(g)+I2(s) △H2=-1377.2 kJ/mol Ⅱ则表示CO燃烧热的热化学方程式为。
-
(2) 结合反应Ⅰ和反应Ⅱ分析,
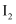 在CO转化为CO2的反应中所起的作用是。
在CO转化为CO2的反应中所起的作用是。
-
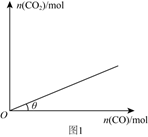
(3) 10℃时,某恒容密闭容器中充有足量的I2O5 , 向该容器中充入CO发生反应Ⅱ,平衡时CO2与充入CO的物质的量关系如图1所示。若降低温度,θ值(填“增大”“减小”或“不变”,下同);压缩容器体积,θ值。
-
(4) 20℃时向装有足量I2O5的2L恒容密闭容器中充入2mol CO,反应达到平衡后固体质量减小8 g。
①该温度下反应的平衡常数K=(可用分数表示)。
②图2是CO的平衡转化率随CO2的移出率[
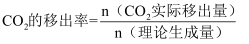 ×100%]关系。则图中a=,b=。
×100%]关系。则图中a=,b=。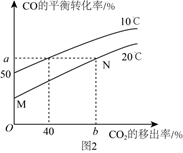
③由M点变为N点耗时5min,则该段时间内的平均反应速率v(CO)=。
-
(1) 火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=−534 kJ∙mol−1
H2O2(l)=H2O(l)+
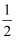 O2(g) ΔH=−98 kJ∙mol−1
O2(g) ΔH=−98 kJ∙mol−1H2O(l)=H2O(g) ΔH=44 kJ∙mol−1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式:。
-
(2) 反应的自发性由焓变和熵变两个因素决定。N2(g)+O2(g)=2NO(g),已知N≡N的键能为946 kJ∙mol−1 , O=O键的键能为498 kJ∙mol−1 , N≡O的键能为630 kJ∙mol−1;该反应的ΔH=,其反应自发的原因是。
-
(3) 电动汽车的电源常以乙醇(CH3CH2OH)为燃料的固体燃料电池,以熔融的氧化物为电解质,其高温下能传导O2− , 写出负极的电极反应式。
-
(4) 以纯铜作阴极,以石墨作阳极,电解某浓度的硫酸铜溶液,阴极产物均附在电极上,通电一段时间后,关闭电源,迅速撤去电极(设阴极产物没有损耗),若在电解后的溶液中加入16.0gCuO固体,则恰好能使溶液恢复到原浓度,则整个电解过程中,所产生的气体体积为(标准状况)L。
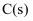 的燃烧热是-
的燃烧热是-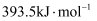 , 则
, 则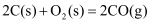 的
的 B . 由C(石墨,s)
B . 由C(石墨,s) C(金刚石,s)
C(金刚石,s) 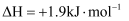 可知金刚石比石墨稳定
C . 同温同压下,
可知金刚石比石墨稳定
C . 同温同压下, 在光照和点燃条件下
在光照和点燃条件下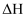 不相同
D . 在稀溶液中:
不相同
D . 在稀溶液中: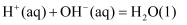
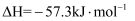 , 若将含2
, 若将含2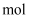
 与含2
与含2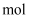
 的稀溶液混合,放出的热量小于114.6
的稀溶液混合,放出的热量小于114.6
- 根据阅读体验,回答问题。 “你(阿廖沙)昨天怎么把牛奶瓶子打破了?你小点声说!”她说话好似在用心地唱歌,字字句句都像鲜花
- An unemployed man is desperate to support his family. His wi
- 下列说法不存在因果关系的是() A.钠容易与空气中的水蒸气和氧气反应,所以钠保存在煤油中 B.碳酸氢钠和碳酸钠的水溶液都
- 阅读下列材料,结合所学知识回答下列问题。 材料一 自然法之父西塞罗说:“执政官乃是会说话的法律,而法律是不会说话的执政官
- Living in thedesert involves a lot of problems, waters
- 在△ABC中,已知cosA=,sinB=,则cosC= ( ) A. B. C
- 向0.10 mol·L-1 H2SO3溶液中逐滴加入0.10 mol·L-1 HNO3溶液,下列所表示的关系正确的是(x
- 1998 葡萄牙 里斯本 海洋—未来的财富 1999 中国 云南 人与自然—迈向21世纪 2000 德国 汉诺威 人类—
- 已知向量,,若,则的最小值( ) A. B.6 C.12 D.
- 下列语句中,没有错别字的一项是( ) A.江湖险恶,人生路上,陷阱重重,千万不可掉以清心,马马虎虎。 B.由于患
- 阅读下面的文言文,完成后面题。 刘平字公子,楚郡彭城人也。王莽时为郡更,政教①大行。其后每属县有剧贼,辄令平守之,所至皆
- 已知函数f(x)=axln x,x∈(0,+∞),其中a>0且a≠1,f′(x)为f(x)的导函数,若f′(1)=3,则
- 如果采用样方法调查某地区(甲地)蒲公英的种群密度,下列做法中正确的是 ( ) A.计数甲地内蒲公英的
- “空谈误国,实干兴邦”,实干首先就要脚踏实地地劳动。这是因为 ①世界的本质是物质 ②思维与
- 已知ABCD-A1B1C1D1是棱长为2的正方体,E、F分别为BB1和DC的中点,建立适当的空间直角坐标系,试写出图中各
- 下列物质分类的正确组合是( ) 选项 酸 碱 碱性氧化物 盐 A H2CO3 纯碱 CaO 明矾 B H2SO4 烧
- 自节假日高速公路免费通行方案出台后,节假日期间越来越多的游客选择“自驾游”。于是,许多经营客运的汽车运输公司纷纷减少发往
- Don’t worry. I’m sure your children will _______ (渐渐地) learn
- He is my father and I know he will forgive me for _______ I
- -Doyou know tomorrow morning? -Sorry. Let’s go and



