第一节 化学反应与能量变化 知识点题库
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJ/mol,
C(s)+0.5O2(g)=CO(g)△H3=akJ/mol,则a=.
-
(1) 已知反应:H2(g)+
 O2(g)═H2O(g)△H1
O2(g)═H2O(g)△H1N2(g)+2O2═2NO2(g)△H2
 N2(g)+
N2(g)+ 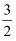 H2(g)═NH3(g)△H3
H2(g)═NH3(g)△H3利用上述三个反应,计算4NH3(g)+7O2(g)═4NO2(g)+6H2O(g)的反应焓变为 (用含△H1、△H2、△H3的式子表示).
-
(2) 已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ•mol﹣1
则以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:.
物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答下列问题:
-
(1) 下列物质本身具有的能量最低的是 (填字母代号).A . H2 B . Cl2 C . Br2 D . I2
-
(2) 下列氢化物中最稳定的是 (填字母代号).A . HCl B . HBr C . HI
-
(3) 1molCl2与足量的H2完全反应时(填“吸收”或“放出”)热量 kJ.
-
(1) I.研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)
 2NO(g) △H=+180.50kJ·mol-1
2NO(g) △H=+180.50kJ·mol-12CO(g)+O2(g)
 2CO2(g) △H=-566.00 kJ·mol-1
2CO2(g) △H=-566.00 kJ·mol-1为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式 。
-
(2) II.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)
 CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2 , 在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2 , 在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。 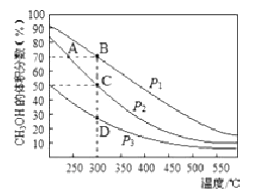
①该反应的反应热△H 0(填“>”或“<”),压强的相对大小与P1P2(填“>”或“<”)。
②该反应化学平衡常数表达式为。
③下列各项中,不能说明该反应已经达到平衡的是。
A.容器内气体压强不再变化
B.v(CO):v(H2):v(CH3OH)=1:2:1
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
④某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
-
(3) III.依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。
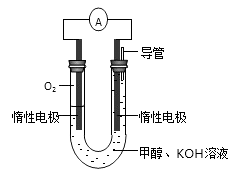
负极电极反应式为。
-
(1) I.在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2混合气体,2 min后,反应达到平衡,生成SO3气体0.5 mol,同时放出热量Q kJ。回答下列问题
写出该反应的热化学方程式为。
-
(2) 在该条件下,反应前后容器的体积之比为。
-
(3) ①若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)0.5mol(填 “大于”、“小于”或“等于”);
②若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量Q kJ(填 “大于”、“小于”或“等于”)。
-
(4) II. 用焦炭还原NO2的反应为:2NO2(g)+2C(s )
 N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示: 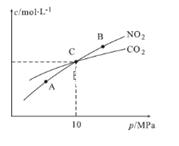
A、B两点的浓度平衡常数关系:Kc(A)Kc(B) (填 “﹥”、“<”或“﹦”)。
-
(5) A,B,C三点中NO2的转化率最高的是(填“A”或“B”或“C”)点。
-
(6) 计算C点时该反应的压强平衡常数Kp(C)=(Kp是用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
-
(1) 0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧的热化学方程式。
-
(2) 通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。下表是一些化学键的键能。
化学键
C-H
C-F
H-F
F-F
键能kJ/mol
414
489
565
155
根据键能数据估算下列反应:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反应热△H为。
-
(3) 1840年瑞士的化学家盖斯(Hess)在总结大量实验事实(热化学实验数据)的基础上提出:“定压或定容条件下的任意化学反应,在不做其它功时,不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
请写出CO还原FeO的热化学方程式:。
-
(4) 在恒温(500K)、体积为1.0L 的密闭容器中通入1.0 mol N2和1.0 mol H2发生合成氨反应N2 + 3H2
 2NH3 , 20 min 后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,该反应的热化学方程式为。
2NH3 , 20 min 后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,该反应的热化学方程式为。
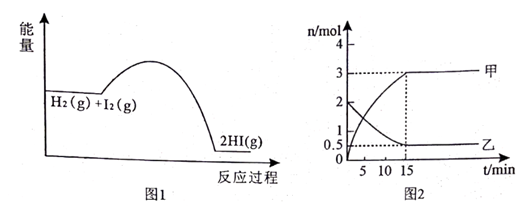
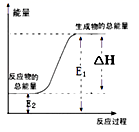
在容积为2L的恒温恒容密闭容器中通入2molH2和b molI2蒸气,反应过程的能量变化如图1所示,部分物质的物质的量随反应时间的变化关系如图2所示。
-
(1) 由图1中曲线变化可知,该反应为(填“放热”或“吸热”)反应;
-
(2) 图2中甲为;
-
(3) 试写出该反应的化学方程式:;
-
(4) 从反应开始到平衡,反应速率v(H2)=;
-
(5) 反应达到平衡时,H2的转化率为;
-
(6) 当b= 时,H2与I2的转化率相等;
-
(7) 5min时,v正(H2) v逆(H2)(填“>”、“<”或“=”);
-
(8) 下列叙述能说明该反应已达到平衡状态的是 。A . v正(HI)=2v逆(I2) B . 反应速率:v(H2)=v(I2)=0.5v(HI) C . 一个H-H键断裂的同时有两个H-I键断裂 D . 温度和体积一定时,某一生成物浓度不再变化 E . 温度和体积一定时,混合气体的颜色不再发生变化 F . 温度和体积一定时,混合气体的平均相对分子质量不再变化 G . 温度和压强一定时,混合气体的密度不再发生变化
-
(1) A、B两种元素的元素符号:A、B。
-
(2) 由A、Z所形成的化合物A2Z的电子式是,化合物类型是 (填“离子化合物”或“共价化合物”)。
-
(3) 由A、Y两元素形成的四核18电子的化合物的电子式为,结构式为 ,由A、Y、B所形成的化合物AYB的电子式是, 存在的化学键。
-
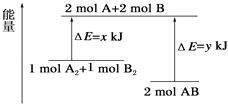
(4) 化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是___________。
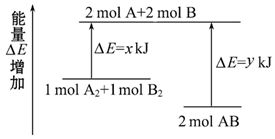 A . 该反应是放热反应 B . 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 C . 断裂2 mol A-B键需要吸收y kJ的能量 D . 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
A . 该反应是放热反应 B . 断裂1 mol A-A键和1 mol B-B键能放出x kJ能量 C . 断裂2 mol A-B键需要吸收y kJ的能量 D . 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
-
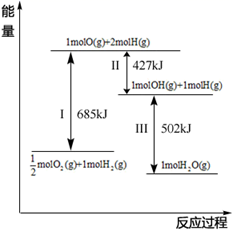
(1) 诺贝尔奖获得者埃特尔提出了合成氨反应吸附解离的机理,通过实验测得合成氨势能如图所示:
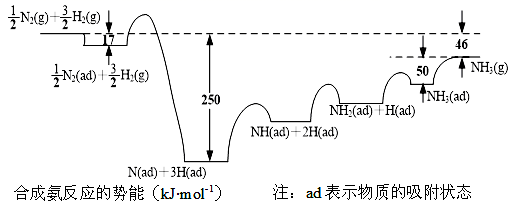
在合成氨吸附解离的过程中,下列状态最稳定的是 (填选项)。
A.
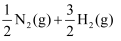 B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)
B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)其中,NH3(ad)
 NH3(g) ∆H= kJ·mol-1 , 若要使该平衡正向移动,可采取的措施是(填选项)。
NH3(g) ∆H= kJ·mol-1 , 若要使该平衡正向移动,可采取的措施是(填选项)。A.升高温度 B.降低温度 C.增大压强 D.减小压强
-
(2) 在上述实验条件下,向一密闭容器中通入 1molN2和 3molH2充分反应,达到平衡时放出 46kJ 热量,计算该条件下 H2的转化率 。
-
(3) 在 t ℃、压强为 3.6 MPa 条件下,向一恒压密闭容器中通入氢氮比[c(H2):c(N2)] 为 3 的混合气体,体系中气体的含量与时间变化关系如图所示:
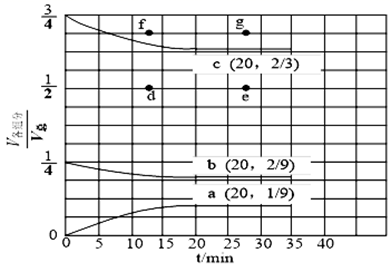
反应 20 min 达到平衡,试求 0~20 min 内氨气的平均反应速率 v(NH3)= MPa·min-1。若起始条件一样,在恒容容器中发生反应,则达到平衡时 H2的含量符合上图中 点(填“d”、“e”、“f”或“g”)。
-
(4) 在合成氨工艺中,未反应的气体(含不参与反应的惰性气体)可多次循环使用。当氢氮比[c(H2):c(N2)]为 3 时,平衡时氨气的含量关系式为:ω (NH3)=0.325·KP·P·(1-i ) 2 , (KP:平衡常数;P:平衡体系压强;i:惰性气体体积分数)。当温度为 500℃,不含惰性气体时,平衡体系压强为 2.4MPa,氨气的含量为 ω ,若此时增大压强,Kp 将(填“变大”、“变小”或“不变”)。若温度不变,体系中有 20%的惰性气体,欲使平衡时氨气的含量仍为 ω ,应将压强调整至 MPa。
-
(1) 目前海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,有关海洋中部分资源的利用如图所示,回答下列问题:
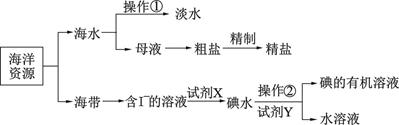
①实验室制取淡水常用的操作①是,操作②使用的玻璃仪器除了烧杯和玻璃棒之外必不可少的是。
②向含I-的溶液中加入试剂X的目的是使I-被氧化成I2 , 若X为硫酸酸化的H2O2溶液,写出该反应的离子方程式。
③下述物质中不可做试剂Y的是(填序号)
A 苯 B 乙醇 C 乙酸 D 四氯化碳
④我国从海水中直接获得的精盐还常常要添加(填序号)来预防地方甲状腺肿。
A 碘酸钾 B 碘单质 C 氯化钾
-
(2) 氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O
 2H2↑+O2↑。制得的氢气可用于燃料电池。
2H2↑+O2↑。制得的氢气可用于燃料电池。 ①分解海水的反应属于(填“放热”或“吸热”)反应,该化学反应中的氧气、氢气的总能量(填“>”、“=”或“<”)水的总能量。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-=2H2O B极:O2+4e-=2O2-
B极是电池的极,电子从该极(填“流入”或“流出”)。当消耗标况下氢气33.6L时,则导线中转移电子的物质的量为mol。
 B .
B . 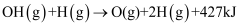 C .
C . 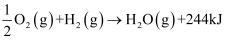 D .
D . 
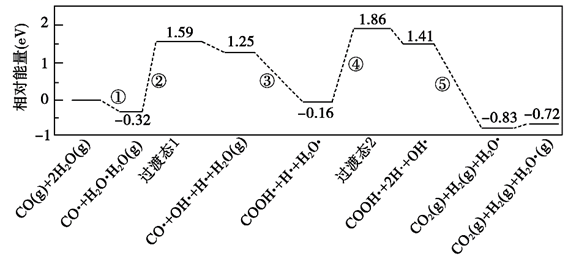
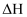 >0
B . 反应过程中发生非极性键的断裂与生成
C . 其他条件不变,使用另一高效催化剂可使CO的平衡转化率增大
D . 该历程中最大能垒(活化能)步骤的反应式为
>0
B . 反应过程中发生非极性键的断裂与生成
C . 其他条件不变,使用另一高效催化剂可使CO的平衡转化率增大
D . 该历程中最大能垒(活化能)步骤的反应式为 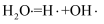
-
(1) 已知:2I2(s)+5O2(g)=2I2O5(s) △H1=-75.6 kJ/mol Ⅰ
I2O5(s)+5CO(g)
 5CO2(g)+I2(s) △H2=-1377.2 kJ/mol Ⅱ
5CO2(g)+I2(s) △H2=-1377.2 kJ/mol Ⅱ则表示CO燃烧热的热化学方程式为。
-
(2) 结合反应Ⅰ和反应Ⅱ分析,
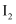 在CO转化为CO2的反应中所起的作用是。
在CO转化为CO2的反应中所起的作用是。
-
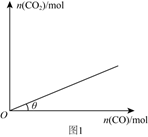
(3) 10℃时,某恒容密闭容器中充有足量的I2O5 , 向该容器中充入CO发生反应Ⅱ,平衡时CO2与充入CO的物质的量关系如图1所示。若降低温度,θ值(填“增大”“减小”或“不变”,下同);压缩容器体积,θ值。
-
(4) 20℃时向装有足量I2O5的2L恒容密闭容器中充入2mol CO,反应达到平衡后固体质量减小8 g。
①该温度下反应的平衡常数K=(可用分数表示)。
②图2是CO的平衡转化率随CO2的移出率[
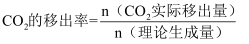 ×100%]关系。则图中a=,b=。
×100%]关系。则图中a=,b=。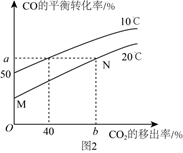
③由M点变为N点耗时5min,则该段时间内的平均反应速率v(CO)=。
-
(1) 火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=−534 kJ∙mol−1
H2O2(l)=H2O(l)+
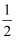 O2(g) ΔH=−98 kJ∙mol−1
O2(g) ΔH=−98 kJ∙mol−1H2O(l)=H2O(g) ΔH=44 kJ∙mol−1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式:。
-
(2) 反应的自发性由焓变和熵变两个因素决定。N2(g)+O2(g)=2NO(g),已知N≡N的键能为946 kJ∙mol−1 , O=O键的键能为498 kJ∙mol−1 , N≡O的键能为630 kJ∙mol−1;该反应的ΔH=,其反应自发的原因是。
-
(3) 电动汽车的电源常以乙醇(CH3CH2OH)为燃料的固体燃料电池,以熔融的氧化物为电解质,其高温下能传导O2− , 写出负极的电极反应式。
-
(4) 以纯铜作阴极,以石墨作阳极,电解某浓度的硫酸铜溶液,阴极产物均附在电极上,通电一段时间后,关闭电源,迅速撤去电极(设阴极产物没有损耗),若在电解后的溶液中加入16.0gCuO固体,则恰好能使溶液恢复到原浓度,则整个电解过程中,所产生的气体体积为(标准状况)L。
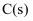 的燃烧热是-
的燃烧热是-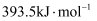 , 则
, 则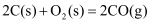 的
的 B . 由C(石墨,s)
B . 由C(石墨,s) C(金刚石,s)
C(金刚石,s) 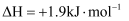 可知金刚石比石墨稳定
C . 同温同压下,
可知金刚石比石墨稳定
C . 同温同压下, 在光照和点燃条件下
在光照和点燃条件下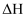 不相同
D . 在稀溶液中:
不相同
D . 在稀溶液中: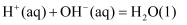
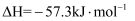 , 若将含2
, 若将含2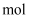
 与含2
与含2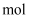
 的稀溶液混合,放出的热量小于114.6
的稀溶液混合,放出的热量小于114.6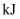
- 读下图“美国田纳西河流域的综合开发与治理示意图”,完成该河流域开发的中心环节是A.发电 B.防洪 C.养
- 硅及其化合物在材料领域中应用广泛。下列说法正确的是() A.硅酸钠可用于制备木材防火剂 B.硅单质广泛用于光纤通讯 C.
- 2013年“十一”长假期间,李丽同学随父母来海滨旅游。当她面朝大海,长发在海风吹拂下向后飘起时,切实感受到惬意舒畅的心情
- 民主是指在一定阶级范围内,按照少数服从多数的原则和平等原则来共同管理国家事务的国家制度。这里的“一定阶级”是指( )
- 复数(m2-5m+6)+(m2-3m)i是纯虚数,则实数m的值是( ) A.3 B.2
- 图5和图6表示黑龙江省同江市(位于松花江与黑龙江的交汇处)沼泽、耕地及人口的变化,据此完成下面试题。关于图5与图6关系的
- 下图表示细胞中一种常见的水解反应。 下列化合物能发生此种反应的有( )①多肽 ②淀粉 ③纤维素
- 朱熹说:“理生万物”,“未有此气,已有此理”。这说明他认为世界的本原是 A.主观精神 B.客观精神
- 阅读下面的文字,根据要求作文。(60分) 校园一隅,阳台一角,小路尽头……平时阳光难至,偏僻无人问津;有些人群也是如此,
- 阅读下面的文字,完成12―15题。中国历史上一场最大的是非垓下一战,项羽的人生之路走到了尽头,而他的命运的悲剧性的显露也
- 商务印书馆出版的第六版《现代汉语词典》新增“洋插队、新能源、电子污染、北漂、贪腐”等词语3000个,真实记录了当代的社会
- 阅读以下材料,回答问题知 材料一 “行仁政而王,莫之能御也。” “处无为之事,行不言之教。”两
- “”是“方程有两个负实数根”的( ). A.充分不必要条件 B.必要不充分条件 C.充要条件 D.既不充
- 已知CH4(气)+2O2(气)2H2O(液)+CO2(气),放出890.3 kJ热量;2H2O(液)2H2(气)+O2(
- 夜色下的玫瑰 女人家有个不大的院落。 院落里盛开着娇艳的玫瑰花。 她的丈夫为救一个落水儿童,永远地离开了她。 她本是一挡
- 通过饲养灰鼠和白鼠(基因型未知)的实验,得到结果如下表,如果亲本一栏中杂交组合Ⅳ中的灰色雌鼠和杂交组合Ⅱ中的灰色雄鼠交配
- 下列燃料中,不属于化石燃料的是: A.煤 B.氢气 C.天然气
- 函数y=sin|x|的图象( )A.关于x轴对称 B.关于原点对称C.关于y轴对称
- 将浓度为0.1mol/L的某酸HA溶液(电离常数为Ka)加水不断稀释,下列各数值始终保增大的是
- 一颗自由下落的小石头,经过某点时的速度是10m/s,经过另一点时的速度为30m/s,求经过这两点的时间间隔和两点间的距离



