第三节 化学键 知识点题库
今有五种有机物:①丙三醇,②丙烷,③乙二醇,④乙醇,⑤丙醇,它们的沸点由高到低排列顺序为 .
下列说法正确的是( )
A . 分子间作用力与化学键的键能大小相当
B . 分子间作用力远强于化学键,是一种很强的作用
C . 氢键主要影响物质的化学性质
D . 分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间存在的相互作用称为分子间作用力
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池和液晶显示器制造中得到广泛应用.NF3是一种三角锥型分子,键角102°,沸点﹣129℃;可在铜的催化作用下由F2和过量NH3反应得到:2NH3+3F2 NF3+3NH4F
NF3+3NH4F
 NF3+3NH4F
NF3+3NH4F
-
(1) 上述化学方程式中的5种物质所含的化学键类型有 (填序号).
a.离子键b.共价键c.配位键d.金属键
-
(2) 与铜属于同一周期,且未成对价电子数最多的元素基态原子价电子排布式为
-
(3) NF3的沸点比NH3的沸点(﹣33℃)低得多的主要原因是
-
(4) 理论上HF、NaAlO2和NaCl按6:1:2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用.该物质为配合物,其中心离子是 ,配位数为
-
(5) 根据下列五种元素的第一至第四电离能数据(单位:kJ•mol﹣1 ),回答下面各题:
元素代号
I1
I2
I3
I4
Q
2080
4000
6100
9400
R
500
4600
6900
9500
S
740
1500
7700
10500
T
580
1800
2700
11600
U
420
3100
4400
5900
①在周期表中,最可能处于同一族的是 和 .
②T元素最可能是 (填“s”、“p”、“d”、“ds”等)区元素.若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物的空间构型为 ,其中心原子的杂化轨道类型为
下列叙述正确的是( )
A . 分子晶体中的每个分子内一定含有共价键
B . 原子晶体中的相邻原子间只存在非极性共价键
C . 离子晶体中可能含有共价键
D . 金属晶体的熔点和沸点都很高
下列有关说法正确的是( )
A . 物质熔沸点的高低顺序是:晶体硅>氯化钠>干冰>汞
B . 分子晶体中一定存在分子间作用力
C . 水是一种非常稳定的化合物,这是由于氢键所致
D . CO2、HCl、CF4、PCl3四种物质分子中的所有原子都满足最外层为8电子的稳定结构
在下列变化中:①干冰气化;②硝酸钾熔化;③食盐溶于水;④HCl溶于水;⑤蔗糖溶于水;⑥HI分解.用序号填空:
-
(1) 未破坏化学键的是.
-
(2) 仅离子键被破坏的是.
-
(3) 仅共价键被破坏的是.
下列观点正确的是( )
A . 化合物电离时,生成的阴离子是氢氧根离子的是碱
B . 某化合物的熔融状态能导电,该化合物中一定有离子键
C . 某化合物的水溶液能导电,该化合物可能是非电解质
D . 某纯净物在常温下为气体,则组成该物质的微粒一定含有共价键
铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO  [Cu(NH3)3CO]+ , 2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+ , 2CH3COOH+2CH2=CH2+O2  2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
 [Cu(NH3)3CO]+ , 2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+ , 2CH3COOH+2CH2=CH2+O2 -
(1) Cu2+基态核外电子排布式为。
-
(2) NH3分子空间构型为。
-
(3) CH3COOCH=CH2分子中碳原子轨道的杂化类型是,1molCH3COOCH=CH2中含
 键数目为。
键数目为。
-
(4) CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为。
-
(5) 配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构可用示意图表示为。
顺铂[Pt(NH3)2Cl2]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸二氨合铂(Ⅱ)的简称,属于第二代铂族抗癌药物,结构简式如图所示,其毒副作用低于顺铂。下列说法正确的是( )
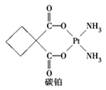
A . 碳铂中所有碳原子在同一个平面中
B . 1 mol 碳铂含有σ键的数目为26NA
C . [Pt(NH3)2Cl2]有顺式和反式两种结构,是一种复盐
D . 碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子之比为1∶2
近年来,德国研究人员利用O2、N2、CH4、NH3、H2O和HCN这6种远古地球上存在的简单物质,再使用硫醇和铁盐等物质模拟当时环境,成功制得核酸的4种基本模块。下列说法正确的是( )
A . O2的沸点比N2的低
B . NH3分子呈三角锥形
C . 配离子[Fe(H2O)6]3+中H与中心原子配位
D . 元素C、N、O、S的第一电离能依次增大
NaOH溶于水的过程中,破坏了( )
A . 离子键
B . 共价键
C . 金属键和共价键
D . 离子键和共价键
下列有关说法正确的是( )
A . 7.8g苯含有0.6NA个σ键
B . 基态F原子核外有9种能量不同的电子
C . 第一电离能:Ga>Zn
D . 每个面心立方晶胞中八面体空隙与四面体空隙个数比为1:2
在一定条件下,氢气既可与活泼金属反应,又可与活泼非金属反应。现有两种氢化物CaH2和H2S,下列有关判断正确的是( )
A . 所含氢元素的化合价均为+1
B . 两者均为共价化合物
C . 两者所含的氢微粒的半径相同
D . 两者混合时会生成氢气
二氧化硅晶体是立体网状结构,其晶体模型如图所示。下列有关二氧化硅晶体的说法正确的是( )
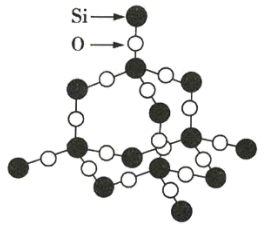
A . 二氧化硅晶体最小环上含有12个原子
B . 每个硅原子为4个最小环所共有
C . 从晶体结构可知,1molSiO2拥有2molSi-O键
D . SiO2晶体是由极性共价键与非极性共价键共同构成的
某小组用温度传感器探究液态物质挥发过程中体系温度变化的大小和快慢。如图a连接装置,将滤纸固定于温度传感器测量端,并插人待测液中使滤纸吸附待测液,待温度示数稳定后,开始采集数据,约10s后取出温度传感器置于空气中放置,采集到的温度变化如图b、图c所示。下列说法错误的是:( )
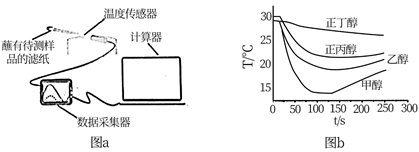
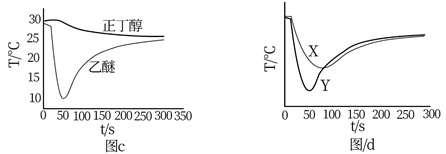
A . 由图b,分子间作用力越弱,气化速率越快
B . 由图c,正丁醇气化温差小于乙醚,是因为正丁醇更稳定
C . 由图d,X的相对分子量可能小于Y
D . 由图d,X、Y可以分别为正己烷、正戊烷
 因具有杀菌能力强,对人体、动物没有危害以及对环境不造成二次污染等特点,备受人们的青睐。下图是一种制
因具有杀菌能力强,对人体、动物没有危害以及对环境不造成二次污染等特点,备受人们的青睐。下图是一种制  的微观示意图。下列有关说法正确的是( )
的微观示意图。下列有关说法正确的是( ) 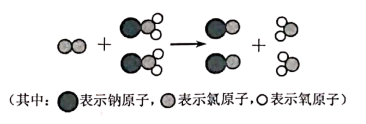
A . 该反应中只有共价键的断裂与形成
B . 该反应中, 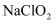 作氧化剂
C . 该条件下,氧化性:
作氧化剂
C . 该条件下,氧化性: 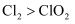 D . 制取
D . 制取 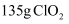 ,有
,有 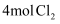 失去电子
失去电子
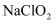 作氧化剂
C . 该条件下,氧化性:
作氧化剂
C . 该条件下,氧化性: 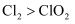 D . 制取
D . 制取 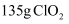 ,有
,有 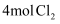 失去电子
失去电子
X、Y、Z、R、W为原子序数依次增大的短周期元素,Z、W为同族元素,R是短周期中原子半径最大的主族元素。其中,X、Y、Z、W形成的化合物可表示为[YX4]+[XWZ4]-。下列说法错误的是( )
A . R与X、Y、Z、W均可形成离子化合物
B . 简单气态氢化物的稳定性:Z>Y
C . X、Y、Z三种元素形成物质的水溶液只能呈酸性
D . [YX4]+为正四面体构型
下列对化学用语的描述中,错误的是( )
A . 硫离子的结构示意图: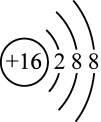 B .
B . 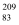 Bi和
Bi和 Bi互为同位素
C . 由H和Cl形成HCl的过程:
Bi互为同位素
C . 由H和Cl形成HCl的过程: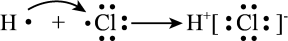 D . 由Na和Cl形成NaCl的过程:
D . 由Na和Cl形成NaCl的过程: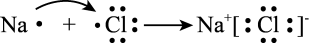
 B .
B . 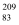 Bi和
Bi和 Bi互为同位素
C . 由H和Cl形成HCl的过程:
Bi互为同位素
C . 由H和Cl形成HCl的过程:
2021年我国科学家实现了二氧化碳到淀粉的人工合成。有关物质的转化过程示意如下,下列说法错误的是( )
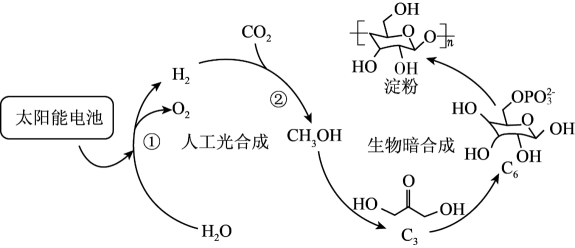
A . 反应①中分解 制备
制备 需从外界吸收能量
B . 反应②中消耗44g
需从外界吸收能量
B . 反应②中消耗44g  , 转移电子数为
, 转移电子数为 C . 1mol
C . 1mol  分子含极性共价单键8 mol
D .
分子含极性共价单键8 mol
D .  淀粉的过程中只涉及
淀粉的过程中只涉及 键的断裂和形成
键的断裂和形成
 制备
制备 需从外界吸收能量
B . 反应②中消耗44g
需从外界吸收能量
B . 反应②中消耗44g  , 转移电子数为
, 转移电子数为 C . 1mol
C . 1mol  分子含极性共价单键8 mol
D .
分子含极性共价单键8 mol
D .  淀粉的过程中只涉及
淀粉的过程中只涉及 键的断裂和形成
键的断裂和形成
下列各组分子中,都属于含有极性键的非极性分子的一组是( )
A . CO2、H2O
B . C2H4、CH4
C . Cl2、C2H2
D . NH3、HCl
最近更新
- 下列对文学名著的评点不正确的一项是( )(3分) A、《格列佛游记》作者以神奇的想象、夸张的手段、寓言的笔法,揭露批判了
- 在俄国,民主革命与社会主义革命紧密相连,形成了急剧发展的两个阶段的革命。这两个阶段的革命是指
- 如图1-1-3,在△ABC中,BC=5,AC=4,cos∠CAD=,且AD=BD,求△ABC的面积.
- We all know that money can't buy happiness, but manytimes we
- 已知,,则( ) A. B. C. D.
- 在将军家门前 阎连科 ①新近,五连受命来接替一连盖一座办公大楼。照说,也没啥大不了的,就是给泥瓦师傅供砖、供灰的
- 推理是一种重要的学习方法.下列推理中正确的是() A.碳酸盐遇酸有气泡产生,则加酸产生气泡的物质一定是碳酸盐 B.单质是
- 单项选择。从下列各题的A、B、C、D中选出能填入所给句子中的空白处的最佳答案。 BeijingOpera is ____
- “八国集团”由美国、英国、法国、德国、意大利、加拿大、日本和俄罗斯组成。在 西方八国中,既实行议会制共和制和多党制又是联
- 函数的最小正周期为 (
- 基因型为AaBb的一个小孢子母细胞,经减数分裂后形成4个花粉粒,其中由一个花粉粒形成的一个营养核和两个精子的基因型分别是
- 已知函数f(x)=ex﹣e﹣x,e为自然对数的底,则下列结论正确的是() A.f(x)为奇函数,且在R上单调递增 B.f
- 2.下列句子中,没有语病、句意明确的一句是( )(3分) A.在本月热播的几部以南京大屠杀为题材的影片中,还原出许多历史
- 从东西半球看,我国位于:( ) A. 西半球 B.北半球 C.东半球
- 新闻媒体在促使法院审判公正方面发挥着重要作用,但部分媒体传递出的有倾向性的社会压力和舆论导向也可能回影响法院的审判程序和
- 实验室里取用金属钠时,用到的仪器用品是 ①试管夹 ②镊子 ③小刀 ④滤纸 ⑤试管
- It is so nice to hear from her, ____, we last met more than
- (1995上海) ____ for the free tickets,I would not have gone to
- 下列哪种物质不是肝脏细胞线粒体和叶肉细胞叶绿体共有的组成成分或直接合成和直接消耗的物质 A.DNA
- 下列句子中,没有语病的一句是( ) A.朝夕相处,谁也不能保证不发生矛盾,但一发生矛盾,就各持己见,争吵不休,互不通融



