第三节 化学键 知识点题库
下列关于氢键的说法中正确的是( )
A . 氢键比分子间作用力强,所以它属于化学键
B . 分子内形成的氢键使物质的熔点和沸点升高
C . 氨溶于水后氨分子和水分子之间形成了氢键
D . 邻羟基苯甲酸的熔点比对羟基苯甲酸的熔点高
请用电子式表示下列化合物的形成过程
MgCl2H2SNa2OH2O2.
根据问题填空:
-
(1) 原子序数为84的元素在元素周期表中的位置.
-
(2) 将序号填入空格中.在①NaOH ②H2O ③H2O2④N2⑤NH4Cl ⑥Na2O2⑦MgBr2 等物质中,只含有离子键的是,只含有共价键的是,既含有离子键又含有极性键的是,既含离子键又含非极性键的是,既含极性键又含非极性键的是,属于离子化合物的是.
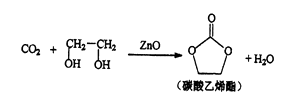
用二氧化碳生产化工产品,有利于二氧化碳的大量回收,二氧化碳和乙二醇在ZnO或锌盐催化下可合成碳酸乙烯酯。
-
(1) 锌基态原子核外电子排布式为。
-
(2) 锌盐水溶液中Zn2+可与H2O之间形成 [Zn(H2O)6]2+ , 其中提供空轨道的是(填微粒符号)。
-
(3) 碳酸乙烯酯中碳原子杂化轨道类型为;1mol碳酸乙烯酯中含有的σ键数目为。
-
(4) 阴离子X-与CO2互为等电子体且X-内含共价键和氢键,则X-的化学式为。
食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是( )
A . 炒菜时放入食盐并不破坏NaCl中的化学键
B . HCl的电子式是H+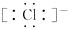 C . NaCl熔化时破坏共价键
D . HCl的结构式是H—Cl
C . NaCl熔化时破坏共价键
D . HCl的结构式是H—Cl
下列有关物质性质的应用正确的是( )
A . 活泼金属与活泼非金属形成的都是离子键
B . 二氧化硅是制造太阳能电池板的主要材料
C . 二氧化硫通入酸性KMnO4溶液,溶液紫红色褪去,体现了SO2的漂白性
D . 化学反应的实质就是反应物中化学键断裂,生成物中形成新的化学键。
下列用电子式表示物质形成过程正确的是( )
A . 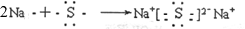 B .
B . 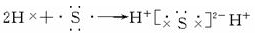 C .
C . 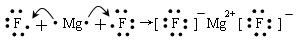 D .
D . 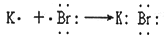
下列有机物中,符合通式CnH2n+2 , 且沸点最高的是( )
A . 环己烷
B . 新戊烷
C . 三氯甲烷
D . 正辛烷
下列物质中,σ键数目与π键数目之比为1:1的是( )
A . N2
B . CO2
C . HCHO
D . H2O2
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中正确的是( )
A . X、M两种元素只能形成X2M型化合物
B . Y 的气态简单氢化物的热稳定性比W 的强
C . X2M、YM2中含有相同类型的化学键
D . 元素W和M的某些单质可作为水处理中的消毒剂
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
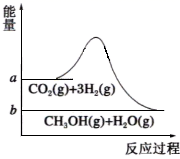
请回答下列问题:
-
(1) 观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
-
(2) 甲醇的结构类似于乙醇,试写出甲醇的结构式:。甲醇分子中的化学键类型是(填“离子键“共价键”)。
-
(3) 科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是,发生的是(填"氧化"或"还原")反应。
-
(4) 欲使合成甲醇的化学反应速率加快,请写出两条措施:;
下列物质既含有离子键,又含有共价键的是( )
A . H2S
B . Na2S
C . H2SO4
D . (NH4)2SO4
下列说法错误的是( )
A . HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关
B . C,Si和Ge的最外层电子数都是4,次外层电子数都是8
C . CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应
D . 白酒中,乙醇分子和水分子间存在范德华力和氢键
近年来科学家发现铝的超原子结构Al13和Al14 , Al13和Al14的性质与元素周期表中某些主族元素的性质相似,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定的Al13-、Al142+。下列说法中错误的是( )
A . Al13与Al14互为同素异形体
B . Al13超原子中Al原子间是通过离子键结合的
C . Al14与氢碘酸反应的化学方程式可表示为:Al14+2HI=Al14I2+H2↑
D . Al13在一定条件下能和镁作用生成Mg(Al13)2
按要求完成下列问题:
-
(1) 三氧化硫的分子式;
-
(2) 氯气中存在的化学键类型是;
-
(3) 沸点:H2OH2S(填“>”或“<”)。
氢化钠与水反应如下:NaH+H2O=NaOH+H2↑。下列说法错误的是( )
A . NaH属于离子化合物
B . 该反应为置换反应
C . NaOH中含有极性共价键
D . H2O分子的空间结构为V形
下列化学用语的书写正确的是( )
A . O2-的离子结构示意图: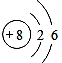 B . 质子数为27、中子数为60的Co原子:
B . 质子数为27、中子数为60的Co原子: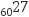 Co
C . H2O的电子式:
Co
C . H2O的电子式: D . 用电子式表示氢溴酸的形成过程为:
D . 用电子式表示氢溴酸的形成过程为: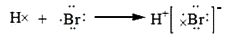
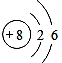 B . 质子数为27、中子数为60的Co原子:
B . 质子数为27、中子数为60的Co原子: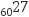 Co
C . H2O的电子式:
Co
C . H2O的电子式: D . 用电子式表示氢溴酸的形成过程为:
D . 用电子式表示氢溴酸的形成过程为: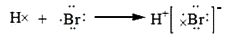
下图是短周期主族元素的单质及其化合物(或其溶液)的转化关系。已知X、Y、Z原子序数依次增大,A~F均为化合物,F为不含金属元素的含氧酸盐。下列说法正确的是( )
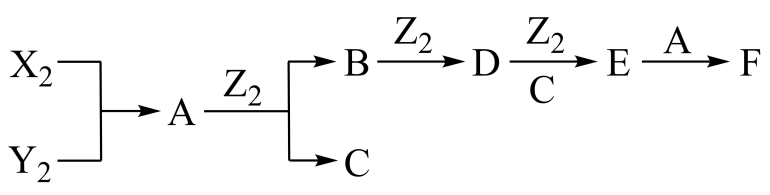
A . 原子半径:X<Y<Z
B . 物质的稳定性:A>C
C . E和F中存在的化学键类型完全相同
D . 常温下,可以用铁质容器盛装E的浓溶液
不同主族的短周期元素X、Y、Z、W其原子序数依次增大,X、Y的简单离子的电子层结构相同,短周期主族元素原子中Y的原子半径最大,Z原子最外层电子数是K层的3倍。下列说法错误的是( )
A . 熔化YW时离子键被破坏
B . X的简单氢化物可作制冷剂
C . 离子的还原性:Z>W
D . Y的氧化物为离子化合物,不含共价键
我国科学家利用Co的化合物在Fe(OH)2氧化过程中的催化作用,促进了电催化过程中流失的Fe催化活性中心的原位自修复(Fe再沉积的主要反应过程) ,反应机理如图所示。下列说法错误的是( )
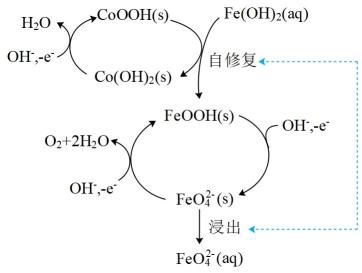
A . 反应过程中CoOOH为催化剂
B . 图中各反应不能在酸性条件下进行
C . 存在反应Co(OH)2+OH- -e- =CoOOH+H2O
D . 图中所示物质之间的转化有非极性键的形成和断裂
最近更新
- 对下列装置,不添加其他仪器无法检查气密性的是( )
- 根据提示补写名句或填写课文内容。(10分 每空1分)1. ,时见一斑。2.
- 如下图,在△ABC中,BC=4,以点A为圆心,2为半径的⊙A与BC相切于点D,交AB于E,交AC于F,点P是⊙A上一点,
- 淀粉酶、纤维素和DNA都含有的元素是 A.C、H、O B.C、O、N、P C.C、H、O、N D.C、
- 已知,用含x的代数式表示y正确的是( ) A. B. C. D.
- ---Where may you advise me to start my business? ---In my op
- 下列设计方案是利用物质的化学性质达到实验目的的是 A.观察小木条燃烧情况,比较“人吸入空气和呼出气体”中氧气含量的大小B
- 所示为一块霍尔元件,其横载面为矩形,霍尔元件的长、宽、高分别为c、b、d。已知其单位体积内的电子数为n、电子电荷量e.将
- 张大爷家的小麦叶色发黄,有倒伏现象,张大爷应该给小麦施下列哪种化肥( ) A.硝酸钾 B.碳酸氢铵
- 通读下面的对话,然后根据上下文补全对话内容。A: Good afternoon, Miller! 【小题1】 ?B:
- 将一盛满Cl2的试管倒立于水槽中,当日光照射相当一段时间后,下列说法不正确的是( ) A.试管中气体颜色逐渐变浅
- 已知. (Ⅰ)求不等式的解集; (Ⅱ)若存在,使得成立,求实数的取值范围.
- 人体红细胞产生ATP的部位、所需ATP的来源、主要呼吸类型分别是() A. 线粒体;葡萄糖;有氧呼吸
- 函数的图象为C,: ①图象关于直线对称; ②函数在区间内是增函数; ③由的图象向右平移个单位长度可以得到图象. 以
- “旧时王谢堂前燕,飞入寻常百姓家”,一些本来只有少数人才买得起的高档商品,过了一段时间之后,其价格会逐渐降低,成为寻常
- —Do you have any plans for this weekend? —Yes.We will go on
- 若一个三角形的一边长为3cm,则它的周长可能为() A. 4cm B. 5cm C. 6cmD. 8cm
- 某可逆反应的正反应是放热反应,则温度对此反应的正、逆反应速率影响的曲线(如图所示)中,正确的是()
- 电脑与我们的生活联系越来越紧密,文字编辑、图片处理、上网浏览等等都离不开它。不知你是否注意,有些软件、网站的名字很有创意
- 如图2所示,C是水平地面,A、B是两个长方体物块,F是作用在物块B上沿水平方向的力,物体A和B一起加速运动.由此可见,A



