第三节 化学键 知识点题库
下列说法正确的是( )
A . HClO和NaClO都是弱电解质
B . 胶体能产生丁达尔效应,而溶液不能
C . 1mol H2SO4与1mol Ba(OH)2反应放出的热量叫做中和热
D . HCl和NaCl溶于水破坏的化学键完全相同
下列几种氢键:①O﹣H…O,②N﹣H…N,③F﹣H…F,④O﹣H…N,其强度由强到弱的排列顺序是( )
A . ③①④②
B . ①②③④
C . ③②①④
D . ①④③②
科学家将石墨在氟磺酸中“溶解”制得石墨烯(即单层石墨),该溶解克服了石墨层与层之间的( )
A . 范德华力
B . 离子键
C . 共价键
D . 金属键
根据键能数据(H﹣Cl 431kJ/mol,H﹣I 297kJ/mol),可得出的结论是( )
A . HI比HCl稳定
B . HI比HCl熔、沸点高
C . 溶于水时,HI比HCl更容易电离,所以氢碘酸是强酸
D . 拆开等物质的量的HI和HCl,HI消耗的能量多
科学家研究发现普通盐水在无线电波的照射下可以燃烧,其原理是无线电频率可以削弱盐水中所含元素原子之间的“结合力”,释放出氢原子和氧原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述中“结合力”的实质是( )
A . 离子键
B . 离子键与共价键
C . 极性共价键
D . 非极性共价键
下列物质中,只含离子键的是( )
A . H2
B . NH3
C . MgCl2
D . NaOH
-
(1) 写出下列微粒的电子式:NaOH;CS2;Na2SNH3;NH4H;
-
(2) 用电子式表示下列物质的形成过程MgCl2
-
(3) 现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl①只由离子键构成的物质是。
②只由极性键构成的物质是。
③由极性键和非极性键构成的物质是。
④由离子键和极性键构成的物质是。
⑤由离子键和非极性键构成的物质是。
下列物质中既含有非极性键,又含有离子键的是( )
A . MgBr2
B . H2O2
C . Na2O2
D . NH4Cl
NaN3是一种易溶于水(NaN3=Na++N3-)的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如下:

-
(1) 钠元素位于周期表第周期族。
-
(2) NaNH2中氮元素的化合价为;Na+的结构示意图为。
-
(3) NaOH的电子式为。
-
(4) 反应NH4NO3
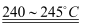 N2O↑+2H2O↑中,每生成1molN2O转移电子数为个。
N2O↑+2H2O↑中,每生成1molN2O转移电子数为个。
-
(5) 反应①的化学方程式为。
-
(6) 销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为(N3-被氧化为N2)。
下列说法中不正确的是( )
A . N2O与CO2、CCl3F与CCl2F2互为等电子体
B . CCl2F2无同分异构体,说明其中碳原子采用sp3方式杂化
C . H2CO3与H3PO4的非羟基氧原子数均为1,二者的酸性(强度)非常相近
D . 由I A族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有共价键的离子化合物
下列说法不正确的是( )
A . Mg2+和S2-的最外电子层都形成了8个电子的稳定结构
B . 石英和金刚石都是原子间通过共价键结合形成的原子晶体
C . 浓硫酸和H2O混合时放出热量与微粒之间的作用力有关
D . H2O2易分解是因为H2O2分子间作用力弱
下列每组物质发生状态变化所克服的粒子间的相互作用属于同种类型的是( )
A . 食盐和蔗糖熔化
B . 钠和硫熔化
C . 碘和干冰升华
D . 二氧化硅和氧化钠熔化
-
(1) 写出CO2的空间构型:。
-
(2) 写出Na3N的电子式:。
-
(3) 写出C2H6O的化学名称:。
-
(4) 写出乙烯的实验式:。
下列物质中,只含离子键的是( )
A . NaOH
B . KCl
C . NH3
D . HCl
A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图如图,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。试回答下列问题:
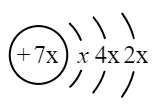
-
(1) 写出C的核外价电子排布图。
-
(2) 用元素符号表示D所在周期第一电离能最大的元素是,电负性最大的元素是。
-
(3) 已知元素周期表可按电子排布分为s区、p区等,则E元素在区,已知E3+离子比E2+离子稳定,解释其原因E元素原子的核电荷数是,E元素在周期表中位于第周期第族;
-
(4) 已知D氢化物比C的氢化物沸点高,原因是。
固体A的化学式为NH5 , 它的所有原子的最外层电子结构都符合相应稀有气体原子的最外层电子结构,则下列有关说法中错误的是( )
A . NH5中既有离子键又有共价键
B . NH5的熔沸点高于NH3
C . 1molNH5中含有5molN—H键
D . 将固体A投入少量水中,可生成H2和NH3·H2O
下列表示物质结构的化学用语或模型正确的是( )
A . 中子数为18的氯原子: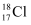 B . 丙烯的结构简式:
B . 丙烯的结构简式: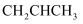 C . CH3CHO的球棍模型:
C . CH3CHO的球棍模型: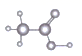 D . 用电子式表示NaCl的形成过程:
D . 用电子式表示NaCl的形成过程: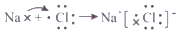
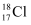 B . 丙烯的结构简式:
B . 丙烯的结构简式: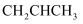 C . CH3CHO的球棍模型:
C . CH3CHO的球棍模型: D . 用电子式表示NaCl的形成过程:
D . 用电子式表示NaCl的形成过程:
下列物质中,含共价键的是( )
A . Na2O
B . KCl
C . CH4
D . MgCl2
X、Y、Z、W为四种短周期元素,有关这四种元素的说法中一定正确的是( )
元素 | X | Y | Z | W |
原子半径(nm) | 0.077 | 0.075 | 0.102 | 0.099 |
最高正价或最低负价 | +4 | +5 | -2 | -1 |
A . X与W形成XW4时,各原子最外层均满足8电子稳定结构,
B . 1molW的单质参加氧化还原反应时转移的电子数为2mol
C . 0.3molCu分别与足量HYO3和H2ZO4的稀溶液反应均产生0.2mol气体
D . Y的氢化物与W的氢化物反应的产物只含有共价键
下列物质的性质或相关数据与氢键无关的是( )
A . 氨气极易溶于水
B . 邻羟基苯甲酸(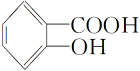 )的熔点为159℃,对羟基苯甲酸(
)的熔点为159℃,对羟基苯甲酸(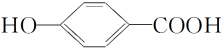 )的熔点为213℃
C . 二甲醚微溶于水,而乙醇可与水以任意比例混溶
D .
)的熔点为213℃
C . 二甲醚微溶于水,而乙醇可与水以任意比例混溶
D . 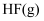 分解时吸收的热量比
分解时吸收的热量比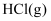 分解时吸收的热量多
分解时吸收的热量多
 )的熔点为159℃,对羟基苯甲酸(
)的熔点为159℃,对羟基苯甲酸(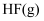 分解时吸收的热量比
分解时吸收的热量比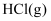 分解时吸收的热量多
分解时吸收的热量多
最近更新
- 26g黄铜(Cu-Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8克。求:⑴黄
- 如图6-2-3所示,沿水平方向做匀变速直线运动的车厢中,悬挂小球的悬线偏离竖直方向37°角,球和车厢相对静止,球的质量为
- 奥运会将带领体育产业实现大跨越的发展。在奥运会结束后,体育对人们的影响将从“鸟巢”、从北京扩散到全国各地,扩散到普通家庭
- 材料:田纳西河流域位于美国东南部,气候温暖湿润,山青水秀,森林繁茂。19世纪后期起,流域内人口激增,开发利用程度加大(图
- (9分,每小题3分) 阅读下面的文言文,完成下列各题 田豫,字国让,渔阳雍奴人也。刘备之奔公孙瓚也,豫时年少,自托于备,
- 苹果酸是一种有机酸,其结构如图所示。下列关于苹果酸的说法不正确的是A.分子式为C4H6O5 B.分子中含有一个手性碳原子
- 国家图书馆建馆100年来,积极服务于广大读者,见证了国人读书的历程和变化,为我国社会文明进步作出了巨大贡献。到图书馆有偿
- You must get a good night sleepfirst, muchwork yo
- 甲、乙两人下棋,和棋的概率为,乙获胜的概率为,则甲获胜的概率和甲不输的概率分别为() A., B.,
- 翻译下面文言文 子曰:“麻冕⑴,礼也;今也纯⑵,俭⑶,吾从众。拜下⑷,礼也;今拜乎上,泰也。虽违众,吾从下。”
- 下列有关硅及其化合物的说法错误的是() A.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料 B.二氧化硅属于酸性氧
- “改造中国、拯救人民之路到底在何方?”1923年前后,在孙中山经历了一次次的失败之后发出了这样的疑问时,你应该这样回答他
- 下列各句中划线的熟语,使用恰当的一句是( ) A.产业要发展,测试需先行,数字电视测试仪器作为数字电视产业链的
- 如图9, △ABC的周长是32,且BD=DC,AD⊥BC于D,△ACD的周长为24,那么AD的长为 。
- 求函数的定义域
- 在水平道路上匀速行驶的汽车,受到扰动后车上的货物随车厢底版上下振动,设货物的振动是简谐运动且振动过程中物体不脱离底版。取
- “黛玉葬花”表现了黛玉当时什么样的处境和心情?答:
- (广东省六校联合体2009届高三第二次联考10题)“盖自三权鼎立之说出,以国会立法,以法官司法,以政府行政,而人主总之…
- 1999年世贸组织西雅图会议期间,世贸组织的反对者进行了大规模示威游行,参加者多是中下层劳动人民,主要是因为 A.经济全
- 已知常温下在溶液中可发生如下两个离子反应: Ce4++Fe2+= Fe3++Ce3+ Sn2++2Fe3+ = 2



