第三节 氧化还原反应 知识点题库
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程表示)
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+ , 并有气体逸出,请写出相应的离子方程式:
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL5mol•L﹣1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+ , 则参加反应的铁粉的质量为 .
 2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )
①16H++10Z﹣+2XO4﹣═2X2++5Z2+8H2O;
②2A2++B2═2A3++2B﹣;
③2B﹣+Z2═B2+2Z﹣ .
由此推断下列说法错误的是( )
-
(1) 该反应的还原剂是(填分子或离子符号).
-
(2) 反应过程中,每有1mol I2发生反应,转移的电子为mol.
-
(3) 写出该反应的离子方程式.
 2H2↑+O2↑
2H2↑+O2↑
 CO2+H2
B . CuO+H2
CO2+H2
B . CuO+H2  Cu+H2O
C . 2F2+2H2O═4HF+O2
D . 3NO2+H2O═2HNO3+NO
Cu+H2O
C . 2F2+2H2O═4HF+O2
D . 3NO2+H2O═2HNO3+NO
CN-+OH-+Cl2→OCN-+Cl-+H2O(未配平) 反应Ⅰ
2OCN-+4OH-+3Cl2=2CO2+N2+6Cl-+2H2O 反应Ⅱ
下列说法中正确的是( )
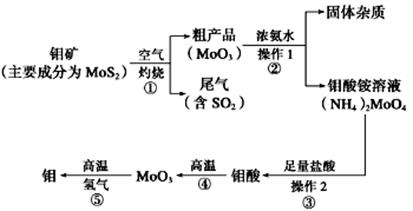
-
(1) 写出在高温下发生反应①的化学方程
-
(2) 生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:
-
(3) 如果在实验室模拟操作 1 和操作 2,则需要使用的主要玻璃仪器有
-
(4) 某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:
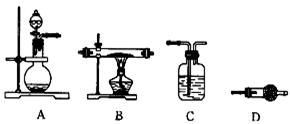
① 请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是
② 在烧瓶 A 中加入少量硫酸铜的目的是
③ 两次使用 D 装置,其中所盛的药品依次是、
-
(1) 写出两种可以食用的含钠化合物的化学式:。将0.01 mol下列物质(①Na2O2;②Na2O;③Na2CO3;④NaCl)分别加入100 mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度由大到小的顺序是(溶液体积变化忽略不计)。
-
(2) 由于钾比钠更活泼,制备K2O一般是用单质钾还原对应的过氧化物、硝酸盐或亚硝酸盐,试写出用钾与硝酸钾反应制取K2O的化学方程式(还有一种单质生成):。K2O2也有强氧化性,试写出其与SO2发生反应的化学方程式:。
-
(3) 某学生用Na2CO3和 KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
实验序号
①
②
③
④
盐酸体积/mL
50
50
50
50
固体质量/g
3.06
6.12
9.18
12.24
生成气体体积/L(标况)
0.672
1.344
1.568
1.344
根据数据计算所用盐酸的物质的量浓度为,原混合物样品中n(Na2CO3)∶n(KHCO3)=。
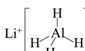 )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2 , LiAlH4在125℃分解为LiH、H2和Al。下列说法错误的是( )
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2 , LiAlH4在125℃分解为LiH、H2和Al。下列说法错误的是( )
 Si+4HCl中,还原剂是( )
Si+4HCl中,还原剂是( )
 、Mg2+、Fe2+、SO
、Mg2+、Fe2+、SO  、MnO
、MnO  、CO
、CO  、SO
、SO  中的若干种,取一定量待测液进行如下实验:
中的若干种,取一定量待测液进行如下实验: 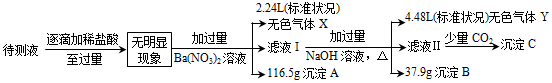
回答下列问题:
-
(1) 该待测液中一定含有的离子是;无法确定是否含有的离子是;
-
(2) 沉淀B的成分及物质的量为(物质写化学式)。
-
(3) 生成无色气体X时的离子方程式为。
-
(4) 生成沉淀C时的离子反应方程式为。
-
(5) 在催化剂、加热条件下气体X与气体Y可以反应转化为对环境无害的物质,该反应的化学方程式为,所得氧化产物与还原产物的质量之比为。
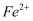 的废液制备硫酸亚铁晶体的流程如:
的废液制备硫酸亚铁晶体的流程如: 请回答下列问题:
请回答下列问题:
-
(1) 加入饱和
 溶液后的操作1为,若
溶液后的操作1为,若 溶液浓度偏低可能会形成胶体,验证的方法为(不用写操作和现象).
溶液浓度偏低可能会形成胶体,验证的方法为(不用写操作和现象).
-
(2) 加入铁粉的作用是.
-
(3) 测定废液中
 的浓度可使用已知浓度的酸性高锰酸钾溶液.
的浓度可使用已知浓度的酸性高锰酸钾溶液.①配平化学方程式,并用单线桥法表示电子转移过程:
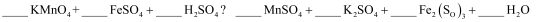 ②已知
②已知 与
与 按物质的量
按物质的量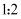 的比例恰好完全反应,该反应的离子方程式为.
的比例恰好完全反应,该反应的离子方程式为. -
(4) 该兴趣小组在研究硫酸亚铁热稳定性时,作出了两种假设:
①假设它按
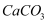 受热分解的方式分解,反应的化学方程式为.
受热分解的方式分解,反应的化学方程式为.②假设它按
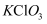 受热分解的方式分解,已知产物中有两种酸性氧化物生成,则反应的化学方程式为.
受热分解的方式分解,已知产物中有两种酸性氧化物生成,则反应的化学方程式为.
 ,
, 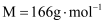 溶于水配成溶液,用
溶于水配成溶液,用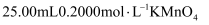 溶液恰好将其完全氧化。则
溶液恰好将其完全氧化。则 的还原产物是( )
的还原产物是( )
 B .
B .  C .
C . 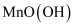 D .
D . 
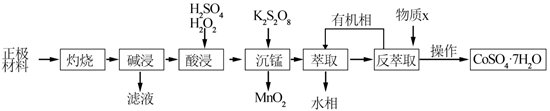
-
(1) 灼烧的目的是。
-
(2) 酸浸时( LiCoO表示)发生反应的化学浸入后,Co 、Mn元素均以+2价形式存在。。
-
(3) 锰时,需先加入适量Mn 2 S 2 O 8 , 将部分Mn 2+氧化成
 ,沉睡时为生成2。
,沉睡时为生成2。
-
(4) 萃取和反萃取的过程表示为:Co 2 ++ 2(HA) 2
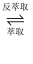 Co (HA 2 ) 2 +2H + , 反萃取时加入的物质X为(填化学式),请从化学平衡的角度说明所加物质的作用。
Co (HA 2 ) 2 +2H + , 反萃取时加入的物质X为(填化学式),请从化学平衡的角度说明所加物质的作用。
-
(5) 2.常温下,为使Ni 2+完全下降 , 溶液的pH值应大于大于(当c(Ni 2+ - 10-5mol / L 时 , 完全下降,
 )
)
-
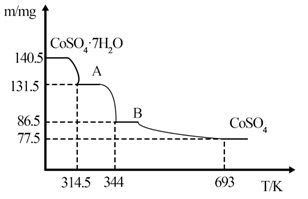
(6) CoSO 4 ·7H 2 O受热时,剩余物质的质量随温度变化情况如图所示,物质B的化学式为。
- 将一根长为L的直导线,由中点折成直角形放在磁感应强度为B的匀强磁场中,导线所在平面与磁感线垂直.当导线中通以电流I后,磁
- 下列疾病中,不是由于激素分泌异常而引起的是( ) A.巨人症 B.甲亢 C.大脖子病 D.脚气
- 中国科学院某研究小组设计了一种高性能锂空气电池,其反应原理可表示为:2Li+O2Li2O2,已知锂元素在化合物中显+1价
- 已知数列{an}是公差d≠0的等差数列,且a5=6. (1)求{an}的前9项的和S9; (2)若a3=3,问在数列{a
- Why are you doing that? If I ____you, I’d stop. A. had been
- 2014年3月5日, 第十二届全国人大二次会议在北京举行,来自工人、农民、知识分子、干部、解放军、民主党派和无党派人士、
- The country needs a _____ government. We have had three Prim
- 作文(40分)小学毕业升入初中,开始了一段全新的生活。对于你来说,有新奇,也有压力,如何调整好学习状态接受新的学习任务?
- (2010年孝感市高三模拟)北宋包拯以断狱英明刚直而著称于世,后世把他当做清官的化身——包青天。包拯为天圣朝进士,历任
- 我国著名的风景名山之一的庐山,其成因是 A.地堑成山 B.向斜成山 C.地垒成山 D.背斜成山
- 最近一则报道称:据专家调查,我国中小学生的计算能力比十年前明显下降。某中学就此话题举行一场辩论会,辩题是:中学生使用计算
- “起来,饥寒交迫的奴隶:起来,全世界受苦的人!”……这首雄壮的《国际歌》创作的最初动机是为了纪念 A.宪章运动
- 下列叙述不正确的是 A.“雨后彩虹”“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的性质有关B.我国规定自2
- Trust has been considered as the basis of anyrelationship, i
- 临淄实验中学的王浩同学把一实心铁球和一空心木球浸没于水中,放手后,木球漂浮而铝球下沉,静止后它们所受浮力大小关系是(
- In the late 1500s, a large powerful gun was placed on top of
- 如图3-3-9过半径为1的圆内一条直径上任意一点作垂直于直径的弦,求弦长超过圆内接等边三角形边长的概率.
- 化学是一门以实验为基础的科学.下列有关实验问题的说法中正确的是()A. 在做“粗盐中难溶性杂质的去除”实验时,一定要用到
- .春秋战国至秦汉时期,各种思想流派纷呈。有的学者对各种思想主张进行整理,将它们分别描述为“全面归服自然的隐士派”、“专制
- 第二节 完型填空 请认真阅读下面短文,从短文后各题所给的A、B、C、D四个选项中,选出最佳选项, 并在答题卡上将该项涂黑



