第三节 氧化还原反应 知识点题库
则下列各微粒氧化能力强弱顺序正确的是( )
-
(1) 亚硝酸钠可少量添加到食物中,用作食品的
-
(2) 已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,该述反应的还原剂是,若反应中转移0.2mol电子,则参与反应的NaNO2为 mol
-
(3) 根据上述反应,鉴别NaNO2和NaCl.可选用的物质有:A . 水 B . 碘化钾淀粉试纸 C . 淀粉 D . 食醋 E . 白酒
-
(4) 实验室模拟用以下反应合成亚硝酸盐
C6H12O6+12HNO3=3HOOC﹣COOH+9NO2+3NO↑+9H2O
NO+NO2+2NaOH=2NaNO2+2H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
其中第一个反应要控制反应液的温度在35~60℃条件下进行,原因是,第二个和第三个反应是NaOH溶液吸收反应生产的气体,所得溶液中的阴离子共有三种OH﹣、NO2﹣、,且第三种离子与NO2﹣的浓度之比为.
-
(5) 亚硝酸钠能氧化酸性条件下的Fe2+ , 同时产生一种气体,该气体在空气中迅速变色,写出亚硝酸钠与亚铁离子反应的离子方程式.
-
(1) 在ClO2 的制备方法中,有下列两种常用制备方法:
方法一:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4═2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为,其中方法二制备的ClO2 更适合用于饮用水的消毒,其主要原因是.
-
(2) 我国最近成功研制出制取ClO2 的新方法,其反应的微观过程如图甲所示:
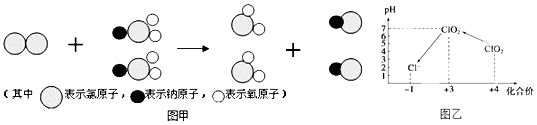
该反应的化学方程式为.
-
(3) 消毒时,ClO2对污水中Fe2+、Mn2+、S2﹣和CN﹣等有明显的去除效果.某工厂污水中含CN﹣ , 现用ClO2将CN﹣氧化,生成两种无毒气体,其离子反应方程式为.
-
(4) 自来水厂用ClO2 处理后的水中,要求ClO2 的浓度在0.1~0.8mg/L之间.碘量法可以检测水中ClO2 的浓度,步骤如下:
Ⅰ.取一定体积的水样用氢氧化钠溶液调至中性,然后加入一定量的碘化钾,并加入淀粉溶液,溶液变蓝.
Ⅱ.加入一定量的Na2S2O3 溶液.(已知:2S2O32﹣+I2═S4O62﹣+2I ﹣ )
Ⅲ.重复上述操作2~3次.
操作时,不同pH环境中粒子种类如图乙所示:
请回答:
①操作Ⅰ中反应的离子方程式是;
②确定操作Ⅱ恰好完全反应的现象是;
③若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10﹣3mol/L的Na2S2O3溶液10mL,则水样中ClO2的浓度是 mg/L.
 FeCl3
B . Na
FeCl3
B . Na  Na2O2
C . CuSO4溶液
Na2O2
C . CuSO4溶液  Cu
D . Fe(OH)3
Cu
D . Fe(OH)3  Fe2O3
Fe2O3
②  +5Cl−+6H+=3Cl2↑+3H2O
+5Cl−+6H+=3Cl2↑+3H2O
下列按物质氧化性顺序由强到弱排列正确的是( )
 >
>  B .
B .  >Cl2>
>Cl2>  C .
C .  >
>  >Cl2
D . Cl2>
>Cl2
D . Cl2> >
>
下列有关说法正确的是( )
 3Cu+N2+3H2O。下列判断正确的是( )
3Cu+N2+3H2O。下列判断正确的是( )
 、NO
、NO  、H+、
、H+、  、Cr3+、六种微粒,已知反应过程中
、Cr3+、六种微粒,已知反应过程中  浓度变化如图所示,下列说法正确的是( )
浓度变化如图所示,下列说法正确的是( ) 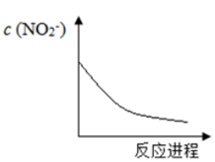
 中Cr化合价是+7价
B . 反应的氧化产物是
中Cr化合价是+7价
B . 反应的氧化产物是  C . 消耗1 mol氧化剂,转移电子3 mol
D . 随着反应的进行,溶液中的H+浓度增大
C . 消耗1 mol氧化剂,转移电子3 mol
D . 随着反应的进行,溶液中的H+浓度增大
-
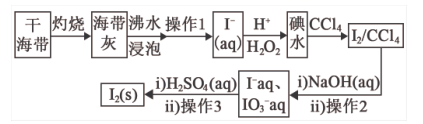
(1) 请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)
试剂:盐酸、NaOH溶液、NaCl溶液、Na2SO4溶液、稀硝酸、FeSO4溶液
①P2O5(一种酸性氧化物)→Na3PO4的离子方程式:。
②完成转化:SO2→H2SO4需要的试剂:。
-
(2) 高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO═2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是(用化学式表示)。
②用“单线桥”在方程式中标出电子转移的情况:。
③若反应中转移了1mol电子,则生成了gH2O。
![]()
-
(1) 写出FeCl3溶液与铜箔发生反应的离子方程式:。
-
(2) 检验废腐蚀液中是否含有Fe3+所需试剂名称:,实验现象:。
-
(3) 向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:,此转化的化学方程式为:。
-
(4) 写出③中所含物质:,⑥发生反应的离子方程式:。
 的溶液,充分反应后剩余的Na2SO3溶液用0.2mol/LKMnO4酸性溶液氧化,消耗KMnO4酸性溶液2mL,则元素R在还原产物中的化合价是( )
的溶液,充分反应后剩余的Na2SO3溶液用0.2mol/LKMnO4酸性溶液氧化,消耗KMnO4酸性溶液2mL,则元素R在还原产物中的化合价是( )
 是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
是一种环保、高效、多功能饮用水处理剂,制备流程如图所示: 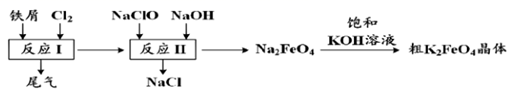
下列叙述错误的是( )
 作水处理剂时,既能杀菌消毒又能净化水
B . 反应Ⅰ中尾气可用
作水处理剂时,既能杀菌消毒又能净化水
B . 反应Ⅰ中尾气可用  溶液吸收再利用
C . 反应Ⅱ中氧化剂与还原剂的物质的量之比为
溶液吸收再利用
C . 反应Ⅱ中氧化剂与还原剂的物质的量之比为 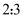 D . 该条件下,物质的溶解性:
D . 该条件下,物质的溶解性: 
 ,下列说法错误的是( )
,下列说法错误的是( )
 是还原剂
B .
是还原剂
B .  既是氧化产物又是还原产物
C .
既是氧化产物又是还原产物
C .  具有强氧化性,能消毒杀菌
D . 1 mol Na2O2发生反应,有4 mol发生电子转移
具有强氧化性,能消毒杀菌
D . 1 mol Na2O2发生反应,有4 mol发生电子转移
| 药品名称 | 84消毒液 |
主要成分 |
| |
注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等 |
请回答下列问题:
-
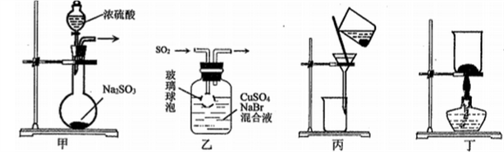
(1) 实验室用二氧化锰和浓盐酸共热制取氯气,该反应的离子方程式为,若含有
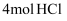 的浓盐酸与足量
的浓盐酸与足量 固体反应,产生
固体反应,产生 的分子数
的分子数 (填大于、等于或小于)。
(填大于、等于或小于)。
-
(2) 若将
 通入到热的
通入到热的 溶液中,可以得到
溶液中,可以得到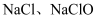 和
和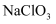 的混合液。当混合液中
的混合液。当混合液中 和
和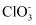 的个数比为
的个数比为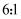 时,混合液中
时,混合液中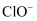 和
和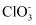 的个数比为。
的个数比为。
-
(3) 家庭用“84”消毒液用法强调,消毒马桶时,洁厕灵(主要成分是盐酸)与“84”消毒液不能混用,若混用会产生黄绿色的有毒气体,其反应的离子方程式为。
-
(4) 某同学欲用
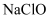 固体配制
固体配制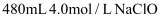 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量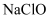 固体的质量为g;若所配得的
固体的质量为g;若所配得的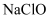 溶液在空气中经光照、久置后,溶液中
溶液在空气中经光照、久置后,溶液中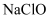 的物质的量浓度将(填增大、减小或不变)。
的物质的量浓度将(填增大、减小或不变)。
- Nobody knows ____. A. what wrongis. B . w
- . I don’t want _____ like I’m speaking ill of anybody, but t
- As a matter of fact, ________ tries again makes no differenc
- 某同学在研究电磁感应现象的实验中,设计了如图所示的装置,线圈A通过电流表甲、高阻值的电阻、滑动变阻器R和开关S连接到干电
- 10.把下列句子翻译成现代汉语。(1)假舟楫者,非能水也,而绝江河。 (2) 蚓无爪牙之利,筋骨之强,上食埃土,下饮黄泉
- 如图,在△ABC中,∠C=90°,点D是AB边上的一点,DM⊥AB,且DM=AC,过点M作ME∥BC交AB于点E. 求证
- 下列关于动物在生态系统中的作用的叙述中,不正确的是( ) A、促进生态系统中的生态平衡 B、帮助植物传粉,使之顺
- 下列有关叶绿体及光合作用的叙述,正确的是 A.破坏叶绿体外膜后,O2不能产生 B.植物生长过程中,叶绿体内各种色素的比例
- 2011年下半年以来,中小企业面临信贷紧、成本涨、订单减少等多种困难,“跑路”成为围绕在温州企业身边的新名词。温州企业民
- 2018年开学之初,长沙市中小学开展了“打赢蓝天保卫战”的活动。下列行动不利于“保卫蓝天”的是:( ) A.加强大
- 假如下学期即将到你校工作的外教Alice正在寻找一名学生助手,你有意承担这一工作,请根据下列信息向Alice 写一封申请
- 如图,把直角三角板的直角顶点O放在破损玻璃镜的圆周上,两直角边与圆弧分别交于点M、N,量得OM=8cm,ON=6cm,则
- ____in the mountains for a week, the two students were fina
- 补写出下列名句名篇中的空缺部分。任选两小题。(4分) ①_________,_______________。地势坤,君子
- (6分)现有下列药品和实验仪器。药品:石灰石、稀硫酸、稀盐酸仪器如下: (1)写出未标注的仪器名称:①
- 阅读下面的古诗文,回答1—2题。 (一)送友人 薛涛 水团莱葭夜有霜,月寒山色共苍苍。 谁言千里自今夕,离梦杳①如关塞长
- DNA分子复制时解旋酶作用于下列哪一结构( ) A. B. C.A—U
- 在电解水的实验中,可以直接观察到的现象是( ) A.水由氢、氧两种元素组成 B.有氢气和氧气产生,且体积比为2∶1C.在
- 下列离子反应方程式书写正确的是 ( ) A.在Ba(OH)2溶液中加入少量的硫酸氢钠溶液:Ba2++2OH-+2
- 1. Chuck s_____1_______ the crash and landson a d_____2_____

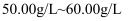
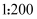 水溶液;餐饮具、瓜果等
水溶液;餐饮具、瓜果等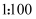 水溶液
水溶液


