第三节 氧化还原反应 知识点题库
-
(1) 是化合反应又是氧化还原反应的.
-
(2) 是分解反应又是氧化还原反应的.
-
(3) 是氧化还原反应又是置换反应的.
-
(4) 写出酸性氧化物与可溶性碱反应的化学方程式.
-
(5) 写出碱性氧化物与水反应的化学方程式.
 Cu+H2O
B . CO2+Ca(OH)2
Cu+H2O
B . CO2+Ca(OH)2  CaCO3↓+H2O
C . Fe2O3+3CO═2Fe+3CO2
D . 2Na+Cl2═2NaCl
CaCO3↓+H2O
C . Fe2O3+3CO═2Fe+3CO2
D . 2Na+Cl2═2NaCl
 2AlN+3CO合成.下列叙述正确的是( )
2AlN+3CO合成.下列叙述正确的是( )
-
(1) 配平化学反应方程式并标出电子转移的方向和总数:
Fe(NO3)3 +NaOH + Cl2 → Na2FeO4 +NaNO3 + NaCl + H2O,
-
(2) 上述反应中元素被氧化,发生还原反应的物质是
-
(3) 写出铁元素在元素周期表中的位置是第周期第族
-
(4) 写出上述反应中还原产物的电子式
-
(5) 若反应中转移了0.1 mol电子,则消耗了L Cl2(标准状况)。
①KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;1∶6
②Fe2O3+2Al  Al2O3+2Fe;1∶2
Al2O3+2Fe;1∶2
③SiO2+3C  SiC(硅为+4价)+2CO↑;1∶2
SiC(硅为+4价)+2CO↑;1∶2
④3NO2+H2O=2HNO3+NO;2∶1
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
B . 实验过程中两次用酸溶解,均需使用稀盐酸
C . KMnO4滴定草酸过程中,标准状况下每产生448mLCO2气体理论上转移0.02mole-
D . 滴定过程中若滴加KMnO4过快会发生反应4MnO
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
B . 实验过程中两次用酸溶解,均需使用稀盐酸
C . KMnO4滴定草酸过程中,标准状况下每产生448mLCO2气体理论上转移0.02mole-
D . 滴定过程中若滴加KMnO4过快会发生反应4MnO  +12H+=4Mn2++5O2↑+6H2O,将导致测定结果偏高
+12H+=4Mn2++5O2↑+6H2O,将导致测定结果偏高
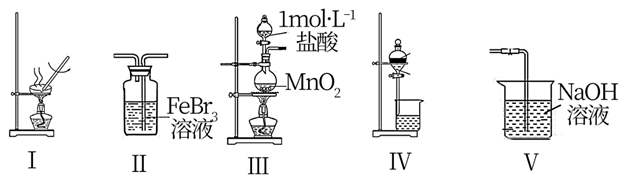
-
(1) I.消除氮氧化物有多种方法:
用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574 kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160 kJ/mol
③H2O(g)=H2O(l)△H=-44.0 kJ/mol
写出CH4(g)与NO2(g)反应生成N2(g),CO2(g)和H2O(l)的热化学方程式。
-
(2) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示:

①由图甲可知,SCR技术中的氧化剂为。
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应的温度分别为。
-
(3) II.氮氧化物的相互转化
T1℃时,在一密闭容器中发生反应4NO(g)
 N2(g)+2NO2(g)△H<0,其正反应速率表达式为:v正=k正·cn(NO),测得反应速率和浓度的关系如下表。
N2(g)+2NO2(g)△H<0,其正反应速率表达式为:v正=k正·cn(NO),测得反应速率和浓度的关系如下表。
则k正=mol-3·L3·s-1。下列对于该反应的说法正确的是。
A.当混合物颜色保持不变时就达到了化学平衡状态
B.当
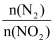 的比值保持不变时就达到了化学平衡状态
的比值保持不变时就达到了化学平衡状态C.达到化学平衡状态时,每消耗0.1 mol NO就会消耗NO20.05 mol
D.达到平衡后,若降低温度,则混合气体的颜色变浅
E.达到平衡后,若减小压强,则混合气体的平均相对分子质量将减小
-
(4) 利用测压法在刚性密闭容器中研究T2℃时4NO(g)
 N2(g)+2NO2(g)的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示:
N2(g)+2NO2(g)的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示: 
①20min时,NO的转化率为。
②T2℃时,用平衡分压代替平衡浓度表示的平衡常数Kp=MPa-1。[已知:气体分压(P分)=气体总压(P总)×体积分数]
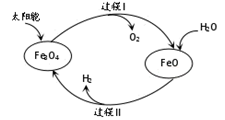
 2Fe3O4
B . 过程Ⅱ中H2为还原剂
C . 整个过程的总反应为:2H2O
2Fe3O4
B . 过程Ⅱ中H2为还原剂
C . 整个过程的总反应为:2H2O  2H2↑+O2↑
D . FeO 是过程Ⅰ的氧化产物
2H2↑+O2↑
D . FeO 是过程Ⅰ的氧化产物
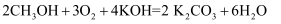 。下列说法正确的是( )
。下列说法正确的是( ) 
 ,此时乙池中银极增重3.2g
C . 甲池通入
,此时乙池中银极增重3.2g
C . 甲池通入  的电极反应为
的电极反应为  D . 反应一段时间后,向丙池中加入一定量盐酸,一定能使
D . 反应一段时间后,向丙池中加入一定量盐酸,一定能使 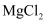 溶液恢复到原浓度
溶液恢复到原浓度
- 若不等式有唯一解,则的取值为( )A. B. C. D.
- 小张同学用下图所示的装置测定空气中氧气的含量,实验后发现所测定氧气的体积分数大于1/5。下列是小张同学对此实验误差的一些
- Mark Twain became rich because of his _________________ ( 小说
- 阅读材料,回答问题。(10分)材料一 1800--1870年英国煤产量(单位:万吨)年代
- 对我国地理区域特征的叙述正确的是( ) A.广袤新疆,绿洲农业 B.黄土高原,雪山连绵 C.港澳地区,重工业发达
- 钱穆在《中国历史政治得失》中指出:“汉宰相是采用领袖制的,而唐代宰相则采用委员制。”唐代宰相的“委员制”指 A.宰相一
- 以下表格内容中,有错误的选项是( )检测物质或生物 检测方法 显示颜色变化 A 酒精 酸性重铬酸钾检测 蓝绿色 B
- ①五岭逶迤腾细浪, 。
- 近年来,股票冷,债券热,债券与股票相比,两者有相同点,以下不属于相同点的是: A.都要承担一定风险 B.都可以在证券
- 2010年9月,100日元兑人民币为8.05元,而5月初,100日元兑人民币仅为7.2元,短短三个月,日元兑人民币进入“
- 将下列句子填写在横线处正确的一项是(2分)( )我往我的玻璃池塘里放进一些小小的水生物,它们叫食蚕。 。
- 2008年1月15日芬兰手机巨头诺基亚公司决定将于今年中旬关闭位于德国西部城市—波鸿的诺基亚手机工厂,并将这座工厂的生产
- 已知:2 SO2(g) + O2(g) 2SO3(g) △H = -196.6 kJ/mol 。现有SO2和O2各
- 各取0.1 mol铜分别投入足量的下列四种酸中(必要时可加热):①浓硫酸;②浓HNO3;③稀H2SO4;④稀HNO3。充
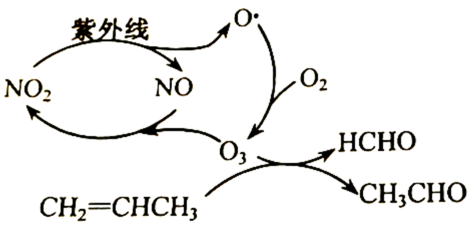
- 酸雨给人类生活和社会发展带来了严重危害。汽车尾气是导致酸雨的重要原因,为减少有害气体的排放,人们在汽车排气管上安装“催化
- 先秦人们种植的农作物中,黍适应粗放的耕种方式,而粟对水肥土壤要求较高,所以春 秋战国时期,粟却成为主要的作物。这主要得
- Though I have often heard this song _______. I have never he
- 依次填入下文横线处的句子,最恰当的一项是( ) 在先秦,主要有五种人格理想:墨子的苦行侠人格:_____ ;杨朱的贵我人
- 下图所示路线为: A.西汉攻打匈奴 B.张骞通西域 C.丝绸之路 D.佛教东来
- 在长度为l、横截面积为S、单位体积内的自由电子数为n的金属导体两端加上电压,导体中就会产生匀强电场.导体内电量为e的自由



