第二节 海水“晒盐“ 知识点题库
我国第四套人民币硬币中使用到镍(Ni)、铜、铁等金属.某兴趣小组决定探究Ni、Fe、Cu的金属活动性顺序.
-
(1) 【查阅资料】镍能与稀硫酸反应,生成可溶于水的NiSO4 , 并放出氢气.
①写出镍与稀硫酸反应的化学方程式.
②结合所学知识,(填“能”或“不能”)直接比较出Ni、Fe的金属活动性强弱.
-
(2) 【探究实验】(所用金属片均已用砂纸打磨.)
实验步骤
实验现象
结 论
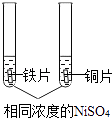
铁片表面有固体析出,
铜片表面
三种金属活动性由强到弱的顺序为
-
(3) 【实验反思】用镍片、硫酸亚铁溶液和(填化学式)溶液通过实验也能判断Fe、Ni、Cu的金属活动性顺序.
-
(4) 【迁移应用】某校化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,此外还有一些不溶性杂质.若废液直接排放到下水道不仅造成重金属污染,而且造成浪费,该校化学兴趣小组同学设计了如图废液处理方案,请回答有关问题:
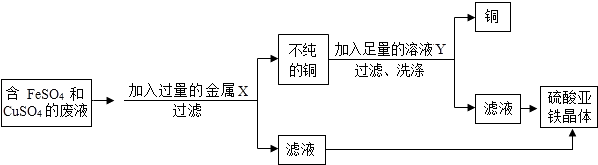
① 废液在加入金属X前需进行过滤,过滤时需要将圆形滤纸折叠处理.如图示中不该出现的情况是.
②加入过量金属X发生反应的化学方程式为,溶液Y是.
选择合适的词语填空(填标号即可):①分解;②溶解;③蒸发;④结晶;⑤化合;⑥挥发.
-
(1) 蔗糖放入水中逐渐消失;
-
(2) 铜绿受热后质量减轻;
-
(3) 敞口放置的酒精逐渐减少;
-
(4) 饱和KNO3 , 溶液降温析出晶体;
-
(5) 镁条燃烧后生成氧化镁;
-
(6) 加热食盐水有食盐析出.
氯化亚铜(CuCl)是一种白色粉末,不溶于水、乙醇(标准状况下沸点是78.2℃)及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用于有机合成工业中的催化剂.以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下:

-
(1) A溶液中溶质的化学式是;
-
(2) 写出反应 III的化学方程式;
-
(3) 反应 VI的化学方程式是:2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4 , 反应中化合价升高的元素是;
-
(4) 本工艺中可循环利用的物质是;
-
(5) 反应 VI后,过滤得到的CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品.70℃真空干燥的目的是.
KNO3和KCl在不同温度时的溶解度曲线如图所示,下列说法正确的是( )

A . 温度低于40℃时,KNO3的溶解度一定小于KCl的溶解度
B . 将等质量的KNO3和KCl的饱和溶液从60℃降温到20℃,析出晶体的质量KNO3大于KCl
C . 将10℃时KNO3、KCl的饱和溶液升温至60℃,KNO3溶液中溶质的质量分数比KCl大
D . 将20℃时100gKCl的饱和溶液升温至60℃,需要再加入11.5gKCl固体才能使溶液恰好饱和
实验室用CuO与稀H2SO4制备CuSO4·5H2O晶体,下列操作错误的是( )
A .  加粉末
B .
加粉末
B .  稀释
C .
稀释
C .  蒸发
D .
蒸发
D .  过滤
过滤
 稀释
C .
稀释
C .  蒸发
D .
蒸发
D .  过滤
过滤
如图为A,B,C三种物质的溶解度曲线,据图回答:

-
(1) 20℃时,A的饱和溶液中溶质的质量分数是.
-
(2) 20℃时,将25g A物质放入50g水中,充分搅拌,所得溶液的质量是g.
-
(3) 若将t1℃三种物质的饱和溶液分别升温到t2℃时,则三种溶液中溶质的质量分数由小到大的顺序是.
-
(4) 要从A物质中混有少量B物质得到A用方法.
下图为甲、乙、丙三种物质的溶解度曲线图,请回答下列问题:

-
(1) 当温度为℃时,甲、乙两物质的溶解度相等。
-
(2) 将10g甲物质(不含结晶水)配成t4℃时的饱和溶液,需水的质量为 g。
-
(3) 将t4℃时甲、乙、丙三种物质等质量的饱和溶液降温到t3℃,下列说法中正确的一项是___________ 。A . 三种溶液仍然为饱和溶液 B . 三种溶液中溶剂的质量大小关系为:甲=乙<丙 C . 三种溶液溶质质量分数的大小关系为:甲=乙>丙 D . 甲、乙析出晶体(不含结晶水)的质量相等,丙无晶体析出
如图是两种固体的溶解度曲线。

-
(1) 40℃时,氯化钠的溶解度(填“>”、“=”或“<”)硝酸钾的溶解度。
-
(2) 硝酸钾的溶解度随温度的升高而。
-
(3) 若将饱和的硝酸钾溶液从40℃降温到10℃,(填“有”或“无”)晶体析出。
-
(4) 20℃时,某实验小组取不同质量的硝酸钾,分别加入到100g水中,充分溶解后,所得溶液的质量与加入硝酸钾的质量对应关系如表:
实验一
实验二
实验三
实验四
硝酸钾的质量/g
20.0
25.0
30.0
35.0
所得溶液的质量/g
120.0
125.0
130.0
131.6
根据上表数据,实验二所得的溶液为(填“饱和”或“不饱和”)溶液;20℃时,硝酸钾的溶解度为g。
下列实验操作图示正确的是( )
A . 称量粗食盐  B . 倾倒稀盐酸
B . 倾倒稀盐酸  C . 过滤悬浊液
C . 过滤悬浊液  D . 移开蒸发皿
D . 移开蒸发皿 
 B . 倾倒稀盐酸
B . 倾倒稀盐酸  C . 过滤悬浊液
C . 过滤悬浊液  D . 移开蒸发皿
D . 移开蒸发皿 
下图是初中化学中常见的实验装置,请认真观察后回答有关问题:

-
(1) 写出带有标号的仪器名称:X,Y;
-
(2) 用A装置制取气体时,长颈漏斗应插入液面以下,其原因是;
-
(3) 用B装置来收集氢气时,气体应从(填“a”或“b”)端进入;
-
(4) C装置中①处得到的气体是;
-
(5) 用D装置除去粗盐中的杂质时,玻璃棒的作用是。
根据图中A,B,C三种固体的溶解度曲线回答:

-
(1) 在某一温度时,A,B两饱和溶液的溶质质量分数相等,此温度为℃;
-
(2) 在t3℃时,将30 g A物质充分溶解在50 g水中,所得溶液的质量为g;
-
(3) 要使C的饱和溶液变为不饱和溶液,可采用的一种方法是。
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:

-
(1) 20℃时,饱和溶液的溶质质量分数相等的物质是。
-
(2) 不改变溶液的成分,将丙的不饱和溶液变为饱和溶液的方法是。
-
(3) 20℃时,把60 g甲物质加入50g水中,得到溶液的质量为g,若要得到溶质质量分数为50%的甲溶液,继续进行的具体操作是。
A、B两种固体物质的溶解度曲线如图所示,请按要求回答下列问题:

-
(1) 温度为0℃时溶解度AB(填“>”“<”或“=”)。
-
(2) 温度变化对A、B溶解度影响较大的是(填“A”或“B”)。
-
(3) 若将A从A、B的混合溶液中析出,宜采用的方法是。
-
(4) 40℃时B的饱和溶液的溶质质量分数为(精确至0.1%),若将50℃时80gA的饱和溶液降温至40℃,析出A的质量是。
根据KNO3和NaCl的溶解度曲线,回答下列问题:

-
(1) 10℃时,溶解度较小的是(选填“KNO3”或“NaCl”);
-
(2) 根据溶解度曲线分析,从海水中获得粗盐不采用降温结晶方法的原因是。
-
(3) 下列说法正确的是。
A 将不饱和的KNO3溶液变为饱和,可采用加KNO3的方法
B 20℃时,KNO3和NaCl两种饱和溶液中,所含溶质质量NaCl大于KNO3
C 30℃时,溶质质量分数为20%的KNO3溶液甲,降温至20℃得到溶液乙,再降温至10℃得到溶液丙,三种溶液中溶质的质量分数大小关系:甲=乙>丙
如图是a、b两种固体物质的溶解度曲线。下列说法中错误的是( )
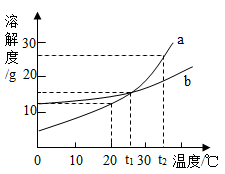
A . a、b两种物质都属于易溶性物质
B . t2℃时,将a、b的饱和溶液分别降温到t1℃时,析出的晶体的质量a比b多
C . t1℃时,a、b两种物质饱和溶液中溶质的质量分数相等
D . 当a中含有少量b时,可以用降温结晶法提纯a
如表是NaCl、KNO3在不同温度时的溶解度:( )
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
据此数据,下列说法正确的是
A . 20℃时,将20gNaCl加入50g水中,得到溶液
B . 50℃时,KNO3溶液的溶质质量分数大于NaCl溶液的溶质质量分数
C . 降温时,KNO3溶液析出的固体质量大于NaCl溶液析出的固体质量
D . NaCl和KNO3的溶解度曲线在20℃~30℃之间相交
能按照溶解、过滤,蒸发的实验操作顺序分离的一组固体混合物是( )
A . MnO2和KCl
B . CuO和木炭粉末
C . NaNO3和NaCl
D . BaSO4和CaCO3
归纳小结是学好化学的重要方法。下列说法完全正确的一组是( )
A . 同种元素组成的物质叫做单质
B . 过滤后滤液仍然浑浊,其原因可能是滤纸未紧贴漏斗内壁
C . 点燃氢气与空气的混合物一定会发生爆炸,因此点燃可燃性气体前一定要验纯
D . 晓晓在化学实验课上建议,用磁铁吸一下五角硬币,以此鉴别硬币能否被磁铁吸引。就这一过程而言,属于科学探究环节中的设计实验
下图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述正确的是( )

A . t3℃时将甲、乙两种物质的饱和溶液降温至t2℃,析出晶体甲>乙
B . t2℃时的甲、乙、丙的饱和溶液降温到t1℃,溶液中溶质质量分数大小顺序为:丙>乙>甲
C . 若要将组成在M点的甲溶液转变为N点的甲溶液,可以采用的方法是:降温到t2℃、过滤、升温到t3℃
D . 若甲物质中混有少量乙物质,不可以用降温结晶的方法提纯甲
下表是甲和乙在不同温度时水中的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | 甲 | 30 | 33 | 35 | 38 | 41 |
乙 | 21 | 31 | 45 | 65 | 88 | |
-
(1) 在30℃时,物质甲的饱和溶液中,溶质与溶剂的质量比为。
-
(2) 由表中的数据分析可知,甲和乙在某一温度时具有相同的溶解度xg。则x取值范围是。
-
(3) 探究20℃时配制乙溶液过程中,溶质质量分数与加入水的质量关系。结合图像判断,坐标图中符合实验结果的描点可能是(填序号)。



-
(4) 下列说法不正确的是(填序号)。
①40℃时,甲、乙的饱和溶液中溶质的质量乙>甲
②物质甲中含有少量乙时,可以采用蒸发结晶的方法提纯甲
③大多数固体物质的溶解度随温度的升高而增大
④分别将50℃时甲、乙的饱和溶液降温至20℃,所得溶液中溶质的质量分数乙大于甲
最近更新
- ......
- Rita and Anna have finished their homework, ______? A. have
- 阅读的另一首诗《水调歌头 游泳》,完成下面各题: 水调歌头 游泳 一九五六年六月 才饮长江水,又食武昌鱼。万里长江横渡,
- We’ve heard it before---we’ve heardit on the news, from te
- “假说—演绎法”是现代科学研究中常用的一种方法,下列属于孟德尔在发现基因分离定律时的“演绎”过程的是() A.生物的性状
- “三个代表”重要思想深化了对中国特色社会主义的认识,表现在 (1)进一步回答了什么是社会主义,怎样建设社会主义的问题(2
- 为迎接中国森博会,某商家计划从厂家采购A,B两种产品共20件,产品的采购单价(元/件)是采购数量(件)的一次函数.下表提
- 梁启超评价辛亥革命具有“空前绝后的大意义”。“第一,觉得凡不是中国人都没有权来管中国人的事;第二,觉得凡是中国人都有权来
- 京是一座饱经沧桑的城市,是近代中国的缩影。……它是中国近代史的起点,也是中国近代史的终点。”以下内容支持这一观点的是①近
- 李宁为妈妈设计了一份午餐食谱:米饭、清炖牛肉、麻辣豆腐。再加上下列哪种食物后可以让这份食谱营养更合理
- 已知A B C D E F分别是硫酸铜、氢氧化钠、铁、盐酸、氧化铁、二氧化碳中的一种物质,用六个圆表示这六种物质,在图中
- 为杜绝操作工手指损伤事故的发生,某厂家设计制造的切纸机,必需将两只手同时分别按住左、右开关,切纸机才能正常工作。下列电路
- 未来三年,国家将投入8500亿元用于缓解群众“看病难,看病贵”问题.将8500亿元用科学记数法表示为( )亿元
- 运用下列各种细胞工程技术培育生物新品种,操作过程中能形成愈伤组织的是 ①植物组织培养②植物体细胞杂交③动物细胞培养④转基
- 根据右表判断,下列说法正确的是 A.铝的相对原子质量是13 B.钠离子核外有三个电子层 C.第二、三周期元素的原子从左至
- The southern provinces in China were struck by a rare snow a
- 14.补写出下列名篇中的空缺部分。 (1)在《念奴娇·赤壁怀古》中苏轼以洒酒祭奠江月的豪举来抒发人生似梦,壮志难酬的感叹
- 下面有关生物实验原理、方法或结果的描述中正确的是 ( ) ①“观察植物细胞有
- 已知(1+x+x2)(x+)n的展开式中没有常数项,n∈N*且2≤n≤8,则n=_____________.
- 时下,在长三角、珠三角、北京等一些经济发达地区,自驾游、农家乐等休闲旅游逐渐成为一种潮流,同时,数字娱乐、艺术欣赏、茶艺



