第四节 酸碱中和反应 知识点题库
①用生石灰作食品干燥剂 ②用熟石灰和硫酸铜配制波尔多液
③施用熟石灰改良酸性土壤 ④用氢氧化钠溶液处理泄漏的浓硫酸
(1)酸与碱之间能发生 反应.
(2)氢氧化钙可以用来调节土壤的 性,它的水溶液常用来检验 气体的存在.
(3)一定量的稀硫酸与氢氧化钠溶液混合,滴入几滴酚酞溶液,混合液显红色,可推断该溶液的pH(填“>”、“<”或“=”) 7.要准确测定该溶液的pH,需要用到的仪器是 .
-
(1) 根据实验现象,你认为氢氧化钠溶液与稀硫酸(填“能”或“不能”)发生化学反应,理由是有.
-
(2) 针对上述实验,你还想探究的问题是有.
①碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液
②氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物;
③酸碱发生中和反应生成盐和水,所以生成水的反应一定是中和反应.
-
(1) 近年来由于空气污染而形成酸雨,向酸雨中滴加紫色石蕊溶液,溶液变色
酸雨会导致土壤的pH(填“变大”或“变小”),加入适量的可改良酸性土壤.
-
(2) 利用二氧化碳生产碳酸型饮料,发生反应的化学方程式为
 K2MnO4+MnO2+O2↑
C . CaO+H2O═Ca(OH)2
D . Ca(OH)2+2HCl═CaCl2+2H2O
K2MnO4+MnO2+O2↑
C . CaO+H2O═Ca(OH)2
D . Ca(OH)2+2HCl═CaCl2+2H2O

-
(1) “O“中填写的离子符号为;
-
(2) 请根据如图信息,从微观角度分析,该反应的实质是结合生成水分子;
-
(3) 由图可知,构成物质的微粒有;(选填“分子”“原子“或“离子”)
-
(4) 请另外再写一个符合上述反应实质的化学方程式。
-
(1) (探究目的)探究所得溶液的酸碱性
(提出猜想)所得溶液可能呈碱性,也可能呈性,还可能呈性.
(实验验证)
实验操作
实验现象
结论
用试管取该溶液1﹣2mL,滴入1﹣2滴无色酚酞试液,振荡
无色酚酞试液变
溶液呈碱性
无色酚酞试液不变色
溶液呈
-
(2) (分析与思考)
若溶液呈碱性,则溶液中使其呈碱性的离子是(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入溶液,直到不再产生沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为.
-
(3) 若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为;若无明显现象,则呈中性.

-
(1) 图甲为酸碱中和反应实验的操作及有关物质质量的变化曲线。则c点时溶液的颜色为,b点时溶液中含有的溶质是。
-
(2) 图乙为实验室用5%的过氧化氢溶液制取氧气的装置。装置内发生反应的化学方程式为,装置中小试管的作用是。为配制300g溶质质量分数为5%的过氧化氢溶液需要溶质质量分数为30%的过氧化氢溶液的质量是g。

-
(1) 实验一:取5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的反应方程式为。
-
(2) 实验二:对实验一反应后溶液中的溶质进行探究。
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想不合理,其理由是。
-
(3) 【设计实验】
实验操作
实验现象
实验结论
取反应后的溶液于试管中,加入
猜想三成立
-
(4) 【拓展应用】我国土壤的酸碱性有“南酸北碱”之说法,你认为需向酸性土壤中加入进行改良。
-
(1) (知识积累)①稀盐酸和NaOH溶液反应无明显现象;
②BaCl2溶液呈中性;
③向稀盐酸中逐滴加入过量NaOH溶液,所得溶液的pH变化曲线合理的是(填字母)。

-
(2) (演示实验)甲组同学将一定量稀盐酸逐滴加入到盛有NaOH溶液的小烧杯中,实验过程中却看到有气泡产生。他们怀疑是不是拿错了药品?经检验确认没有拿错药品。
(提出问题)为什么会产生气体?
(分析回题)可能是氢氧化钠溶液已变质,变质的原因是(用化学方程式表示)。
-
(3) (猜想假设)针对疑问和分析,大家对NaOH溶液中的成分纷纷提出猜想。
猜想1:溶液中有NaOH和Na2CO3
猜想2:溶液中只有Na2CO3
(实验探究)为了验证猜想,同学们进行如下实验探究:
实验方案
Ⅰ、测溶液pH
Ⅱ、滴加足量BaCl2溶液;取反应后的上层清液滴加无色酚酞溶液
实验操作



实验现象
试纸变色,对比比色卡,pH>7
产生白色沉淀
实验结论
溶液中有NaOH
溶液中有
溶液中有NaOH
(得出结论)通过探究,同学们一致确定猜想1是正确的。
-
(4) (评价反思)老师对本组同学能用两种方法进行探究,并且得出正确结论给予肯定,同时指出上述实验方案中有一个是错误的,请你帮同学们找出错误的方案并说明原因。
-
(5) (反思拓展)通过探究可知氢氧化钠必须密封保存。为了防止药品与空气中的某些成分反应而变质,实验室中必须密封保存的药品还有很多,试举一例(填药品名称)。
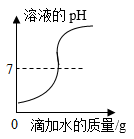 向一定量的稀盐酸中滴入水
B .
向一定量的稀盐酸中滴入水
B .  O2的溶解度与温度、压强的关系
C .
O2的溶解度与温度、压强的关系
C . 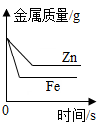 在等质量、等质量分数的两份稀硫酸中,分别加入过量且等质量的铁粉、锌粉
D .
在等质量、等质量分数的两份稀硫酸中,分别加入过量且等质量的铁粉、锌粉
D .  向稀硫酸和硫酸铜的混合溶液中加入足量的氢氧化钡溶液
向稀硫酸和硫酸铜的混合溶液中加入足量的氢氧化钡溶液
- (2009江苏镇江调研)一曲富含现代音乐元素的奥运歌曲《北京欢迎你》红遍全国。而这首灵感源自童谣的歌曲是用中国古代宫、商
- 已知函数y=f(x+1)定义域是[﹣2,3],则y=f(2x﹣1)的定义域( ) A.
- 请看右图,在这一购物流程中A.货币执行了流通手段职能 B.货币充当了价值尺度职能 C.货币表现了其它商品的价
- A high public tolerance for - and lowpublic awareness of -
- 如图所示,一个装满水的饮料瓶,正放在水平桌面上时,瓶底对桌面的压力为Fa,压强为pa,倒放在水平桌面上时,瓶盖对桌面的压
- 阅读下面一首诗,回答问题 北陂杏花 王安石 一①陂春水绕花身,花影妖娆各占春。 纵被春风吹作雪,绝剩南②
- W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可
- 为提纯下列物质(括号内为杂质),所选用的试剂和分离方法均正确的是 ( ) A、溴乙烷(乙醇):水,分液
- 下表是某年人口流动的地区构成,分析完成2- 3题。2.表中显示人口流动特征是 A.城市到农村 B.城市到城市 C.中西部
- 民生问题是2010年“两会”代表委员关注的热点。据此回答32—33题。 “两会”期间,代表委员们就社会热点问题,展开讨论
- 亚硝酸(HNO2)既可作氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的是( ) A.N2O5
- 如右图,一有界区域内,存在着磁感应强度大小均为B,方向分别垂直于光滑水平桌面向下和向上的匀强磁场,磁场宽度均为L,边长为
- 测得某金属冶炼厂的酸性工业废水中,含有一定量的Fe3+、Cu2+、Au3+等离子。按照“变废为宝”的原则,设计了下图中的
- Each time tourists travel to Beijing, they_______ the Forbid
- 有四种粒子的结构示意图,下列说法不正确的是( ) ① ②
- Books are made __________ paper while paper is mainly made _
- Mrs. King put acoat ________ the sleeping girl to keep her w
- 下列关于细胞核的说法,不正确的是 A.所有的真核细胞均有细胞核 B.细胞核是遗传物质贮存和复制的场所 C.DNA主要
- 设向量a=(-2sinα,2cosα)(0<α<π),向量b=(-,0),则a·b的夹角是 A.α
- At a laboratory in Germany ,volunteers slide into a machine



