第四节 酸碱中和反应 知识点题库
-
(1) 夏天天气炎热时,鱼塘里的鱼为什么总是接近水面游动?
-
(2) 废弃塑料的急剧增加会带来“白色污染”,请你为解决“白色污染”问题提出一条合理化建议.
-
(3) 有些胃药中含有氢氧化镁,它起什么作业?
小红同学进行酸碱中和反应的实验(如图所示).她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,震荡,观察到试管中溶液颜色没有变化.于是她对烧杯中的溶液进行了以下探究:

-
(1) 小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸过量.
小明同学却断定不可能“氢氧化钠有剩余”,他的理由是:;
-
(2) 他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证.请根据相关内容填写如表:
试验方法
可能观察到的现象
结论
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中.
如果
则盐酸过量
如果
则盐酸与氢氧化钠恰好完全反应
-
(3) 经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的.你认为其中不正确的是 (填序号).A . 生锈的铁钉 B . 碳酸钠粉末 C . 硫酸钠粉末 D . 氢氧化铜
-
(4)
如图曲线能够表示小红所做试验中溶液pH变化趋势的是(填序号).

 向盛有部分变质的氢氧化钠溶液的烧杯中滴加稀硫酸至过量
B .
向盛有部分变质的氢氧化钠溶液的烧杯中滴加稀硫酸至过量
B .  向盛有一定量的氢氧化钠溶液的烧杯中逐滴加入pH=2的稀盐酸至过量
C .
向盛有一定量的氢氧化钠溶液的烧杯中逐滴加入pH=2的稀盐酸至过量
C .  相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应
D .
相同质量的镁、锌分别与足量的溶质质量分数相同的稀盐酸反应
D .  某温度时,向一定量的饱和氢氧化钙溶液中加入少量氧化钙,再恢复到原温度
某温度时,向一定量的饱和氢氧化钙溶液中加入少量氧化钙,再恢复到原温度

-
(1) A是;
-
(2) B是;
-
(3) A和B反应的化学方程式为:.
 通电分解水
B .
通电分解水
B .  向一定量稀硫酸中加氧化铜
C .
向一定量稀硫酸中加氧化铜
C .  向一定量的硝酸银溶液中加铜
D .
向一定量的硝酸银溶液中加铜
D .  向一定量盐酸中滴加氢氧化钠溶液
向一定量盐酸中滴加氢氧化钠溶液

-
(1) 图1,焙制糕点所用的发酵粉中含有(填化学式)和有机酸.
-
(2) 图2,为了适应北方春季低温气候,在种植叶类蔬菜时适宜施加的一种复合肥是(填化学式).
-
(3) 图3中农作物应施加的一类化肥是①(填种类),该化肥能促进植物生长,增强植物的②能力.
-
(4) 图4,人们常向土壤中加入适量①(填俗称)以中和其酸性,但改良后不能立即施加铵态氮肥的原因是②.
A.化学与安全 | B.化学与健康 |
煤气泄漏应立即关闭阀门,禁止烟火 油锅着火用锅盖盖灭 | 食用松花蛋时用食醋除去涩味 氮气用作食品保护气 |
D.化学与生活 | D.化学与农业 |
用洗洁精去除餐具油污 用铝质饭盒长时间贮存酸性食品 | 用熟石灰改良酸性土壤 二氧化碳用作农业生产的气体肥料 |
(实验探究)
-
(1) 方案一:某同学按如图所示的方法先向试管中加入约2mL NaOH溶液,再滴入几滴酚酞溶液,溶液变红色.然后慢慢滴入稀硫酸,边滴边振荡,直至溶液恰好变为色,证明NaOH溶液与稀硫酸恰好完全反应.

①请指出如图操作中的不符合题意.
②写出NaOH溶液与稀硫酸反应的化学方程式.
-
(2) 方案二:
实验步骤
实验现象
结论
取2mLNaOH溶液于试管中,滴入一定量的稀硫酸,振荡后加入镁条
若
稀硫酸过量
若没有现象
NaOH溶液与稀硫酸恰好完全反应
-
(3) (实验反思)
方案一在滴入稀硫酸的过程中,若观察到曾有少量气泡出现,请分析产生气泡的原因可能是(写出一条即可).
-
(4) 有同学提出方案二不能证明NaOH溶液与稀硫酸恰好完全反应,其原因是.为此,还需要选择(填一种试剂),再进行实验即可.
-
(5) (拓展应用)
请举一例说明中和反应在生产生活中的应用.

请根据图示回答下列问题:
-
(1) H的化学式为
-
(2) A和B反应的化学方程式为。
(查阅资料)蚁酸化学名称叫甲酸,化学式为  ,一定条件会分解为两种氧化物。白色无水硫酸铜粉末遇水变蓝。
,一定条件会分解为两种氧化物。白色无水硫酸铜粉末遇水变蓝。
(提出问题)蚁酸的酸碱性及分解产物是什么?
-
(1) (猜想与假设)猜想①:蚁酸的分解产物是水和二氧化碳;猜想②:蚁酸的分解产物是水和一氧化碳;猜想③:蚁酸的分解产物是一氧化碳和二氧化碳。
经讨论,小组同学认为猜想③是错误的,理由是。
-
(2) (实验探究)

探究蚁酸的酸碱性。用
 试纸测得蚁酸溶液的
试纸测得蚁酸溶液的 
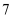 (填“
(填“  、
、 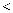 或=”),证明蚁酸溶液呈酸性。
或=”),证明蚁酸溶液呈酸性。 -
(3) 探究蚁酸分解的两种产物。为了确认蚁酸分解的所有产物,小组同学设计实验,将蚁酸分解的产物通入如图所示的实验装置,并观察现象。
(现象与结论)实验中观察到
 中无水硫酸铜变蓝,
中无水硫酸铜变蓝,  中澄清石灰水未变浑浊,
中澄清石灰水未变浑浊,  中黑色粉末逐渐变红,
中黑色粉末逐渐变红,  中澄清的石灰水变浑浊。写出
中澄清的石灰水变浑浊。写出  中发生的反应的化学方程式;通过对实验现象的分析,上述猜想正确。
中发生的反应的化学方程式;通过对实验现象的分析,上述猜想正确。 -
(4) (实验反思)从环保的角度考虑,上述实验装置设计上存在的不足之处是。
-
(5) (拓展应用)人们被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒,下列物质中你会选择的物质是(填选项)。
A.氢氧化钠 B.食醋 C.肥皂水
 和
和  装置溶液均为澄清石灰水,其作用(填“相同”或“不同”),其中
装置溶液均为澄清石灰水,其作用(填“相同”或“不同”),其中  的作用是。
的作用是。

-
(1) 此反应操作是向溶液中滴加另一种溶液,化学方程式为。要得到中性溶液,需借助试液,当溶液恰好中和时,现象是。
-
(2) M点所含的离子有。
-
(1) 探究一:按图示进行实验。

向A烧杯中滴入2滴无色酚酞试液后,振荡,烧杯中溶液呈现红色,说明氢氧化钠溶液显(选填“酸性”、“中性”或“碱性”)。
-
(2) 在B烧杯中接着滴入稀盐酸,用玻璃棒不断搅拌的原因是。写出氢氧化钠与稀盐酸反应的化学方程式。
-
(3) 当C烧杯中溶液呈现无色时,溶液中(填“一定”或“不一定”)含有氢离子。请你设计一个实验来证明C烧杯的溶液中一定含有过量的稀盐酸。
实验操作
实验现象
实验结论
溶液中含有过量的稀盐酸
-
(4) 探究二:通过pH传感器和滴数传感器完成以下实验:向40mL溶质质量分数为0.4%的氢氧化钠溶液中逐滴滴入稀盐酸,测定溶液的pH随滴入稀盐酸的体积(单位为ml)发生变化情况如图所示。

在A点时,溶液中所含溶质的化学式为。
-
(5) 当pH=7时,消耗稀盐酸的体积为,实验所用氢氧化钠溶液和稀盐酸的密度近似看作1g/mL,计算稀盐酸的溶质质量分数为。
-
(6) 小强利用温度传感器测得反应过程中溶液温度发生变化的曲线如图所示。该曲线说明中和反应是(选填“吸热”或“放热”)反应:在20s-44s之间,溶液pH的变化趋势为。

-
(7) 探究三:经过对中和反应一系列研究后,真真小组又通过实验探究:证明酸与碱反应有水生成。
(查阅资料)a.变色硅胶吸水后由蓝色变红色
b.无水醋酸在常温下为无色液体
c.无水醋酸和氢氧化钠固体混合后生成醋酸钠和水
(实验方案)按下图所示,首先分别往4支试管中装入对应的试剂,然后迅速塞紧橡胶塞。

能证明酸与碱反应生成水的现象是。
-
(8) 装入试剂后迅速塞紧橡胶塞的目的是。

-
(1) a点溶液中所含有的阳离子是(填离子符号)。
-
(2) 当pH=7时,所得溶液中溶质质量分数为多少?(写出计算过程)

-
(1) 写出图Ⅰ反应的化学方程式:。
-
(2) 结合图Ⅱ的微观图示,判断图Ⅲ中①代表 (用化学符号表示),若要验证反应后溶液中稀盐酸有剩余,下列操作可行的是 (填字母)。
A.取样,加入CuO粉末
B.取样,滴加NaOH溶液
C.取样,加入CaCO3粉末
D.取样,滴加AgNO3溶液
-
(1) 某同学利用数字化传感设备,探究硫酸和烧碱溶液反应过程中温度和pH的变化,测定结果如图所示。

通过图像可知,该实验是将(填“硫酸”或“烧碱溶液”)滴入另一溶液中;该反应属于反应(填“吸热”或“放热”);当滴加液体的体积为10mL时,溶液中的溶质为。
-
(2) 现有一包固体粉末,可能由碳酸钙、氧化钙、碳酸钠中的一种或几种组成。为确定其组成,称量20g固体粉末,进行了如下图所示的实验:

①根据上述实验可以确定白色沉淀是;
②为进一步确定固体粉末的成分,将白色沉淀烘干称量其质量是10g,将X溶液蒸干称量其质量是11.7g,最终可知固体粉末是由(填化学式)组成的。
- 如图,△ABC的面积为63,D是BC上的一点,且BD∶CD=2∶1,DE∥AC交AB于点E,延长DE到F,使FE∶ED=
- 名著阅读。(5分)(1)《三国演义》第17回中,曹操的马匹受惊,践踏了麦田,曹操欲自刎谢罪,被军士阻拦,于是曹操用
- 阅读下面古诗词,完成第7-8题。(4分) 酬乐天扬州初逢席上见赠 刘禹锡 巴山楚水凄凉地,二十三年弃置身。 怀旧空吟闻笛
- 20世纪30年代,德国法西斯专政建立的过程与日本相比,突出的特点是 A.通过暗杀、政变等恐怖事件掌握国家政权
- 夜上受降城①闻笛 李益(4分)回乐烽前沙似雪,受降城外月如霜、不知何处吹芦管,一夜征人尽望乡。① 降城:贞观二十年,
- 4.工业生产果汁时,常常利用果胶酶破除果肉细胞壁以提高出汁率,为研究温度对果胶酶活性的影响,某学生设计了如下实验:①将果
- 在下图中属于次级卵母细胞继续分裂过程中染色体平均分配示意图的是( )
- 如图,线圈M和线圈N绕在同一铁芯上。M与电源、开关、滑动变阻器相连,P为滑动变阻器的滑动端,开关S处于闭合状态。N与电阻
- ---It’s disappointing that Johnfailed in the maths exam.
- 复数,,那么复数在复平面上对应的点所在的象限是 A.第一象限 B.第二象限 C.
- 阅读下面短文,根据所读内容在表格中的空白处填入恰当单词 注意:每个空格只填一个单词 There are many
- 除夕之夜,小强一家人坐在一起看电视。爷爷深有感触地说:“我年轻的时候,只能听广播。”爸爸接着说:“我年轻的时候,要跑到几
- 南北朝时期范缜指出:“形存则神存,形谢则神灭”,物质实体乃产生精神的基础。十八世纪英国主教贝克莱说:“我说我写字的桌子存
- 24.______ life began on earth is one of the biggest puzzles
- 下列变化中,没有新物质生成的是 ( )
- 下列说法正确的是 A.因为钠盐不吃不排,钾盐不吃也排,所以在不进食的情况下,可以维持钠盐平衡,但钾盐不可以 B.对于高烧
- 杨家将的故事流传至今已有800多年了,这些故事反映的是澶渊之盟订立之前A.北宋与辽的争战B.北宋与金的争战C.南宋与辽的
- 商鞅变法既是当时经济发展的需要,也是争霸战争现实压力的必然结果。下列变法中的哪一举措最能体现出当时经济发展的需求?
- 孟浩然的《过故人庄》中表现恬静的农家生活的诗句是: , 。
- 下列叙述正确的是() A.化学反应中都会放热 B.在化学反应中只有燃烧才能放热 C.化学反应伴随着能量变化 D.人类利用



