高考二轮复习知识点:原子轨道杂化方式及杂化类型判断4
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
【化学-选修3:物质结构与性质】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等.回答下列问题:
|
|
| 2. 综合题 | 详细信息 |
|
[化学--选修3:物质结构与性质]东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
|
臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为
 和 和  ,NOx也可在其他条件下被还原为N2。 ,NOx也可在其他条件下被还原为N2。
|
|
| 4. 综合题 | 详细信息 | ||||||||||
|
【选修三:物质结构与性质】
在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu2微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要村料。回答下列问题:
|
|||||||||||
| 5. 综合题 | 详细信息 |
|
[选修3——物质结构与性质]
|
|
| 6. 综合题 | 详细信息 |
|
铜是人类最早使用的金属之一,最近科学家发现 Cu 元素有很强的杀菌作用,还可代替Al
布线在硅芯片上。用黄铜矿(主要成分为 CuFeS2)生产粗铜,其反应原理如下:
回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
B、Si和P 是组成半导体材料的重要元素。回答下列问题
|
|
| 8. 综合题 | 详细信息 |
|
闪锌矿与纤锌矿的主要成分均为ZnS。在一定条件下ZnO与ZnS、Se共热可制备荧光材料ZnSe。回答下列问题:
|
|
| 9. 综合题 | 详细信息 |
|
硒(Se)是一种非金属元素。可以用作光敏材料、电解锰行业催化剂、动物体必需的营养元素和植物有益的营养元素等。请回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
海洋是元素的摇篮,海水中含有的大量元素在生产、生活、科学研究等多方面具有重要作用。回答下列问题。
|
|
- 2015年广西柳州市柳铁一中高考化学模拟试卷(8)
- 2017年高考化学备考复习专题三:氧化还原反应
- 2016-2017学年山东省济宁市兖州实验高中高三上学期期中化学试卷
- 云南省昆明市2018-2019学年高考理综-化学4月模拟考试试卷
- 上海市奉贤区2017-2018学年高考理综-化学模拟考试试卷
- 2015-2016学年山东省淄博市高青一中高一下学期月考化学试卷(4月份)
- 2015-2016学年安徽省合肥市高升学校高二上学期期中化学试卷
- 天津市和平区2017-2018学年高考理综-化学一模考试试卷
- 天津市静海区大邱庄中学2019-2020学年高三上学期化学第一次月考试卷
- 四川省乐山市2017-2018学年高三理综-化学二模考试试卷
- 2016-2017学年河南省周口市淮阳县实验高中高二上学期开学化学试卷
- 2016-2017学年安徽省宣城市六校联考高二下学期期中化学试卷
- 已知是定义在上的奇函数,且,若、,,有; (1)判断函数在上的单调性,并证明你的结论; (2)若≤对所有的、恒成立,求实
- 小球由地面竖直上抛,上升的最大高度为H,设所受阻力大小恒定,地面为零势能面。在上升至离地高度h处,小球的动能是势能的两倍
- It was in the Ming Dynasty __________ the Great Wall was reb
- 城市是国家和地区经济的“桥头堡”,合理发展城市非常重要。完成下面试题: 下列四图,能正确反映城市发展一般规律的是下列途径
- 人们食用的大豆油,主要来自大豆种子的() A.胚芽 B.子叶 C.胚轴 D.胚根
- 世界上人口最多的国家是( ) A.俄罗斯 B.中国 C.美国
- 阅读下列材料并回答问题: “中国之法,非不变也,中兴以后,讲求洋务,三十余年,创行新政,不一而足。然屡见败衄、莫克振救。
- In 1896, the first modern Olympic Games(现代奥运会) were on in At
- 用分子的观点对下列常见现象的解释,错误的是A.热胀冷缩——分子的大小随温度变化而改变B.花香四溢——分子在不停运动C.酒
- 12月4日是我国现行宪法(1982年宪法)正式颁布的日子,早在2001年就被设立为全国法制宣传日。根据中共十八届四中全会
- 沙漠治理是公认的世界性难题,鄂尔多斯人另辟溪径,变“征服沙漠”为“善待自然”。他们把沙漠绿化、沙产品开发和生态旅游有机结
- 二次函数y=ax2+bx与指数函数y=()x的图象只可能是( )
- 阅读《丈量幸福的尺寸》,回答20-23题(13分) 丈量幸福的尺寸 ①4岁的时候,你会为得到一颗糖果而快乐;14
- 下列关于蛋白质的叙述中错误的是 () A.蛋白质是两性化合物 B.蛋白质溶液中分别加入浓NaCl溶液、CuSO4溶液,其
- 有机物A的结构简式为,它可通过不同化学反应分别制得B、 C、D和E四种物质。请回答下列问题: (1)指出反应的类型
- 下列关于化学反应的实验现象描述不正确的是( ) A.铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成黑色固体 B.
- 下列有关性质的比较,不能用元素周期律解释的是( ) A.酸性:H2SO4>H3PO4 B.
- 已知定义在R上的函数f(x),对任意x∈R,都有f(x+8)=f(x)+f(4)成立,若函数f(x+1)的图象关于直线x
- 最近科学家发现了一种与天体中的中子星构成类似的,只由四个中子构成的粒子,这种粒子称为“四中子”,也称为“零号元素”。有关
- The FrenchRevolution was successful in________society of ine







 中的溶解度:
中的溶解度: 
 位于元素周期表中第四周期族,基态
位于元素周期表中第四周期族,基态  可与
可与  ,反应生成
,反应生成  ,新生成的化学键为键。
,新生成的化学键为键。  的结构为体心立方堆积,晶胞参数为
的结构为体心立方堆积,晶胞参数为  中锰的原子半径为pm。已知阿伏加德罗常数的值为
中锰的原子半径为pm。已知阿伏加德罗常数的值为 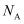 ,
,  的理论密度
的理论密度 
 。(列出计算式)
。(列出计算式)

 蓝色沉淀
蓝色沉淀  ,则 C 原子的坐标参数为 。若该晶体的密度为 dg/cm3 , 阿伏加德罗常数的值为NA , 则该晶胞中 Cu 原子与 O 原子之间的距离为 pm。(用含 d 和 NA的式子表示)。
,则 C 原子的坐标参数为 。若该晶体的密度为 dg/cm3 , 阿伏加德罗常数的值为NA , 则该晶胞中 Cu 原子与 O 原子之间的距离为 pm。(用含 d 和 NA的式子表示)。 


 。
。 pm和
pm和  pm,则Ⅱ的空间占有率为。
pm,则Ⅱ的空间占有率为。 的电负性由大到小的顺序为。制备
的电负性由大到小的顺序为。制备  过程中会产生少量
过程中会产生少量  ,其中
,其中  原子采用杂化,
原子采用杂化,  晶胞相似(如图),晶胞中距离最近的两个
晶胞相似(如图),晶胞中距离最近的两个  的距离为
的距离为  ,请计算
,请计算  。
。 

 离子。I
离子。I 
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为  )。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为。
)。该吡啶和嘌呤中都含有大π键,则该吡啶中的大π键表示为。
 )
)


