近三年高考化学真题分类汇编:化学键与物质的性质(2021年)
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列含有共价键的盐是( )
A . CaCl2
B . H2SO4
C . Ba(OH)2
D . Na2CO3
|
|
| 2. 单选题 | 详细信息 |
|
有关
 的说法错误的是( ) 的说法错误的是( )
A . 分子中至少有12个原子共平面
B . 完全水解后所得有机物分子中手性碳原子数目为1个
C . 与FeCl3溶液作用显紫色
D . 与足量NaOH溶液完全反应后生成的钠盐只有1种
|
|
| 3. 综合题 | 详细信息 | ||||||||
|
|||||||||
| 4. 综合题 | 详细信息 |
|
[化学——选修3:物质结构与性质]
过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用,回答下列问题:
|
|
| 5. 综合题 | 详细信息 | ||||||||
|
[选修3:物质结构与性质]
KH2PO4晶体具有优异的非线性光学性能。我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
|
|||||||||
| 6. 综合题 | 详细信息 | |||||||||||||||
|
[选修3:物质结构与性质]
硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
|
||||||||||||||||
| 7. 单选题 | 详细信息 |
|
W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是( )
A . 原子半径:
 B . W与X只能形成一种化合物
C . Y的氧化物为碱性氧化物,不与强碱反应
D . W、X和Z可形成既含有离子键又含有共价键的化合物
B . W与X只能形成一种化合物
C . Y的氧化物为碱性氧化物,不与强碱反应
D . W、X和Z可形成既含有离子键又含有共价键的化合物
|
|
| 8. 综合题 | 详细信息 |
|
[化学-选修3:物质结构与性质]
我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
|
|
| 9. 综合题 | 详细信息 |
|
[选修3:物质结构与性质]
很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
|
|
| 10. 单选题 | 详细信息 |
|
下列“类比”结果不正确的是( )
A .
 的热稳定性比 的热稳定性比  的弱,则 的弱,则  的热稳定性比 的热稳定性比  的弱
B . 的弱
B .  的分子构型为V形,则二甲醚的分子骨架( 的分子构型为V形,则二甲醚的分子骨架(  )构型为V形
C . )构型为V形
C .  的溶解度比 的溶解度比  的大,则 的大,则  的溶解度比 的溶解度比  的大
D . 将丙三醇加入新制 的大
D . 将丙三醇加入新制  中溶液呈绛蓝色,则将葡萄糖溶液加入新制 中溶液呈绛蓝色,则将葡萄糖溶液加入新制  中溶液也呈绛蓝色 中溶液也呈绛蓝色
|
|
- 四川省内江市2017-2018学年高三理综-化学三模考试试卷
- 广西北流市实验中学2019-2020学年高二下学期化学期中考试试卷
- 甘肃省兰州市2017-2018学年高考理综-化学二模考试试卷
- 高中化学鲁科版(2019)必修第二册 第1章第3节 元素周期表的应用
- 湖南省岳阳市2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年吉林省吉林二中高一上学期期中化学试卷
- 人教版高中化学选修五 第一章第一节:有机化合物的分类
- 河南省驻马店市2019-2020学年高二下学期化学期末考试试卷
- 备考2020年高考化学二轮专题 01化学用语
- 2015年湖南省长沙市高考化学模拟试卷(4月份)
- 第9讲:碳族元素 无机非金属材料
- 广西靖西市第二中学2019-2020学年高二下学期化学开学考试卷
- 现有50 ℃硝酸钾饱和溶液,欲使其成为不饱和溶液,下列可采用的方法有()。 ①降低温度;②升高温度;③增加溶质;④减少溶
- 下列哪项比例不符合1:3() A.基因型为Aa的初级卵母细胞经过减数分裂后形成的卵细胞和极体个数之比 B.一对相对性状遗
- 已知f(x)为二次函数,且f(0)=2,f(x+1)﹣f(x)=x﹣1,求f(x).
- 如图,△ABC是等腰直角三角形,,BC=AC,直角顶点C在x轴上,一锐角顶点B在y轴上。 (1)如图①,若点C的坐标是(
- 已知正比例函数y=(m-1)x,若y随x增大而增大,则点(m,1-m)所在的象限是( ) A.第一象限
- 人类的红绿色盲基因位于X染色体上,母亲为携带者,父亲色盲,生下4个孩子,其中一个正常且不带致病基因,WWW.K**S*8
- 从以下表格内,选出适当的单词完成句子,使句子意思通顺。festival, twelfth, students,
- 如图所示是银杏树上结的“白果”,对白果的描述正确的是( )A.白果是银杏的种子,成熟时果皮脱落 B.白果是银杏的
- 邵阳市某学校举行以解决“白色污染”为题的主题班会.会上,同学们发言踊跃,说法众多.下列说法错误的是()A.禁止使用塑料制
- 下列划线字注音全对的一项( )(3分)A.荒谬(miào) 震悚(shǒng)溃退 (kuì) 锐不可当(dān
- 在中国近代史上,共和政体确立的标志是() A.湖北军政府成立 B.南京临时政府成立 C.清帝退位 D.袁世凯当选
- 地球上一年内昼夜变化最大的地区是( )A.赤道地区
- 物质的分离、提纯对于人类的生产、生活和科学研究具有十分重要的意义。下面除去物质中杂质的方法,正确的是( ) A.
- 中国人待客时“聊备薄酒”的自谦,可能被外国人误解为“慢待客人”;西方人聚餐时各付各的账,往往被东方人视为吝啬小气;东西方
- 下表为2011年中国、巴西、印度和印度尼西亚四个国家的城市人口占总人口比重表,读表完成11-12题。11.表中序号代表巴
- 不等式的整数解有( )个。
- 阅读下面的选文,回答问题。 宝钗见他羞得满脸飞红,满口央告,便不肯再往下追问,因拉他坐下吃茶,款款的告诉他道:“
- 下列加点字注音完全正确的一组是 ( ) (2分) A.痴想(chī) 隐秘(mì) 凝成(
- 人类双眼皮为显性,单眼皮为隐性。某年轻夫妇均为单眼皮,生了一个单眼皮的女孩。后来母亲去美容院通过外科手术变成了双眼皮,该
- 实验室常用下列装置制取气体,请你根据所学知识回答下列问题。(1)A装置经过改进可以进行木炭还原氧化铜的实验,你的改进方法


 和
和  ,则金属原子空间占有率为%(列出计算表达式)。
,则金属原子空间占有率为%(列出计算表达式)。
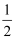 表示,与之相反的用-
表示,与之相反的用-  )形式存在的原因是。
)形式存在的原因是。 电子总数相同的等电子体的分子式为。
电子总数相同的等电子体的分子式为。
 如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为。
如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为。 和K+ , KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO
和K+ , KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO 

 ,
, 



 ,其结构如图所示:
,其结构如图所示:
 键;
键; 、
、  、
、  三种元素形成的某化合物的晶胞示意图。
三种元素形成的某化合物的晶胞示意图。 
 ,则该晶体的密度
,则该晶体的密度 
 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 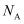 ,用含a、b、c、
,用含a、b、c、  含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2 , 中间体SiCl4(H2O)中Si采取的杂化类型为(填标号)。
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2 , 中间体SiCl4(H2O)中Si采取的杂化类型为(填标号)。 键和个
键和个  键。
键。






