中考化学试题
把少量下列物质分别放入水中,充分搅拌,可得到溶液的是
A . 牛奶
B . 面粉
C . 花生油
D . 葡萄糖
氢气是一种可持续研发的新能源和工业原料。
( 1 ) 利用太阳能将水转化为氢能是一种理想途径。某种光分解水的过程如图甲所示。


①该转化中循环利用的物质有 Fe 3 O 4 和 ______ (填化学式);
②与电解水相比,该方法的优点是 ______ 。
( 2 ) CH 2 ﹣ H 2 O 催化重整是目前大规模制取 H 2 的重要方法,生产过程中涉及的重要反应有 CH 4 +H 2 O 

①向催化重整体系中投入一定量的 CaO 可提高 H 2 的百分含量,原因是 ______ ;
②如图乙所示,投入纳米 CaO 时, H 2 的百分含量最大的原因是 ______ 。
( 3 ) 氢气可用于钢铁冶炼、合成氨和合成甲醇等工业。写出赤铁矿(主要成分为 Fe 2 O 3 )与氢气在高温下炼铁的化学方程式: ______ 。
大米、面粉中含有的糖类物质主要是淀粉,淀粉的化学式为 ______ (填 “ C 2 H 5 OH ”、“ C 6 H 12 O 6 ”或“( C 6 H 10 O 5 ) n”);施用化肥是农业增产的重要手段,尿素( CO(NH 2 ) 2 )属于 ______ (填 “氮肥”“磷肥”或“钾肥”)。
下列做法中一定发生化学变化的是( )
A.用石油分馏制得汽油、柴油等
B.用碱和树叶制作“叶脉书签”
C.用钢丝球擦除灶具上的污渍
D.用汽油清洗衣服上的油污
小云通过探究发现, 氯酸钾与氧化铜 (CuO) 或氧化铁 ( ) 混合加热,也能较快产生氧气,于是进行如下探究 :

(查阅资料)氯酸钾的熔点为 356°C ,常温下稳定,在 400°C 以上则分解产生氧气。酒精灯加热温度为 400°C ~ 500°C 。
(提出猜想)除 

也可以作氯酸钾分解的催化剂。
(完成实验)按如表进行实验并测定分解温度。 ( 分解温度越低,催化效果越好 ) 。
| 实验编号 | 实验药品 | 分解温度 |
| 1 | 3.0g 氯酸钾 | 460°C |
| 2 | 3.0g 氯酸钾和 0.5g 二氧化锰 | 248°C |
| 3 | 3.0g 氯酸钾和 0.5g 氧化铜 | 267°C |
| 4 | 3.0g 氯酸钾和 xg 氧化铁 | 290°C |
(分析数据,得出结论)
( 1 ) 实验 4 中 x 的值应为 _______ ,由实验 ______ 与实验 4 相比,证明猜想合理 .
( 2 ) 小云从如图中选择该实验的最佳发生装置是 ________ ( 填字母 ) ,该装置的优点是 ______________ 。
( 3 ) 实验 3 的符号表达式为 : __________ ;
( 4 ) 同种催化剂还有哪些因素会影响催化效果,请写出一种因素并设计实验方案进行验证 :
影响因素 : ______________ ;
实验方案 : ______________ ;
回收含铜废料 ( 主要成分为 Cu) 中的铜,部分实验流程如下:
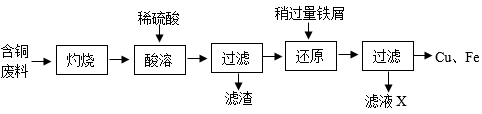
注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
下列关于该流程的说法,错误的是
A . “ 灼烧 ” 的主要目的是将 Cu 转变为 CuO B . 滤液 X 中的溶质为 FeSO 4
C . “ 酸溶 ” 和 “ 还原 ” 过程中发生的反应均为置换反应 D . 将 Cu 、 Fe 混合物加入足量稀硫酸中,充分反应后过滤得 Cu
火药是我国的四大发明之一,已知黑火药爆炸的化学方程式为: 
A . 硝酸钾中的硝酸根离子: 
C . 单质硫中硫元素的化合价: 
除去下列物质中的少量杂质(括号内为杂质),其操作不正确的是
A. Cu粉(Fe粉)------用磁铁吸引
B. N2(O2)-------将混合气体通过灼热的铜丝网
C. CO(CO2)------将混合气体通过灼热的氧化铁粉末
D. MnO2(KCI)------将混合物溶解于水、过滤、洗涤、干燥
元素之间的根本区别是原子的()
A. 核内质子数不同 B. 核外电子数不同
C. 核内中子数不同 D. 相对 原子质量不同
物质世界处处离不开化学。以下说法正确的是
①氮气可作食品保鲜的保护气
②汽油去除油污是因为乳化作用
③合成橡胶和塑料都属于合成材料
④河水经过沉降、过滤、杀菌消毒、蒸馏等净化过程得到自来水
⑤石油和酒精是不可再生资源,应加以综合利用
A . ①② B . ③⑤ C . ①③ D . ④⑤
小明发现铜质水龙头表面出现了一层绿色物质,小鹏和同学们特别好奇,决定对该绿色物质进行探究。
(查阅资料)铜长期暴露在潮湿的空气中会生锈,表面有绿色物质生成,俗称铜绿,主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。
探究一:铜在什么条件下会生锈
(提出猜想)同学们对空气中参与铜生锈的物质提出以下猜想:
猜想①:O2
猜想②:H2O
猜想③:N2
(交流讨论)经过讨论后,同学们一致认为猜想______________不合理,请解释理由_____________。
(拓展提升)除上述猜想外,你认为参与铜生锈的物质可能还有_____________。
探究二:铜绿的化学性质
(实验1)小芳同学取一定量干燥的铜绿放在试管中隔绝空气加热,如图所示。一段时间后,观察到绿色粉末逐渐变成黑色,试管口有无色液滴生成,且烧杯中的澄清石灰水变浑浊;请你用化学方程式解释澄清石灰水变浑浊的原因_______________。

(实验2)小华同学另取一定量的铜绿于试管中,加入适量的稀盐酸,可观察到的现象是_____________。
(得出结论)根据小芳、小华同学的实验,同学们总结出铜绿的化学性质为:①铜绿受热易分解;②铜绿能与稀盐酸反应。
(反思交流)同学们从安全角度考虑,认为小芳同学在结束实验1时,应该进行的操作是_________。
(拓展应用)①小明发现不同地点收集的两个铜器(一个是纯铜做的,一个是表铜做的),纯铜器的铜绿比青铜器的少,他据此分析铜比纯铜易锈蚀,小明的分析是否全面?请你说明理由_______________。
②日常生活中为防止铜制品、铁制品的生锈,应保持其表面洁净和干燥;在金属表面涂保护层;镀一层不易生锈的金属;改变金属的组成和结构。
物质变化是化学研究的重要内容。下列变化中与其他三种变化有本质区别的是
A. 活性炭净水 B. 工业制氧气 C. 干冰制冷 D. 工业炼铁
如图为枣庄市某中学的午餐食谱:

下列说法正确的是( )
A.牛肉富含淀粉 B.番茄富含维生素 C.花生油富含纤维素 D.米饭富含蛋白质
如图是元素周期表的部分信息。

完成下列填空:
(1)H+核外电子数为_______;
(2)写出一条第三周期元素原子的核外电子排布规律_____________;
(3)第 7 号元素与第 12 号元素的原子形成化合物的化学式为_______________;
(4)X、Y、Z、W 元素表示 4 种物质,它们的微观示意图如图:

物质 X 和 Y 在高温和催化剂条件下反应生成 Z 和 W 两种物质,反应的化学方程式为________。
安全意识是人类生存所必须具有的基本素质之一,下列实验操作比较安全的是( )
A. 用鼻子湊到容器口直接嗅闻未知气体的气味
B. 用嘴品尝未知物质的味道
C. 进入久未开启的菜窖、干涸的深井和深洞前,要做灯火试验
D. 发现家里煤气泄漏时,应立即打开排气扇
由Na2SO4、Na2SO3,Na2S三种物质组成的混合物中,测得氧元素质量分数为22% ,则其中硫元素的质量分数为
A.无法确定 B.23% C.45% D.32%
某化验室用20%的氢氧化钠溶液洗涤一定量工业产品中残余的H2SO4(工业产品及其他杂质都不与氢氧化钠溶液反应),当恰好完全反应时,共消耗氢氧化钠溶液80g,求产品中残余的H2SO4质量和生成硫酸钠的质量。
在一定条件下,下列物质的转化不能一步实现的是( )
A.Fe→Fe3O4 B.CuSO4→Cu C.CO2→CO D.H2O2→H2
(2020·南宁模拟)生活中处处有化学,下列变化属于化学变化的是( )
A. 榨果汁 B. 铁生锈 C. 糖溶于水 D. 汽油挥发
高锰酸钾是实验室制取氧气的一种原料,其中所含锰的原子结构示意图如右,下列与高锰酸钾及锰有关的说法中正确的是( )
A.锰原子易失去电子
B.锰的相对原子质量是 25
C.高锰酸钾中锰的化合价是+6
D.排水法收集氧气时应先熄火酒精灯,后将导管离开水槽

- 某一年,农民甲开展多种经营,承包土地年收入3万元,利用业余时间炒股嫌得2万元,用自己的私家货车跑运输得到报酬4万元。那么
- 某材料显示:清前期,景德镇民窑接受欧洲人的定制,并经由荷兰人运往欧洲,器型种类包括西式餐具或人物饰像等。对于该材料的解读
- 从下图《变动着的市场价格》可以得出的合理结论有 ①如果高档耐用品在N点,其替代产品需求量增加②如果生活必需品在M点,
- 肉毒碱(化学式为C7H15NO3)是一种具有多种生理功能的物质,被公认为人体必需的营养物质和最佳的减肥营养素。下列关于
- 下列实验基本操作中正确的是 A.闻气味 B.熄灭酒精灯C.滴加液体D.倾倒液体
- 完形填空。 “Nancy,try to cook for us today,” my mother called.“Bu
- 现代类人猿和人类的共同祖先是( ) A.东非人 B.森林古猿 C.长臂猿 D.北京人
- 如图,在△ABC中,AB=AC,AE是∠BAC的平分线,∠ABC的平分线 BM交AE于点M,点O在AB上,以点O为圆心,
- 细菌相对于真菌,明显不同的特点是( ) A.能分解动植物遗体
- 下列措施不合理的是()A.用SO2漂白纸浆和草帽辫 B.用硫酸清洗锅炉中的水垢 C.高温下用焦
- 下列各句中,没有语病的一句是 A、有关部门对极少数不尊重环卫工人劳动、无理取闹的事件,及时进行了批评教育和严肃处理。
- 右图是耸立在国家博物馆北广场的孔子青铜雕像,它成为天安门地区的文化新地标。下列有关孔子的说法不符合史实的是A.春秋时期鲁
- 下图为我国某区域多年平均气温分布图(单位:℃),读图回答下面试题。 影响图示地区气温分布的主要因素是 A.纬度因素
- 21.下列叙述正确的是()A.同周期元素中,ⅦA族元素的原子半径最大B.ⅥA族元素的原子,其半径越大,越容易得到电子C.
- 如图所示,当神经冲动在轴突上传导时,下列叙述错误的是 A.丁区域发生K+外流和Na+内流 B.甲区与丙区可能刚恢复为静息
- 皇帝主要通过奏事、朝议、刺察等形式掌握全国的军政信息,控制和指挥着整个国家机器的运转。秦朝时期能够参加朝议的官员不包括
- Mr Li began to teach in this school, _______, some time late
- 1)实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验.①图中仪器d的名称是:. ②要制取较多的O2用来探究其性质
- 在高温环境下排尿少的原因是( ) A.消化道在高温条件下吸水能力差 B.代谢消耗水分增多
- 阅读下面两段文言文,完成1-3题。(共20分,选择题每小题3分) (一) 张良出,要项伯。项伯即入见沛公。沛公奉卮酒为寿



